19. 高锰酸钾是一种重要的氧化剂,某化学实验小组制备高锰酸钾并测其纯度的步骤如图,请回答相关问题:
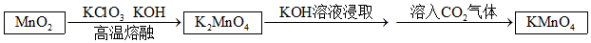
I.高锰酸钾的制备
(1)将4g KClO
3和7.5g KOH固体混匀放入坩埚中,边加热边搅拌,待熔融后慢慢加入5g MnO
2粉末,不断搅拌,呈颗粒状后,再加强热10min得墨绿色产物(K
2MnO
4为墨绿色固体),冷却。
①制K
2MnO
4反应的化学方程式为
_________。
②本实验中使用的坩埚及搅拌棒的材质可以是
___________。
A.石英
B.瓷
C.刚玉(氧化铝)
D.铁
(2)取出墨绿色产物研细,每次用10mL 4%的热KOH溶液浸取,过滤后对滤渣重复浸取两次。合并三次浸取液,得墨绿色溶液。将墨绿色产物研细并分三次浸取,这样做的目的是
____。
(3)K
2MnO
4在水溶液中会发生歧化反应:3K
2MnO
4+2H
2O

2KMnO
4+MnO
2↓+4KOH,通入CO
2气体可促进反应趋于完全。向(2)制得的墨绿色溶液中连续通入CO
2气体至溶液pH在10~11之间,过滤。滤液中的溶质除KMnO
4外,还主要含有杂质
_____。
II.高锰酸钾纯度的测定
(4)称取
mg KMnO
4粗品,加入煮沸并冷却后的稀硫酸配成
V0 mL溶液。量取
V1 mL
c1 mol/L的草酸(H
2C
2O
4)溶液于锥形瓶中,用所配KMnO
4溶液进行滴定。重复滴定两次,平均消耗KMnO
4溶液的体积为
V2mL。
①滴定开始时,溶液颜色褪去较慢,随后加快,原因是
_______。
②滴定终点的标志是
________。
③KMnO
4纯度(质量分数)的计算式为
____________。