名校
1 . 根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 实验结论 |
A | 将 溶液与 溶液与 溶液混合,生成白色 溶液混合,生成白色 沉淀 沉淀 | 结合质子能力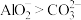 |
B | 将溴乙烷和氢氧化钠的乙醇溶液共热后产生的气体通入酸性 溶液,溶液褪色 溶液,溶液褪色 | 溴乙烷发生消去反应 |
C | 向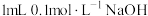 溶液中加入 溶液中加入 溶液,振荡后滴加 溶液,振荡后滴加 葡萄糖溶液,加热,无砖红色沉淀 葡萄糖溶液,加热,无砖红色沉淀 | 葡萄糖中不含有醛基 |
D | 向淀粉溶液中加适量20%的 溶液,加热,冷却后加 溶液,加热,冷却后加 溶液至中性,再滴加碘水,溶液变蓝 溶液至中性,再滴加碘水,溶液变蓝 | 淀粉未水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 根据下列实验事实能得出相应结论的是
| 选项 | 实验事实 | 结论 |
| A | 常温下,分别向等体积 的盐酸和硫酸中加入大小相同的铝片,前者反应速率更快 的盐酸和硫酸中加入大小相同的铝片,前者反应速率更快 | 酸性: |
| B | 常温下,向0.1 mol/L  溶液中滴加酚酞,不变红 溶液中滴加酚酞,不变红 |  不能发生水解 不能发生水解 |
| C | 常温下,分别向浓度均为0.1 mol/L的 和 和 溶液中通入 溶液中通入 气体至饱和,仅后者生成沉淀 气体至饱和,仅后者生成沉淀 | 溶度积常数: |
| D | 向酸性 溶液中滴加苯甲醛,溶液褪色 溶液中滴加苯甲醛,溶液褪色 | 苯甲醛有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 室温下,向 溶液中加入足量氨水
溶液中加入足量氨水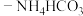 混合溶液,生成
混合溶液,生成 沉淀。已知:
沉淀。已知: ,
,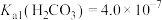 ,
,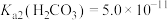 。下列说法正确的是
。下列说法正确的是
 溶液中加入足量氨水
溶液中加入足量氨水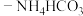 混合溶液,生成
混合溶液,生成 沉淀。已知:
沉淀。已知: ,
,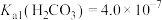 ,
,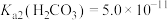 。下列说法正确的是
。下列说法正确的是A.生成 的离子方程式: 的离子方程式: |
B.0.1   溶液中:( 溶液中:( ): ):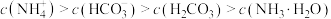 |
C.0.2  氨水和0.2 氨水和0.2   溶液等体积混合: 溶液等体积混合: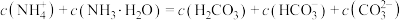 |
D.生成 沉淀后的滤液中: 沉淀后的滤液中: |
您最近一年使用:0次
名校
4 . 以磷石膏(含CaSO4和少量SiO2等)为原料制备轻质CaCO3的部分流程如图12图所示。室温下,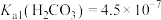 ,
,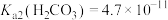 ,
, 。
。
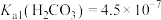 ,
,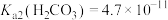 ,
, 。
。
A. 溶液中: 溶液中: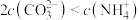 |
B.室温下,pH=6的NH4Cl溶液中: |
C.“转化”后的清液中一定存在 |
D.“浸取”发生反应 |
您最近一年使用:0次
2024-05-14更新
|
261次组卷
|
3卷引用:江苏省南京市2024届高三下学期第二次模拟考试化学试题
5 . 室温下,探究 溶液的性质。下列实验方案能达到探究目的的是
溶液的性质。下列实验方案能达到探究目的的是
 溶液的性质。下列实验方案能达到探究目的的是
溶液的性质。下列实验方案能达到探究目的的是| 选项 | 探究目的 | 实验方案 |
| A | 验证溶液中含有 | 向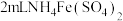 溶液中滴加几滴 溶液中滴加几滴 溶液,将湿润的红色石蕊试纸靠近试管口,观察试纸颜色变化 溶液,将湿润的红色石蕊试纸靠近试管口,观察试纸颜色变化 |
| B | 溶液中是否含有 | 向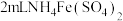 溶液中滴加几滴新制氯水,再滴加KSCN溶液,观察溶液的颜色变化 溶液中滴加几滴新制氯水,再滴加KSCN溶液,观察溶液的颜色变化 |
| C |  是否发生水解 是否发生水解 | 用玻璃棒蘸取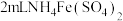 溶液滴在干燥的广泛pH试纸上,将试纸显色的颜色与标准比色卡比较 溶液滴在干燥的广泛pH试纸上,将试纸显色的颜色与标准比色卡比较 |
| D |  是否具有氧化性 是否具有氧化性 | 向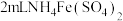 溶液中滴加几滴 溶液中滴加几滴 溶液,再滴加淀粉溶液,观察溶液颜色变化 溶液,再滴加淀粉溶液,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-14更新
|
262次组卷
|
2卷引用:江苏省南京市2024届高三下学期第二次模拟考试化学试题
6 . 部分弱电解质的电离常数如表所示。
下列说法错误的是
| 弱电解质 | HCOOH | HCN | H2CO3 |
| 电离常数(25℃) | Ka=1.8×10-4 | Ka=6.2×10-10 |  =4.5×10-7 =4.5×10-7 =4.7×10-11 =4.7×10-11 |
A.结合H+的能力: >CN-> >CN-> >HCOO- >HCOO- |
B.反应2CN-+H2O+CO2=2HCN+C 能发生 能发生 |
| C.中和等体积、等c(H+)的HCOOH和HCN,消耗NaOH的量前者小于后者 |
D.25℃时,反应HCOOH+CN- HCN+HCOO-的化学平衡常数约为2.9×105 HCN+HCOO-的化学平衡常数约为2.9×105 |
您最近一年使用:0次
7 . 下列实验方案能达到探究目的的是
| 选项 | 探究目的 | 实验方案 |
| A |  溶液发生了水解反应 溶液发生了水解反应 | 向 溶液中滴加少量 溶液中滴加少量 溶液,观察现象(已知: 溶液,观察现象(已知: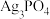 为黄色沉淀) 为黄色沉淀) |
| B | 酸性: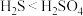 | 向 溶液中通入 溶液中通入 气体,观察现象 气体,观察现象 |
| C |  在浓KI溶液中的溶解能力大于在 在浓KI溶液中的溶解能力大于在 中的溶解能力 中的溶解能力 | 向 的 的 溶液中加入等体积浓KI溶液,振荡,观察现象 溶液中加入等体积浓KI溶液,振荡,观察现象 |
| D |  中含有Fe(II) 中含有Fe(II) | 将 溶于盐酸所得溶液浓缩后,滴入酸性 溶于盐酸所得溶液浓缩后,滴入酸性 溶液,观察溶液颜色的变化 溶液,观察溶液颜色的变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 室温下,通过下列实验探究某些碳酸盐溶液及碳酸氢盐溶液的性质。
已知: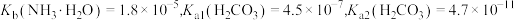 。
。
下列有关说法正确的是
已知:
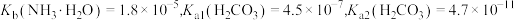 。
。| 实验 | 实验操作和现象 |
| 1 | 测量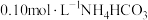 溶液的 溶液的 ,测得 ,测得 为 为 |
| 2 | 测量某浓度的 溶液的 溶液的 ,测得 ,测得 约为9.4 约为9.4 |
| 3 | 将两种浓度均为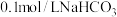 和 和 溶液等体积混合,测量其 溶液等体积混合,测量其 |
A.实验1溶液中: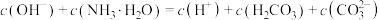 |
B.实验1测得的 值 值 |
C.实验2溶液中: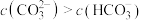 |
D.实验3所得溶液中: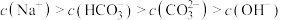 |
您最近一年使用:0次
9 . 草酸是植物(特别是草本植物)常具有的成分,有广泛的用途。草酸晶体( )无色,熔点为101℃,易溶于水。常温下草酸的电离常数
)无色,熔点为101℃,易溶于水。常温下草酸的电离常数 ,
, 。
。
(1)写出草酸第一步电离方程式:______
(2)草酸具有很强的还原性,与氧化剂作用易被氧化成二氧化碳和水,可以使酸性高锰酸钾( )溶液褪色,写出发生反应的离子方程式:
)溶液褪色,写出发生反应的离子方程式:______ 。为了探究浓度对化学反应速率的影响,相同温度条件下,分别用2支试管设计了如下实验:
此实验中,加入 溶液的体积应为
溶液的体积应为______ mL。
(3)结合题干所给的电离平衡常数,判断 溶液的酸碱性,应显
溶液的酸碱性,应显______ 性(填“酸”或“碱”)。
(4)设计实验证明草酸为弱酸的方案及其现象均正确的有______(填序号)。
(5)为测定某 溶液的浓度,取20.00mL
溶液的浓度,取20.00mL 溶液于锥形瓶中,滴入2~3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL。
溶液于锥形瓶中,滴入2~3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL。
①若所用指示剂为酚酞,则滴定终点时的现象为______ ;
② 溶液物质的量浓度为
溶液物质的量浓度为______ mol/L;
③下列操作会引起测定结果偏高的是______ (填序号)。
A.滴定管在盛装NaOH溶液前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.锥形瓶水洗后未干燥
D.滴定前读数正确,滴定终点时仰视读数
 )无色,熔点为101℃,易溶于水。常温下草酸的电离常数
)无色,熔点为101℃,易溶于水。常温下草酸的电离常数 ,
, 。
。(1)写出草酸第一步电离方程式:
(2)草酸具有很强的还原性,与氧化剂作用易被氧化成二氧化碳和水,可以使酸性高锰酸钾(
 )溶液褪色,写出发生反应的离子方程式:
)溶液褪色,写出发生反应的离子方程式:试管 | A | B |
加入试剂 | 4mL 0.01moL/L | ______0.02moL/L |
1mL 0.1moL/L | 1mL 0.1moL/L | |
2mL 0.1moL/L | 2mL 0.1moL/L |
 溶液的体积应为
溶液的体积应为(3)结合题干所给的电离平衡常数,判断
 溶液的酸碱性,应显
溶液的酸碱性,应显(4)设计实验证明草酸为弱酸的方案及其现象均正确的有______(填序号)。
A.室温下,取0.01mol/L 溶液,测其pH=2; 溶液,测其pH=2; |
B.室温下,取0.01mol/L 溶液,测其pH>7; 溶液,测其pH>7; |
C.室温下,取pH=a( )的 )的 溶液稀释100倍后,测其 溶液稀释100倍后,测其 ; ; |
D.标况下,取0.1moL/L的 溶液100mL与足量锌粉反应,收集到 溶液100mL与足量锌粉反应,收集到 体积为224mL; 体积为224mL; |
 溶液的浓度,取20.00mL
溶液的浓度,取20.00mL 溶液于锥形瓶中,滴入2~3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL。
溶液于锥形瓶中,滴入2~3滴指示剂,用0.1000mol/L的NaOH溶液进行滴定,并进行3次平行实验,所用NaOH溶液体积分别为19.98mL、20.02mL和22.02mL。①若所用指示剂为酚酞,则滴定终点时的现象为
②
 溶液物质的量浓度为
溶液物质的量浓度为③下列操作会引起测定结果偏高的是
A.滴定管在盛装NaOH溶液前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.锥形瓶水洗后未干燥
D.滴定前读数正确,滴定终点时仰视读数
您最近一年使用:0次
解题方法
10 . 氯化镍(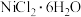 )常用于电镀、陶瓷等工业,某实验室以单质Ni为原料制取氯化镍的实验步骤如下:
)常用于电镀、陶瓷等工业,某实验室以单质Ni为原料制取氯化镍的实验步骤如下: 完全沉淀pH为3.2;
完全沉淀pH为3.2; 开始沉淀pH为7.2,完全沉淀pH为9.2。
开始沉淀pH为7.2,完全沉淀pH为9.2。
② 易水解,从溶液中获取
易水解,从溶液中获取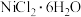 须控制pH<2。
须控制pH<2。
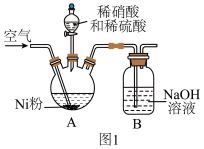
(1)在三颈烧瓶中(装置见图1)加入一定量Ni粉和水,通入空气,滴入稀硝酸和稀硫酸的混酸,至反应结束,过滤,制得 溶液。
溶液。
①向A装置中通入空气的作用除搅拌外还有___________ 。
②若镍粉过量,判断反应完成的现象是___________ 。 溶液与
溶液与 溶液混合反应得到
溶液混合反应得到 沉淀,过滤,洗涤。
沉淀,过滤,洗涤。
①沉淀反应的离子方程式为___________ 。
②检验 沉淀已经洗涤完全的方法是
沉淀已经洗涤完全的方法是___________ 。
(3)所得 固体中混有少量
固体中混有少量 。
。
请补充完整由 固体制备
固体制备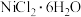 的实验方案:
的实验方案:
向 固体中加入盐酸,搅拌,
固体中加入盐酸,搅拌,___________ 。
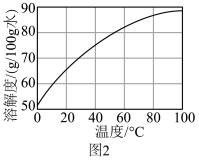
[ 溶解度曲线如图2所示。实验中
溶解度曲线如图2所示。实验中须 选用的仪器和试剂:pH计、盐酸、冰水、 ]
]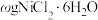 晶体产品于锥形瓶中,加入足量的蒸馏水溶解配成250mL溶液,取25.00mL所配溶液于锥形瓶中,用
晶体产品于锥形瓶中,加入足量的蒸馏水溶解配成250mL溶液,取25.00mL所配溶液于锥形瓶中,用 的标准溶液EDTA(
的标准溶液EDTA( )滴定至终点(发生反应
)滴定至终点(发生反应 ),四次实验消耗标准液的体积分别为20.02mL、19.98mL、19.60mL,20.00mL则
),四次实验消耗标准液的体积分别为20.02mL、19.98mL、19.60mL,20.00mL则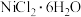 的纯度为
的纯度为___________ %(只列计算式,不考虑杂质反应)。
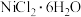 )常用于电镀、陶瓷等工业,某实验室以单质Ni为原料制取氯化镍的实验步骤如下:
)常用于电镀、陶瓷等工业,某实验室以单质Ni为原料制取氯化镍的实验步骤如下:
 完全沉淀pH为3.2;
完全沉淀pH为3.2; 开始沉淀pH为7.2,完全沉淀pH为9.2。
开始沉淀pH为7.2,完全沉淀pH为9.2。②
 易水解,从溶液中获取
易水解,从溶液中获取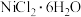 须控制pH<2。
须控制pH<2。(1)在三颈烧瓶中(装置见图1)加入一定量Ni粉和水,通入空气,滴入稀硝酸和稀硫酸的混酸,至反应结束,过滤,制得
 溶液。
溶液。①向A装置中通入空气的作用除搅拌外还有
②若镍粉过量,判断反应完成的现象是
 溶液与
溶液与 溶液混合反应得到
溶液混合反应得到 沉淀,过滤,洗涤。
沉淀,过滤,洗涤。①沉淀反应的离子方程式为
②检验
 沉淀已经洗涤完全的方法是
沉淀已经洗涤完全的方法是(3)所得
 固体中混有少量
固体中混有少量 。
。请补充完整由
 固体制备
固体制备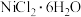 的实验方案:
的实验方案:向
 固体中加入盐酸,搅拌,
固体中加入盐酸,搅拌,[
 溶解度曲线如图2所示。实验中
溶解度曲线如图2所示。实验中 ]
]
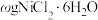 晶体产品于锥形瓶中,加入足量的蒸馏水溶解配成250mL溶液,取25.00mL所配溶液于锥形瓶中,用
晶体产品于锥形瓶中,加入足量的蒸馏水溶解配成250mL溶液,取25.00mL所配溶液于锥形瓶中,用 的标准溶液EDTA(
的标准溶液EDTA( )滴定至终点(发生反应
)滴定至终点(发生反应 ),四次实验消耗标准液的体积分别为20.02mL、19.98mL、19.60mL,20.00mL则
),四次实验消耗标准液的体积分别为20.02mL、19.98mL、19.60mL,20.00mL则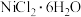 的纯度为
的纯度为
您最近一年使用:0次



