1 . 硼氢化钠 是一种理想的储氢材料。
是一种理想的储氢材料。
(1) 的制备
的制备
碱性条件下,电解偏硼酸钠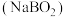 溶液可制备
溶液可制备 。总反应式为
。总反应式为 。已知:电负性B<H。
。已知:电负性B<H。
①写出阴极的电极反应式:__________ 。
②研究表面上述反应为间接还原反应,包括2步反应,请描述出这2步反应的合理假设:__________ 。
(2) 的性质
的性质
常温下, 在水溶液中将发生水解反应生成
在水溶液中将发生水解反应生成 ,
, 的半衰期(
的半衰期( 水解掉一半所耗费的时间,用
水解掉一半所耗费的时间,用 表示)与溶液pH、温度(T)的关系如下:
表示)与溶液pH、温度(T)的关系如下: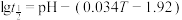 。
。
①写出 在水溶液发生水解反应的化学方程式:
在水溶液发生水解反应的化学方程式:__________ 。
②给出保存 水溶液的2点建议:
水溶液的2点建议:__________ 。
(3) 的运用
的运用
第四周期过渡金属及其化合物是催化 水解产氢的良好催化剂。
水解产氢的良好催化剂。
①Ag-铁基纳米颗粒催化剂可催化硼氢化钠水解制氢。相同条件下,控制 浓度相等,改变其中稳定剂
浓度相等,改变其中稳定剂 的浓度,测得
的浓度,测得 浓度对催化活性的影响如题图所示。
浓度对催化活性的影响如题图所示。 浓度相对过大催化活性下降的原因可能是
浓度相对过大催化活性下降的原因可能是__________ 。 、
、 、
、 催化
催化 水解制氢性能对比如下:
水解制氢性能对比如下:
根据表格,写出你所得到的结论:__________ 。
 是一种理想的储氢材料。
是一种理想的储氢材料。(1)
 的制备
的制备碱性条件下,电解偏硼酸钠
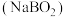 溶液可制备
溶液可制备 。总反应式为
。总反应式为 。已知:电负性B<H。
。已知:电负性B<H。①写出阴极的电极反应式:
②研究表面上述反应为间接还原反应,包括2步反应,请描述出这2步反应的合理假设:
(2)
 的性质
的性质常温下,
 在水溶液中将发生水解反应生成
在水溶液中将发生水解反应生成 ,
, 的半衰期(
的半衰期( 水解掉一半所耗费的时间,用
水解掉一半所耗费的时间,用 表示)与溶液pH、温度(T)的关系如下:
表示)与溶液pH、温度(T)的关系如下: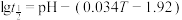 。
。①写出
 在水溶液发生水解反应的化学方程式:
在水溶液发生水解反应的化学方程式:②给出保存
 水溶液的2点建议:
水溶液的2点建议:(3)
 的运用
的运用第四周期过渡金属及其化合物是催化
 水解产氢的良好催化剂。
水解产氢的良好催化剂。①Ag-铁基纳米颗粒催化剂可催化硼氢化钠水解制氢。相同条件下,控制
 浓度相等,改变其中稳定剂
浓度相等,改变其中稳定剂 的浓度,测得
的浓度,测得 浓度对催化活性的影响如题图所示。
浓度对催化活性的影响如题图所示。 浓度相对过大催化活性下降的原因可能是
浓度相对过大催化活性下降的原因可能是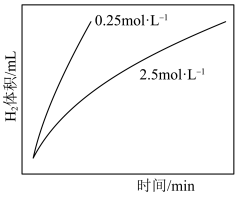
 、
、 、
、 催化
催化 水解制氢性能对比如下:
水解制氢性能对比如下:
|
|
| |
金属d电子数 | 6 | 7 | 8 |
反应活化能/ | 52.01 | 46.33 | 58.70 |
产氢速率 | 最慢 | 最快 | 较慢 |
您最近一年使用:0次
2024-06-06更新
|
69次组卷
|
2卷引用:江苏省南通市2023-2024学年高三下学期期中考试化学试题
名校
2 . 室温下,下列实验探究方案能达到探究目的的是
| 选项 | 探究目的 | 探究方案 |
| A | Ka(HClO)与Ka(HCN)的大小关系 | 用pH计测量NaClO溶液和NaCN溶液的pH,比较HClO和HCN的Ka大小 |
| B | 碘在浓KI溶液中与CCl4中的溶解能力比较 | 向碘的CCl4溶液中加入等体积浓KI溶液,振荡,观察有机层颜色的变化 |
| C | SO2是否具有漂白性 | 向盛有SO2水溶液的试管中滴加几滴KMnO4溶液,振荡,观察溶液颜色变化 |
| D | 探究1—溴丁烷的消去产物 | 向圆底烧瓶中加入2.0gNaOH、15mL无水乙醇、碎瓷片和5mL1-溴丁烷,微热,将产生的气体通入酸性KMnO4溶液,观察现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 探究卤族元素单质及其化合物的性质,下列实验方案能达到探究目的的是
| 探究目的 | 实验方案 | |
| A | I2在饱和KI溶液与CCl4中的溶解能力大小 | 向I2的CCl4溶液中加入等体积饱和KI溶液,振荡 |
| B | Cl与C的非金属性强弱 | 将稀盐酸滴入NaHCO3溶液中,将产生的气体通入澄清石灰水中 |
| C | AgCl与AgI溶度积大小 | 向2mL0.1mol∙L-1AgNO3溶液中先滴加4滴0.1mol∙L-1KCl溶液,再滴加4滴0.1mol∙L-1KI溶液 |
| D | HClO是否为弱酸 | 用玻璃棒蘸取NaClO溶液点在pH试纸上 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 铁及其化合物的转化具有重要应用。在指定条件下,下列物质间转化能实现的是
A.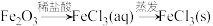 |
B.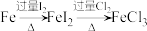 |
C.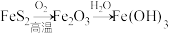 |
D.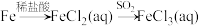 |
您最近一年使用:0次
解题方法
5 . 室温下,下列实验研究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 向葡萄糖溶液中滴加酸性 溶液, 溶液, 溶液红色褪去 溶液红色褪去 | 葡萄糖中含有醛基 |
| B | 向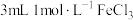 溶液逐滴加入同体积同浓度 溶液逐滴加入同体积同浓度 溶液,先出现红褐色沉淀,放置 溶液,先出现红褐色沉淀,放置 后沉淀消失,溶液变为绿色 后沉淀消失,溶液变为绿色 |  与 与 在水溶液中存在水解反应和氧化还原反应的竞争 在水溶液中存在水解反应和氧化还原反应的竞争 |
| C | 用pH试纸测定浓度均为 的 的 溶液和 溶液和 溶液的pH 溶液的pH | 比较 、 、 酸性相对强弱 酸性相对强弱 |
| D | 向CO还原 所得到的产物中加入稀盐酸,再滴加KSCN溶液,观察颜色变化 所得到的产物中加入稀盐酸,再滴加KSCN溶液,观察颜色变化 | CO还原 实验中, 实验中, 是否全部被还原 是否全部被还原 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 已知: 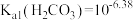 、
、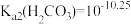 。室温下,通过下列实验探究NaHCO3溶液的性质。
。室温下,通过下列实验探究NaHCO3溶液的性质。
下列有关说法正确的是
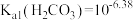 、
、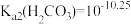 。室温下,通过下列实验探究NaHCO3溶液的性质。
。室温下,通过下列实验探究NaHCO3溶液的性质。| 实验 | 实验操作和现象 |
| 1 | 测量0.1mol·L-1的NaHCO3溶液的pH为7.8 |
| 2 | 向0.1mol·L-1的NaHCO3溶液中持续通入CO2,溶液的pH减小 |
| 3 | 向0.1mol·L-1的NaHCO3溶液中加入少量 溶液,产生白色沉淀 溶液,产生白色沉淀 |
| 4 | 向0.5mol·L-1的NaHCO3溶液中滴加少量0.5mol·L-1的CaCl2溶液,产生白色沉淀和无色气体 |
A.实验1溶液中存在: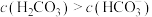 |
B.实验2中随CO2的不断通入,溶液中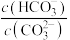 的值逐渐变小 的值逐渐变小 |
C.实验3反应的离子方程式为 |
D.实验4所得溶液中存在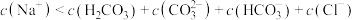 |
您最近一年使用:0次
名校
解题方法
7 . 室温下,向 溶液中加入足量氨水
溶液中加入足量氨水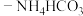 混合溶液,生成
混合溶液,生成 沉淀。已知:
沉淀。已知: ,
,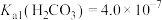 ,
,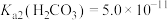 。下列说法正确的是
。下列说法正确的是
 溶液中加入足量氨水
溶液中加入足量氨水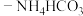 混合溶液,生成
混合溶液,生成 沉淀。已知:
沉淀。已知: ,
,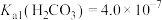 ,
,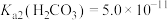 。下列说法正确的是
。下列说法正确的是A.生成 的离子方程式: 的离子方程式: |
B.0.1   溶液中:( 溶液中:( ): ):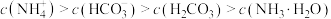 |
C.0.2  氨水和0.2 氨水和0.2   溶液等体积混合: 溶液等体积混合: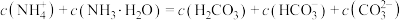 |
D.生成 沉淀后的滤液中: 沉淀后的滤液中: |
您最近一年使用:0次
8 . 室温下,探究 溶液的性质。下列实验方案能达到探究目的的是
溶液的性质。下列实验方案能达到探究目的的是
 溶液的性质。下列实验方案能达到探究目的的是
溶液的性质。下列实验方案能达到探究目的的是| 选项 | 探究目的 | 实验方案 |
| A | 验证溶液中含有 | 向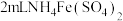 溶液中滴加几滴 溶液中滴加几滴 溶液,将湿润的红色石蕊试纸靠近试管口,观察试纸颜色变化 溶液,将湿润的红色石蕊试纸靠近试管口,观察试纸颜色变化 |
| B | 溶液中是否含有 | 向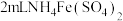 溶液中滴加几滴新制氯水,再滴加KSCN溶液,观察溶液的颜色变化 溶液中滴加几滴新制氯水,再滴加KSCN溶液,观察溶液的颜色变化 |
| C |  是否发生水解 是否发生水解 | 用玻璃棒蘸取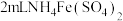 溶液滴在干燥的广泛pH试纸上,将试纸显色的颜色与标准比色卡比较 溶液滴在干燥的广泛pH试纸上,将试纸显色的颜色与标准比色卡比较 |
| D |  是否具有氧化性 是否具有氧化性 | 向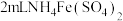 溶液中滴加几滴 溶液中滴加几滴 溶液,再滴加淀粉溶液,观察溶液颜色变化 溶液,再滴加淀粉溶液,观察溶液颜色变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 .  ,探究
,探究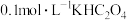 溶液的性质。下列实验方案能达到探究目的的是
溶液的性质。下列实验方案能达到探究目的的是
 ,探究
,探究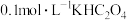 溶液的性质。下列实验方案能达到探究目的的是
溶液的性质。下列实验方案能达到探究目的的是| 选项 | 探究目的 | 实验方案 |
| A | 钾元素的焰色试验 | 用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色 |
| B |  是否有还原性 是否有还原性 | 向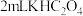 溶液中滴加氯水,再滴入 溶液中滴加氯水,再滴入 溶液,观察是否有白色沉淀产生 溶液,观察是否有白色沉淀产生 |
| C |  是否水解 是否水解 | 向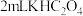 溶液中滴加2~3滴酚酞试液,观察溶液颜色的变化 溶液中滴加2~3滴酚酞试液,观察溶液颜色的变化 |
| D | 比较溶液中 与 与 的大小 的大小 | 用 计测量 计测量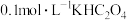 溶液的 溶液的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 以某石膏矿(主要成分是 ,含少量的
,含少量的 、
、 等杂质)为原料制备轻质
等杂质)为原料制备轻质 、
、 和
和 产品的工艺流程如下:
产品的工艺流程如下: 溶出。
溶出。
①“溶浸”时发生反应的化学方程式为______ 。
②“溶浸”时通常还加入一定量的氨水,加入氨水的作用是______ 。
③“溶浸”时, 的浸出率与
的浸出率与 的关系如图所示:
的关系如图所示:
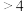 时,
时, 浸出率随着
浸出率随着 的增大而减小的原因是
的增大而减小的原因是______ 。
(2)将滤渣高温煅烧,冷却后用 溶液浸取,可生成硅酸、氢氧化铝、氯化钙等,氯化钙最终可生成轻质碳酸钙。
溶液浸取,可生成硅酸、氢氧化铝、氯化钙等,氯化钙最终可生成轻质碳酸钙。
①滤渣中含有的物质是______ 。
②在敞口容器中,用 溶液浸取高温煅烧的固体,随着浸取液温度上升,溶液中
溶液浸取高温煅烧的固体,随着浸取液温度上升,溶液中 增大的原因是
增大的原因是______ 。
(3)“盐化”过程中加入适量盐酸的目的是______ 。
(4) 、
、 的溶解度如图所示,“结晶”过程中先分离出
的溶解度如图所示,“结晶”过程中先分离出 晶体的方法是
晶体的方法是______ 。 的标准NaOH溶液滴定至终点,消耗NaOH溶液的体积19.40mL,已知:
的标准NaOH溶液滴定至终点,消耗NaOH溶液的体积19.40mL,已知: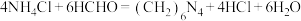 ,计算样品中
,计算样品中 的质量分数。
的质量分数。______ (写出计算过程)
 ,含少量的
,含少量的 、
、 等杂质)为原料制备轻质
等杂质)为原料制备轻质 、
、 和
和 产品的工艺流程如下:
产品的工艺流程如下: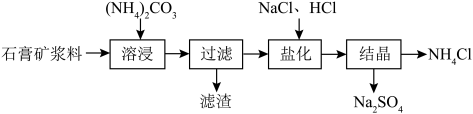
 溶出。
溶出。①“溶浸”时发生反应的化学方程式为
②“溶浸”时通常还加入一定量的氨水,加入氨水的作用是
③“溶浸”时,
 的浸出率与
的浸出率与 的关系如图所示:
的关系如图所示: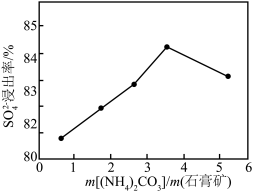

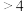 时,
时, 浸出率随着
浸出率随着 的增大而减小的原因是
的增大而减小的原因是(2)将滤渣高温煅烧,冷却后用
 溶液浸取,可生成硅酸、氢氧化铝、氯化钙等,氯化钙最终可生成轻质碳酸钙。
溶液浸取,可生成硅酸、氢氧化铝、氯化钙等,氯化钙最终可生成轻质碳酸钙。①滤渣中含有的物质是
②在敞口容器中,用
 溶液浸取高温煅烧的固体,随着浸取液温度上升,溶液中
溶液浸取高温煅烧的固体,随着浸取液温度上升,溶液中 增大的原因是
增大的原因是(3)“盐化”过程中加入适量盐酸的目的是
(4)
 、
、 的溶解度如图所示,“结晶”过程中先分离出
的溶解度如图所示,“结晶”过程中先分离出 晶体的方法是
晶体的方法是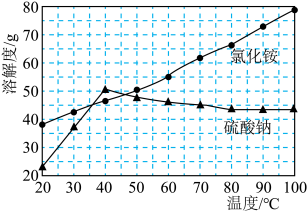
 的标准NaOH溶液滴定至终点,消耗NaOH溶液的体积19.40mL,已知:
的标准NaOH溶液滴定至终点,消耗NaOH溶液的体积19.40mL,已知: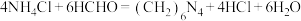 ,计算样品中
,计算样品中 的质量分数。
的质量分数。
您最近一年使用:0次




