名校
1 . 焦亚硫酸钠 常用作葡萄酒、果脯等食品的抗氧化剂,在空气中、受热时均易分解,某实验小组通过实验制备焦亚硫酸钠并测定焦亚硫酸钠的纯度。回答下列问题:
常用作葡萄酒、果脯等食品的抗氧化剂,在空气中、受热时均易分解,某实验小组通过实验制备焦亚硫酸钠并测定焦亚硫酸钠的纯度。回答下列问题:
I.焦亚硫酸钠的制备
实验室制备少量 的装置如图所示。
的装置如图所示。 左右,向
左右,向 过饱和溶液中通入
过饱和溶液中通入 ,当溶液的
,当溶液的 为4.1时,停止通入
为4.1时,停止通入 ,
, 静置结晶,经减压抽滤、洗涤、
静置结晶,经减压抽滤、洗涤、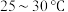 干燥,可获得
干燥,可获得 固体。
固体。
(1) 的VSEPR模型名称为
的VSEPR模型名称为__________ 。
(2)控制反应温度在 左右的原因是
左右的原因是_____________ 。
(3)装置 的作用是
的作用是__________ 。
(4)工业上亦可用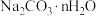 (固体)与
(固体)与 气体充分接触反应制备焦亚硫酸钠,此法常称为干法制备焦亚硫酸盐,写出反应的化学方程式:
气体充分接触反应制备焦亚硫酸钠,此法常称为干法制备焦亚硫酸盐,写出反应的化学方程式:_______________ 。
(5)因为 具有
具有_________ 性,所以产品 中不可避免地存在
中不可避免地存在 。检验产品中含有
。检验产品中含有 的方法是
的方法是_____________ 。
Ⅱ.焦亚硫酸钠纯度的测定
工业焦亚硫酸钠优质品要求焦亚硫酸钠的质量分数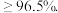 通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为
通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为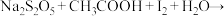
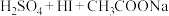 (未配平),
(未配平), 。
。
准确称取 样品,快速置于预先加入
样品,快速置于预先加入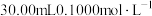 碘标准液及
碘标准液及 水的
水的 碘量瓶中,加入
碘量瓶中,加入 乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处
乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处 ,用
,用 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗 标准溶液
标准溶液 。
。
(6)滴定终点的现象是_____________ 。
(7)该样品中焦亚硫酸钠的质量分数为__________  ,
,__________ (填“是”或“不是”)优质品。
 常用作葡萄酒、果脯等食品的抗氧化剂,在空气中、受热时均易分解,某实验小组通过实验制备焦亚硫酸钠并测定焦亚硫酸钠的纯度。回答下列问题:
常用作葡萄酒、果脯等食品的抗氧化剂,在空气中、受热时均易分解,某实验小组通过实验制备焦亚硫酸钠并测定焦亚硫酸钠的纯度。回答下列问题:I.焦亚硫酸钠的制备
实验室制备少量
 的装置如图所示。
的装置如图所示。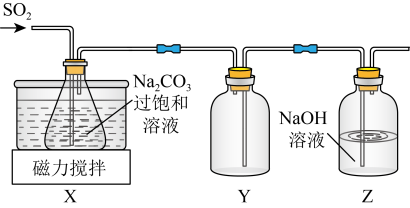
 左右,向
左右,向 过饱和溶液中通入
过饱和溶液中通入 ,当溶液的
,当溶液的 为4.1时,停止通入
为4.1时,停止通入 ,
, 静置结晶,经减压抽滤、洗涤、
静置结晶,经减压抽滤、洗涤、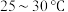 干燥,可获得
干燥,可获得 固体。
固体。(1)
 的VSEPR模型名称为
的VSEPR模型名称为(2)控制反应温度在
 左右的原因是
左右的原因是(3)装置
 的作用是
的作用是(4)工业上亦可用
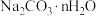 (固体)与
(固体)与 气体充分接触反应制备焦亚硫酸钠,此法常称为干法制备焦亚硫酸盐,写出反应的化学方程式:
气体充分接触反应制备焦亚硫酸钠,此法常称为干法制备焦亚硫酸盐,写出反应的化学方程式:(5)因为
 具有
具有 中不可避免地存在
中不可避免地存在 。检验产品中含有
。检验产品中含有 的方法是
的方法是Ⅱ.焦亚硫酸钠纯度的测定
工业焦亚硫酸钠优质品要求焦亚硫酸钠的质量分数
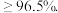 通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为
通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为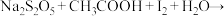
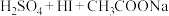 (未配平),
(未配平), 。
。准确称取
 样品,快速置于预先加入
样品,快速置于预先加入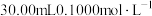 碘标准液及
碘标准液及 水的
水的 碘量瓶中,加入
碘量瓶中,加入 乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处
乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处 ,用
,用 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗 标准溶液
标准溶液 。
。(6)滴定终点的现象是
(7)该样品中焦亚硫酸钠的质量分数为
 ,
,
您最近一年使用:0次
昨日更新
|
131次组卷
|
3卷引用:2024届山西省晋城市高三下学期第三次模拟考试理科综合试题-高中化学
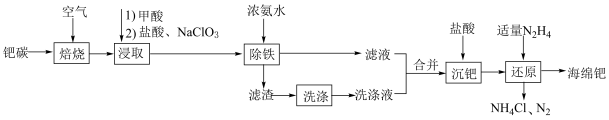
2 . 钯(Pd)是一种不活泼的金属,在新型合金、有机催化剂方面应用广泛。以废钯催化剂(简称钯碳,含有5%~6%钯、93%~94%积碳、1%~2%铁等)为原料回收钯的工艺流程如图所示。
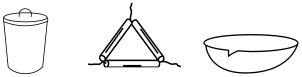
(1)“焙烧”的主要目的是_______ ;在实验室进行“焙烧”时,下列仪器中需要用到的是_______ (填仪器名称)。 ,有
,有 (二元强酸)生成,写出生成
(二元强酸)生成,写出生成 反应的离子方程式:
反应的离子方程式:_______ 。
(3)常温下“除铁”时,铁元素恰好沉淀完全时的pH为_______ {结果保留两位小数,已知:常温下,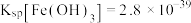 ,该条件下认为溶液中
,该条件下认为溶液中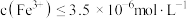 时沉淀完全,lg2=0.3}。
时沉淀完全,lg2=0.3}。
(4)滤渣需要洗涤,并将洗涤液和滤液合并,其目的是_______ 。
(5)“沉钯”时 转化为难溶于冷水的
转化为难溶于冷水的 ,其化学方程式为
,其化学方程式为_______ 。
(6)“还原”过程中还有其他副产物生成,该副产物可循环至_______ 工序利用。
(1)“焙烧”的主要目的是
 ,有
,有 (二元强酸)生成,写出生成
(二元强酸)生成,写出生成 反应的离子方程式:
反应的离子方程式:(3)常温下“除铁”时,铁元素恰好沉淀完全时的pH为
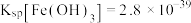 ,该条件下认为溶液中
,该条件下认为溶液中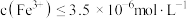 时沉淀完全,lg2=0.3}。
时沉淀完全,lg2=0.3}。(4)滤渣需要洗涤,并将洗涤液和滤液合并,其目的是
(5)“沉钯”时
 转化为难溶于冷水的
转化为难溶于冷水的 ,其化学方程式为
,其化学方程式为(6)“还原”过程中还有其他副产物生成,该副产物可循环至
您最近一年使用:0次
7日内更新
|
59次组卷
|
3卷引用:2024届山西省天一大联考高三下学期考前模拟考试理科综合试题-高中化学
解题方法
3 . 铬酰氯是一种无机化合物,化学式为 ,熔点:
,熔点: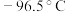 ,沸点:
,沸点: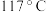 ,常温下为深红棕色液体,遇水剧烈反应产生大量白雾(铬酸、氯化氢)。在实验室中可由重铬酸钾、浓硫酸与氯化钾反应得到铬酰氯,反应机理为:浓硫酸先分别与重铬酸钾和氯化钾反应生成
,常温下为深红棕色液体,遇水剧烈反应产生大量白雾(铬酸、氯化氢)。在实验室中可由重铬酸钾、浓硫酸与氯化钾反应得到铬酰氯,反应机理为:浓硫酸先分别与重铬酸钾和氯化钾反应生成 和氯化氢气体两种中间产物,然后
和氯化氢气体两种中间产物,然后 迅速与氯化氢气体反应生成铬酰氯,实验装置如图(夹持装置略):
迅速与氯化氢气体反应生成铬酰氯,实验装置如图(夹持装置略):
(1)铬酰氯中 元素的化合价为
元素的化合价为___________ 。
(2)装置图中,仪器 的名称分别是
的名称分别是___________ 、___________ 。
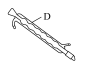
(3)有人建议将仪器B换成如图仪器D,效果会更好,你同意此观点吗?___________ (填“是”或“否”),若不同意,请说出原因:___________ 。 总反应方程式为
总反应方程式为___________ 。
(5)反应结束后,用电热套加热反应装置,收集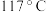 左右的馏分,收集装置选用冰水浴的目的是
左右的馏分,收集装置选用冰水浴的目的是___________ 。
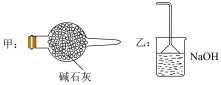
(6)铬酰氯遇水反应的化学方程式为___________ ,据此可知C中应选用下图装置中的___________ (填“甲”或“乙”),不用另一个的主要原因是___________ 。
 ,熔点:
,熔点: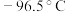 ,沸点:
,沸点: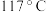 ,常温下为深红棕色液体,遇水剧烈反应产生大量白雾(铬酸、氯化氢)。在实验室中可由重铬酸钾、浓硫酸与氯化钾反应得到铬酰氯,反应机理为:浓硫酸先分别与重铬酸钾和氯化钾反应生成
,常温下为深红棕色液体,遇水剧烈反应产生大量白雾(铬酸、氯化氢)。在实验室中可由重铬酸钾、浓硫酸与氯化钾反应得到铬酰氯,反应机理为:浓硫酸先分别与重铬酸钾和氯化钾反应生成 和氯化氢气体两种中间产物,然后
和氯化氢气体两种中间产物,然后 迅速与氯化氢气体反应生成铬酰氯,实验装置如图(夹持装置略):
迅速与氯化氢气体反应生成铬酰氯,实验装置如图(夹持装置略):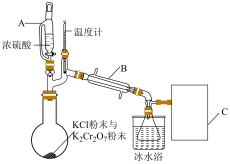
(1)铬酰氯中
 元素的化合价为
元素的化合价为(2)装置图中,仪器
 的名称分别是
的名称分别是(3)有人建议将仪器B换成如图仪器D,效果会更好,你同意此观点吗?
 总反应方程式为
总反应方程式为(5)反应结束后,用电热套加热反应装置,收集
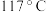 左右的馏分,收集装置选用冰水浴的目的是
左右的馏分,收集装置选用冰水浴的目的是(6)铬酰氯遇水反应的化学方程式为
您最近一年使用:0次
解题方法
4 . 下列实验能达到目的的是
| 实验目的 | 实验方法或操作 | |
| A | 探究 光照分解产物 光照分解产物 | 用强光照射氯水,同时利用 传感器、氯离子传感器和氧气传感器采集数据并分析 传感器、氯离子传感器和氧气传感器采集数据并分析 |
| B | 验证 与浓硫酸反应产物中含有 与浓硫酸反应产物中含有 | 向反应后溶液中加入适量水,观察溶液颜色变化 |
| C | 探究浓度对化学反应速率的影响 | 量取同体积 和 和 的 的 溶液,分别加入等体积等浓度的 溶液,分别加入等体积等浓度的 溶液,对比现象 溶液,对比现象 |
| D | 验证苯与液溴发生了取代反应 | 将反应后的气体通入盛有 溶液的试管中,生成淡黄色沉淀 溶液的试管中,生成淡黄色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 立方晶系Sb2O3对光稳定,是制备聚对苯二甲酸乙二醇酯的优良催化剂。制备的实验步骤如下:
①按下图装置安装仪器(加热仪器略),添加试剂,通入NH3,得到固液混合物。
②向容器a中加入一定量的蒸馏水,搅拌一段时间,过滤、洗涤、110℃烘干。
①SbCl3易水解成SbOCl,SbOCl难溶于乙醇、能溶于乙二醇,SbOCl也可水解为Sb2O3,但如果反应只发生在表面,则得不到单一晶型。
②无水乙醇和乙二醇都可能含少量水。
回答下列问题:
(1)步骤①生成Sb2(OCH2CH2O)3,写出化学方程式___________ 。
(2)仪器a的名称为___________ ,装置B的作用为___________ 。
(3)洗涤时Sb2O3晶体洗净的判断标准是___________ 。
(4)烘干时,晶体装在___________ (填仪器名称)。
(5)如果将乙二醇改为乙醇用上述同样方法制备,往往得到Sb2O3混晶,解释原因___________ 。
(6)用___________ 法可以测定Sb2O3是混晶还是单晶。
(7)取mg产品于锥形瓶中,用盐酸等试剂预处理后,用amol·L-1碘标准液滴定。接近终点时加入2滴淀粉溶液,继续滴定至终点,消耗碘标准液VmL。反应原理为 。
。
①滴定终点现象是___________ 。
②产品中Sb元素的质量分数是___________ 。
①按下图装置安装仪器(加热仪器略),添加试剂,通入NH3,得到固液混合物。
②向容器a中加入一定量的蒸馏水,搅拌一段时间,过滤、洗涤、110℃烘干。

①SbCl3易水解成SbOCl,SbOCl难溶于乙醇、能溶于乙二醇,SbOCl也可水解为Sb2O3,但如果反应只发生在表面,则得不到单一晶型。
②无水乙醇和乙二醇都可能含少量水。
回答下列问题:
(1)步骤①生成Sb2(OCH2CH2O)3,写出化学方程式
(2)仪器a的名称为
(3)洗涤时Sb2O3晶体洗净的判断标准是
(4)烘干时,晶体装在
(5)如果将乙二醇改为乙醇用上述同样方法制备,往往得到Sb2O3混晶,解释原因
(6)用
(7)取mg产品于锥形瓶中,用盐酸等试剂预处理后,用amol·L-1碘标准液滴定。接近终点时加入2滴淀粉溶液,继续滴定至终点,消耗碘标准液VmL。反应原理为
 。
。①滴定终点现象是
②产品中Sb元素的质量分数是
您最近一年使用:0次
2024-05-01更新
|
259次组卷
|
3卷引用:山西省平遥中学2023-2024学年高三二模考试化学试题
解题方法
6 . 肉桂酸广泛应用于香精香料、食品添加剂、医药工业、美容和有机合成等方面。其合成原理及实验室制备方法如下:
i.在 仪器a中加入
仪器a中加入 苯甲醛、
苯甲醛、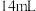 乙酸酐和
乙酸酐和 无水碳酸钾粉末(过量),加热回流
无水碳酸钾粉末(过量),加热回流 。
。
ⅱ.向反应混合物中加入 蒸馏水浸泡几分钟,进行水蒸气蒸馏。
蒸馏水浸泡几分钟,进行水蒸气蒸馏。
ⅲ.将烧瓶冷却后,加入 碳酸钠,再加入
碳酸钠,再加入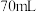 水,加热煮沸,趁热过滤。
水,加热煮沸,趁热过滤。
iV。待滤液冷却至室温后,在搅拌下小心加入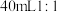 盐酸,使溶液呈酸性。
盐酸,使溶液呈酸性。
V。冷却结晶,抽滤,用少量试剂b洗涤, 烘干,得粗产品
烘干,得粗产品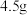 。
。
回答下列问题:
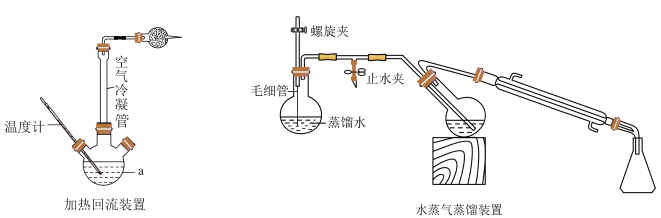
(1)加热回流装置中仪器a的名称是_______ ,不使用水冷冷凝管而用空气冷凝管是为了_______ 。
(2)碳酸钾使用前应干燥并研细,目的是_______ 。
(3)水蒸气蒸馏装置中毛细管的主要作用是_______ ,步骤ⅱ中蒸出的物质是_______ 与水的低沸点共沸物,判断蒸馏完成的方法是_______ 。
(4)步骤ⅲ中趁热过滤除去的主要物质是_______ (填名称)。
(5)步骤V中试剂b是_______ 。
(6)本实验肉桂酸的产率最接近_______(填标号)。
主反应: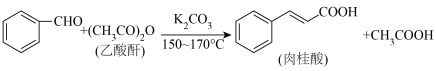
副反应: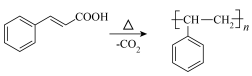
i.在
 仪器a中加入
仪器a中加入 苯甲醛、
苯甲醛、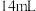 乙酸酐和
乙酸酐和 无水碳酸钾粉末(过量),加热回流
无水碳酸钾粉末(过量),加热回流 。
。ⅱ.向反应混合物中加入
 蒸馏水浸泡几分钟,进行水蒸气蒸馏。
蒸馏水浸泡几分钟,进行水蒸气蒸馏。ⅲ.将烧瓶冷却后,加入
 碳酸钠,再加入
碳酸钠,再加入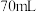 水,加热煮沸,趁热过滤。
水,加热煮沸,趁热过滤。iV。待滤液冷却至室温后,在搅拌下小心加入
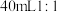 盐酸,使溶液呈酸性。
盐酸,使溶液呈酸性。V。冷却结晶,抽滤,用少量试剂b洗涤,
 烘干,得粗产品
烘干,得粗产品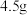 。
。
| 名称 | 相对分 子质量 | 密度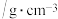 | 熔点 | 沸点 | 溶解度: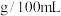 | ||
| 水 | 醇 | 醚 | |||||
| 苯甲醛 | 106 | 1.04 | 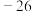 | 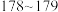 | 0.3 | 互溶 | 互溶 |
| 乙酸酐 | 102 | 1.08 | 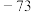 | 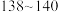 | 遇水生成乙酸 | 溶 | 不溶 |
| 肉桂酸 | 148 | 1.24 | 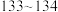 | 300 | 0.04 | 24 | 溶 |
(1)加热回流装置中仪器a的名称是
(2)碳酸钾使用前应干燥并研细,目的是
(3)水蒸气蒸馏装置中毛细管的主要作用是
(4)步骤ⅲ中趁热过滤除去的主要物质是
(5)步骤V中试剂b是
(6)本实验肉桂酸的产率最接近_______(填标号)。
A. | B. | C. | D. |
您最近一年使用:0次
解题方法
7 . 将铁粉和硫粉混合物放置在石棉网上,用炽热玻璃棒引燃,混合物剧烈燃烧至完全反应,关于该实验的说法正确的是
| A.燃烧过程中有SO3生成 | B.生成的固体产物中只有FeS |
| C.该实验应在通风蹰中进行 | D.反应中玻璃棒起催化作用 |
您最近一年使用:0次
2024-04-06更新
|
67次组卷
|
2卷引用:山西省教育发展联盟2023-2024学年高一下学期3月份调研测试化学试题
名校
解题方法
8 . AlCl3是有机合成的催化剂,易潮解,升华温度为178℃。已知:实验室制备氯气的常用方法之一为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。某小组设计实验制备的装置如图所示。下列说法中正确的是

| A.②和③的位置可以互换 |
| B.先启动①中反应,当④中充满黄绿色时再点燃酒精灯 |
| C.上述实验方案只存在1处错误 |
| D.如果用MnO2替代KMnO4也可以完成上述实验 |
您最近一年使用:0次
名校
解题方法
9 . 某化学实验室产生的废液中含有 Fe3+、Cu2+、Ag+三种金属离子,甲同学设计了如图所示的方案对废液进行处理,以回收金属,下列说法正确的是
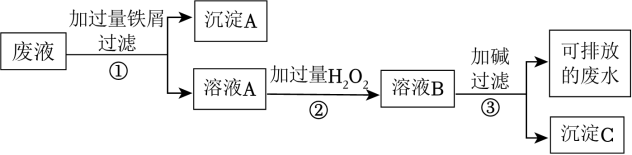

| A.沉淀A中含有2种金属单质 |
| B.可用KSCN溶液来检验溶液B中所含的金属离子 |
| C.溶液A若只经过操作③最终将无法得到沉淀C |
| D.操作①②③中都需要用到玻璃棒、漏斗 |
您最近一年使用:0次
2024-03-19更新
|
94次组卷
|
20卷引用:山西省太原市第五中学2020-2021学年高一上学期12月阶段性检测化学试题
山西省太原市第五中学2020-2021学年高一上学期12月阶段性检测化学试题浙江省温州市新力量联盟2018-2019学年高一上学期期末考试化学试题贵州省思南中学2018-2019学年高一下学期期末考试化学试题江西省上高县第二中学2019-2020学年高一上学期第三次月考化学试题河北省安平中学2019-2020学年高一上学期第四次月考化学试题江苏省盐城市大丰区新丰中学2019-2020学年高一上学期期末考试化学试题河北省保定市涞水波峰中学2019-2020学年高一下学期第三次质检考试化学试题宁夏石嘴山市第三中学2020-2021学年高一上学期第二次月考化学试题(已下线)【浙江新东方】在线化学 (14)(已下线)练习9 铁的多样性-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)(已下线)【浙江新东方】在线化学33浙江省淳安县汾口中学2020-2021学年高二12月月考化学试题云南省楚雄天人中学2019-2020学年高一上学期12月月考化学试题四川师范大学附属中学2020-2021学年高一上学期12月月考化学试题云南省玉溪师范学院附属中学2021-2022学年高一下学期开学测试化学试题湖南省常德市桃源县第一中学2022-2023学年高三上学期9月月考化学试题河北省廊坊市第一中学2022~2023 学年高一上学期期末考试化学试题甘肃省张掖市高台县第一中学2022-2023学年高一下学期开学检测化学试题广东省广州天省实验学校2022-2023学年高一上学期期末考试化学试卷浙江省淳安县汾口中学2023-2024学年高二上学期12月检测化学试题
名校
解题方法
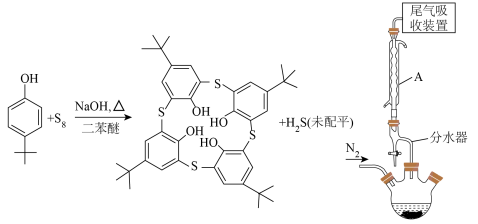
10 . 自分子识别兴起以来,冠醚、杯酚烃等的合成引起了研究者的广泛关注。硫代杯[4]芳烃已被应用于许多方面,如监测和分离一些阳离子、阴离子等。合成对叔丁基硫代杯[4]芳烃(M=720.0g⋅mol-1)的原理表示如下:
利用如图所示装置(加热、搅拌、夹持等装置省略),将60.00g对叔丁基苯酚、25.60gS8、8g氢氧化钠和40mL二苯醚加入500mL三颈烧瓶中,在N2气氛下磁力加热搅拌,逐步升温到230℃,温度保持在230℃反应4小时。停止加热并冷却至100℃以下后,加入40mL 6mol·L-1的盐酸和400mL乙醇的混合溶液,搅拌,抽滤,用乙醇和蒸馏水交替洗涤固体,得到粗产物。将粗产物在氯仿/乙醇中重结晶,得到30.24g纯化的对叔丁基硫代杯[4]芳烃。回答下列问题:
(1)仪器A的名称是___________ ,其作用是___________ 。
(2)对叔丁基邻苯二酚(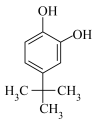 )的沸点小于2-叔丁基对苯二酚(
)的沸点小于2-叔丁基对苯二酚(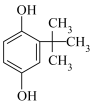 )的原因是
)的原因是___________ 。
(3)加热过程中要不断通入氮气,目的是___________ 。
(4)停止加热后,向反应器中加入盐酸和乙醇混合溶液的目的是___________ 。
(5)实验过程中会产生一种有毒气体,尾气吸收装置中应用___________ (填试剂名称)将该气体除去。
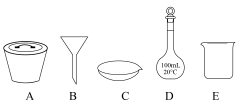
(6)在重结晶过程中,需要用到如图所示仪器中的___________ (填字母)___________ (计算结果精确到0.1%)。
利用如图所示装置(加热、搅拌、夹持等装置省略),将60.00g对叔丁基苯酚、25.60gS8、8g氢氧化钠和40mL二苯醚加入500mL三颈烧瓶中,在N2气氛下磁力加热搅拌,逐步升温到230℃,温度保持在230℃反应4小时。停止加热并冷却至100℃以下后,加入40mL 6mol·L-1的盐酸和400mL乙醇的混合溶液,搅拌,抽滤,用乙醇和蒸馏水交替洗涤固体,得到粗产物。将粗产物在氯仿/乙醇中重结晶,得到30.24g纯化的对叔丁基硫代杯[4]芳烃。回答下列问题:
(1)仪器A的名称是
(2)对叔丁基邻苯二酚(
 )的沸点小于2-叔丁基对苯二酚(
)的沸点小于2-叔丁基对苯二酚( )的原因是
)的原因是(3)加热过程中要不断通入氮气,目的是
(4)停止加热后,向反应器中加入盐酸和乙醇混合溶液的目的是
(5)实验过程中会产生一种有毒气体,尾气吸收装置中应用
(6)在重结晶过程中,需要用到如图所示仪器中的
您最近一年使用:0次
2024-03-10更新
|
617次组卷
|
2卷引用:山西省晋城市第一中学校2023-2024学年高三下学期开学考试理综化学试题



