解题方法
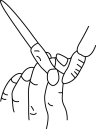
1 . 化学实验操作是进行科学实验的基础。下列操作符合规范的是
|
|
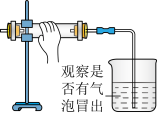
| A.碱式滴定管排气泡 | B.检查装置气密性 |
|
|
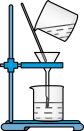
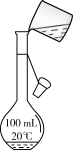
| C.过滤 | D.溶液的转移 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
2 . 连二亚硫酸钠 是一种强碱弱酸盐,利用
是一种强碱弱酸盐,利用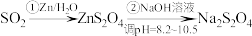 转化制取连二亚硫酸钠的装置如图。已知:
转化制取连二亚硫酸钠的装置如图。已知: 属于两性氢氧化物。下列说法错误的是
属于两性氢氧化物。下列说法错误的是
 是一种强碱弱酸盐,利用
是一种强碱弱酸盐,利用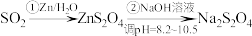 转化制取连二亚硫酸钠的装置如图。已知:
转化制取连二亚硫酸钠的装置如图。已知: 属于两性氢氧化物。下列说法错误的是
属于两性氢氧化物。下列说法错误的是
A.转化①中的氧化剂是 |
| B.开始滴加NaOH溶液的标志是三颈烧瓶中出现浑浊 |
C.调pH至碱性的目的是抑制 水解 水解 |
D.NaOH溶液不能过量,原因是防止 溶解,不利于与 溶解,不利于与 分离 分离 |
您最近一年使用:0次
名校
解题方法
3 . 下列有关实验基本操作的说法正确的是
| A.蒸馏开始时先打开加热器,再通冷凝水;蒸馏结束后先关闭冷凝水,再关闭加热器 |
| B.用浓氨水清洗做过银镜反应的试管,除去银镜 |
| C.用苯萃取溴水中的溴单质,分液时应先放出有机相,再倒出无机相 |
D.用标准 溶液滴定海水,测定其中氯离子的浓度,需要棕色滴定管、锥形瓶 溶液滴定海水,测定其中氯离子的浓度,需要棕色滴定管、锥形瓶 |
您最近一年使用:0次
名校
4 . 钛酸钡( )因其优良的电学性能被广泛应用于多层陶瓷电容器(MLCC)等电子元器件,某同学以
)因其优良的电学性能被广泛应用于多层陶瓷电容器(MLCC)等电子元器件,某同学以 和高活性偏钛酸(
和高活性偏钛酸( )为原料,在实验室中采用低温固相法制备亚微米级钛酸钡粉体。
)为原料,在实验室中采用低温固相法制备亚微米级钛酸钡粉体。
已知:①氧化性: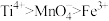 ;
; 。②四氧化钛极易水解,易挥发。
。②四氧化钛极易水解,易挥发。
Ⅰ.制备偏钛酸(装置如图) 固体于三颈烧瓶中,加入浓盐酸配成
固体于三颈烧瓶中,加入浓盐酸配成 溶液,然后加水稀释转化成一定浓度的
溶液,然后加水稀释转化成一定浓度的 溶液,最后将装在仪器B中的氨水缓慢滴入
溶液,最后将装在仪器B中的氨水缓慢滴入 溶液中,搅拌,析出
溶液中,搅拌,析出 。反应过程中注意控制温度,以免反应过于剧烈。
。反应过程中注意控制温度,以免反应过于剧烈。
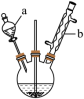
(1)仪器B的名称是_____ 。
(2)仪器A中冷凝水从_____ (填“a”或“b”)口通入。
(3)写出氨水与 溶液反应产生
溶液反应产生 的化学方程式
的化学方程式_____ 。
Ⅱ.制备钛酸钡
将上述制得的作为反应原料,与按照物质的量之比为1:1混合后放入球磨罐中,放置于“罐磨机”上,按照700r/min罐磨,5h后倒入坩埚中,并置于烘箱中100℃反应3h,得到亚微米级白色钛酸钡样品粉体。
(4)写出 与
与 反应的化学方程式
反应的化学方程式_____ 。
(5)在固相反应过程中,会经历“接触扩散—化学反应—成核—晶粒生长”的历程,“罐磨机”的作用是_____ ,若想获得比亚微米级钛酸钡晶体更大颗粒的晶体,应置于_____ (填“<”或“>”)100℃的烘箱中反应。
Ⅲ.测定产品纯度
取wg ,产品溶于稍过量的稀硫酸中配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量
,产品溶于稍过量的稀硫酸中配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量 mL
mL mol/L
mol/L 溶液,充分反应后,用
溶液,充分反应后,用 mol/L
mol/L 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 mL。(
mL。( 的摩尔质量为Mg/mol)
的摩尔质量为Mg/mol)
(6)实验中所用滴定管为_____ (填“酸式”或“碱式”或“酸式和碱式”)滴定管。
(7)产品的纯度为_____ %。(用含c、w、V、M的代数式表示)
 )因其优良的电学性能被广泛应用于多层陶瓷电容器(MLCC)等电子元器件,某同学以
)因其优良的电学性能被广泛应用于多层陶瓷电容器(MLCC)等电子元器件,某同学以 和高活性偏钛酸(
和高活性偏钛酸( )为原料,在实验室中采用低温固相法制备亚微米级钛酸钡粉体。
)为原料,在实验室中采用低温固相法制备亚微米级钛酸钡粉体。已知:①氧化性:
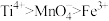 ;
; 。②四氧化钛极易水解,易挥发。
。②四氧化钛极易水解,易挥发。Ⅰ.制备偏钛酸(装置如图)

 固体于三颈烧瓶中,加入浓盐酸配成
固体于三颈烧瓶中,加入浓盐酸配成 溶液,然后加水稀释转化成一定浓度的
溶液,然后加水稀释转化成一定浓度的 溶液,最后将装在仪器B中的氨水缓慢滴入
溶液,最后将装在仪器B中的氨水缓慢滴入 溶液中,搅拌,析出
溶液中,搅拌,析出 。反应过程中注意控制温度,以免反应过于剧烈。
。反应过程中注意控制温度,以免反应过于剧烈。(1)仪器B的名称是
(2)仪器A中冷凝水从
(3)写出氨水与
 溶液反应产生
溶液反应产生 的化学方程式
的化学方程式Ⅱ.制备钛酸钡
将上述制得的作为反应原料,与按照物质的量之比为1:1混合后放入球磨罐中,放置于“罐磨机”上,按照700r/min罐磨,5h后倒入坩埚中,并置于烘箱中100℃反应3h,得到亚微米级白色钛酸钡样品粉体。
(4)写出
 与
与 反应的化学方程式
反应的化学方程式(5)在固相反应过程中,会经历“接触扩散—化学反应—成核—晶粒生长”的历程,“罐磨机”的作用是
Ⅲ.测定产品纯度
取wg
 ,产品溶于稍过量的稀硫酸中配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量
,产品溶于稍过量的稀硫酸中配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量 mL
mL mol/L
mol/L 溶液,充分反应后,用
溶液,充分反应后,用 mol/L
mol/L 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液
溶液 mL。(
mL。( 的摩尔质量为Mg/mol)
的摩尔质量为Mg/mol)(6)实验中所用滴定管为
(7)产品的纯度为
您最近一年使用:0次
7日内更新
|
64次组卷
|
2卷引用:黑龙江省大庆市实验中学实验二部2023-2024学年高三下学期得分训练化学试题(五)
解题方法
5 . 工业上常用的一种海水中提溴技术叫做“吹出法”,其过程主要包括氧化、吹出、吸收和蒸馏等环节(如下图),下列有关说法错误的是
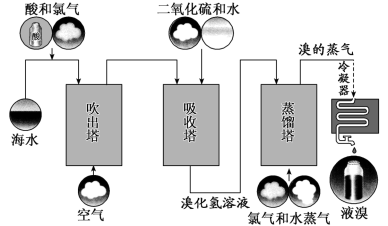
A.过程中酸化海水的目的是抑制 的溶解 的溶解 |
B.吸收塔中发生的主要反应的化学方程式为 |
| C.实验室模拟蒸馏过程,用到的主要仪器包括:蒸馏烧瓶、球形冷凝管、温度计等 |
D.保存液溴的过程中,水封的主要目的是防止或减弱 的挥发 的挥发 |
您最近一年使用:0次
6 . 下列实验操作或实验现象与预期实验目的或所得实验结论一致的是
选项 | 实验操作或实验现象 | 实验目的或结论 |
A | 一块表面打磨过的铝箔在酒精灯上加热至熔化,液态铝不会滴落 | 铝的熔点高于三氧化二铝 |
B | 将吸有NaOH溶液的长胶头滴管伸入盛有FeSO4溶液的试管底部并缓慢挤出碱液 | 制备并观察到白色絮状的 沉淀 沉淀 |
C | 蒸馏实验操作时将温度计插入液面以下但不能触碰到烧瓶内壁 | 准确测定馏分的温度,以便于液体混合物分离 |
D | Fe(OH)3胶体可用于杀菌消毒 | 说明Fe(OH)3胶体表面积大,有较强的吸附性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
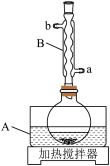
7 . 实验室由安息香制备二苯乙二酮的反应式如下:
装置示意图如下图所示,实验步骤为: 冰乙酸、
冰乙酸、 水及
水及 ,边搅拌边加热,至固体全部溶解。
,边搅拌边加热,至固体全部溶解。
②停止加热,待沸腾平息后加入 安息香,加热回流45-60min。
安息香,加热回流45-60min。
③加入 水,煮沸后冷却,有黄色固体析出。
水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用 的乙醇重结晶,干燥后得淡黄色晶体
的乙醇重结晶,干燥后得淡黄色晶体 。
。
回答下列问题:
(1)下列关于安息香分子说法正确的是___________。
(2)仪器A中应加入___________ (填“水”或“油”)作为热传导介质。
(3)仪器 的名称是
的名称是___________ ;冷却水应从___________ (填“a”或“b”)口通入。
(4)获得粗品中若含有未被氧化的安息香,可用少量___________ 洗涤除去。
(5)粗品重结晶操作为:加热溶解 活性炭脱色
活性炭脱色
___________ 
___________  过滤
过滤 洗涤
洗涤 干燥。
干燥。
(6)本实验的产率最接近于___________ (填标号)。
a. b.
b. c.
c. d.
d.

| 物质 | 性状 | 熔点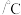 | 沸点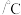 | 溶解性 |
| 安息香 | 白色固体 | 133 | 344 | 难溶于冷水,溶于热水、乙醇、乙酸 |
| 二苯乙二酮 | 淡黄色固体 | 95 | 347 | 不溶于水,溶于乙醇、苯、乙酸 |
| 冰乙酸 | 无色液体 | 17 | 118 | 与水、乙醇互溶 |
 冰乙酸、
冰乙酸、 水及
水及 ,边搅拌边加热,至固体全部溶解。
,边搅拌边加热,至固体全部溶解。②停止加热,待沸腾平息后加入
 安息香,加热回流45-60min。
安息香,加热回流45-60min。③加入
 水,煮沸后冷却,有黄色固体析出。
水,煮沸后冷却,有黄色固体析出。④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用
 的乙醇重结晶,干燥后得淡黄色晶体
的乙醇重结晶,干燥后得淡黄色晶体 。
。回答下列问题:
(1)下列关于安息香分子说法正确的是___________。
| A.分子所含官能团名称为羧基 | B.一氯代物有6种 |
C.分子式为 | D.分子中所有碳原子可能共平面 |
(2)仪器A中应加入
(3)仪器
 的名称是
的名称是(4)获得粗品中若含有未被氧化的安息香,可用少量
(5)粗品重结晶操作为:加热溶解
 活性炭脱色
活性炭脱色

 过滤
过滤 洗涤
洗涤 干燥。
干燥。(6)本实验的产率最接近于
a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次
2024·黑龙江·模拟预测
解题方法
8 . 利用传统方式制备乙炔的过程中,存在一些问题难以解决,如反应速率过快、放热过多不易控制,生成的糊状物流难以实现固液分离导致乙炔气流不平稳,甚至发生堵塞等问题。为解决上述问题,某校化学兴趣小组设计出一套乙炔制备、净化和收集实验的一体化实验装置。
(1)下列仪器中与上述装置中储液杯和流量调节器作用相同的是___________ 。
(2)①仪器B的名称是___________ 。
②向A反应器中填装固体反应物时,电石放置位置为___________ (填“甲处”或“乙处”),反应器中装有7mm玻璃珠,其作用为___________ 。
③B装置中可用次氯酸钠吸收混杂在乙炔中H2S、PH3,反应中PH3被氧化为最高价氧化物对应的水化物,请写出次氯酸钠与PH3反应的离子方程式___________ 。
(3)兴趣小组在制备乙炔时对反应液进行了一系列筛选(如下图),依据图表选择最合适的反应液为___________ (填标号),原因是___________ 。
(4)选取合适的反应液后,小组称取电石1.25g(杂质的质量分数为4.0%)完成实验,除杂后测得乙炔气体体积为336mL(标准状况下),计算该实验中乙炔的产率:___________ %(结果保留两位有效数字)。

(1)下列仪器中与上述装置中储液杯和流量调节器作用相同的是
|
|
|
|
| A.漏斗 | B.分液漏斗 | C.恒压滴液漏斗 | D.布氏漏斗 |
(2)①仪器B的名称是
②向A反应器中填装固体反应物时,电石放置位置为
③B装置中可用次氯酸钠吸收混杂在乙炔中H2S、PH3,反应中PH3被氧化为最高价氧化物对应的水化物,请写出次氯酸钠与PH3反应的离子方程式
(3)兴趣小组在制备乙炔时对反应液进行了一系列筛选(如下图),依据图表选择最合适的反应液为

(4)选取合适的反应液后,小组称取电石1.25g(杂质的质量分数为4.0%)完成实验,除杂后测得乙炔气体体积为336mL(标准状况下),计算该实验中乙炔的产率:
您最近一年使用:0次
2024·黑龙江·模拟预测
解题方法
9 . 苯甲醛是一种重要的化工原料,某小组同学利用如图实验装置(夹持装置已略去)制备苯甲醛。
实验步骤:
①向容积为500mL的三颈烧瓶加入90.0mL质量分数为5%的次氯酸钠溶液(稍过量),调节溶液的pH为9-10后,加入3.0mL苯甲醇、75.0mL二氯甲烷,不断搅拌。
②充分反应后,用二氯甲烷萃取水相3次,并将有机相合并。
③向所得有机相中加入无水硫酸镁,过滤,得到有机混合物。
④蒸馏有机混合物,得到2.08g苯甲醛产品。
回答下列问题:
(1)苯甲醇中碳原子的杂化方式为___________ ,可用___________ (填试剂编号)试剂鉴别苯甲醇和苯甲醛。
A.酸性高锰酸钾 B.溴水 C.新制的银氨溶液 D.Na
(2)仪器b的名称为___________ ,三颈烧瓶中苯甲醇与NaClO反应的化学方程式为___________ 。
(3)步骤①中,投料时,次氯酸钠不能过量太多,原因是___________ ;步骤③中加入无水硫酸镁,若省略该操作, 可能造成的后果是___________ 。
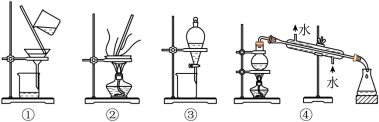
(4)步骤②中,应选用的实验装置是___________ (填序号),该操作中分离出有机相的具体操作方法是___________ 。___________ 左右。
(6)本实验中,苯甲醛的产率为___________ (保留到小数点后一位)。
| 有机物 | 沸点℃ | 密度为g/cm3 | 溶解性 |
| 苯甲醛 | 178.1 | 1.04 | 微溶于水,易溶于乙醇、醚和卤代烃 |
| 苯甲醇 | 205.7 | 1.04 | 微溶于水,易溶于乙醇、醚和卤代烃 |
| 二氯甲烷 | 39.8 | 1.33 | 难溶于水,易溶于有机溶剂 |
①向容积为500mL的三颈烧瓶加入90.0mL质量分数为5%的次氯酸钠溶液(稍过量),调节溶液的pH为9-10后,加入3.0mL苯甲醇、75.0mL二氯甲烷,不断搅拌。
②充分反应后,用二氯甲烷萃取水相3次,并将有机相合并。
③向所得有机相中加入无水硫酸镁,过滤,得到有机混合物。
④蒸馏有机混合物,得到2.08g苯甲醛产品。
回答下列问题:
(1)苯甲醇中碳原子的杂化方式为
A.酸性高锰酸钾 B.溴水 C.新制的银氨溶液 D.Na
(2)仪器b的名称为
(3)步骤①中,投料时,次氯酸钠不能过量太多,原因是
(4)步骤②中,应选用的实验装置是
(6)本实验中,苯甲醛的产率为
您最近一年使用:0次
2024·黑龙江·模拟预测
解题方法
10 . 为检测某品牌银耳中添加剂亚硫酸盐的含量,取 银耳样品和
银耳样品和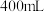 蒸馏水放入三颈瓶中;取
蒸馏水放入三颈瓶中;取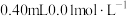 碘标准溶液和
碘标准溶液和 淀粉溶液加入锥形瓶中,并加入适量蒸馏水搅拌,部分装置如图。向三颈瓶中通氮气,再加入过量磷酸,加热并保持微沸,同时用
淀粉溶液加入锥形瓶中,并加入适量蒸馏水搅拌,部分装置如图。向三颈瓶中通氮气,再加入过量磷酸,加热并保持微沸,同时用 碘标准溶液滴定,至终点时滴定消耗了
碘标准溶液滴定,至终点时滴定消耗了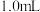 碘标准液。另做空白实验,消耗
碘标准液。另做空白实验,消耗 碘标准溶液。下列说法错误的是
碘标准溶液。下列说法错误的是
 银耳样品和
银耳样品和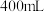 蒸馏水放入三颈瓶中;取
蒸馏水放入三颈瓶中;取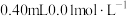 碘标准溶液和
碘标准溶液和 淀粉溶液加入锥形瓶中,并加入适量蒸馏水搅拌,部分装置如图。向三颈瓶中通氮气,再加入过量磷酸,加热并保持微沸,同时用
淀粉溶液加入锥形瓶中,并加入适量蒸馏水搅拌,部分装置如图。向三颈瓶中通氮气,再加入过量磷酸,加热并保持微沸,同时用 碘标准溶液滴定,至终点时滴定消耗了
碘标准溶液滴定,至终点时滴定消耗了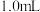 碘标准液。另做空白实验,消耗
碘标准液。另做空白实验,消耗 碘标准溶液。下列说法错误的是
碘标准溶液。下列说法错误的是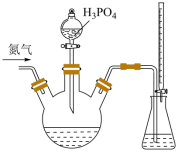
| A.选择的三颈瓶规格为1000mL |
| B.滴定终点溶液变为蓝色,读数时应单手持滴定管 |
| C.“不通氮气”或者“先加磷酸再通氮气”,这两种做法都会使测定结果偏高 |
D.银耳样品中亚硫酸盐的百分含量(以 质量计)为 质量计)为 |
您最近一年使用:0次