名校
1 . 焦亚硫酸钠 常用作葡萄酒、果脯等食品的抗氧化剂,在空气中、受热时均易分解,某实验小组通过实验制备焦亚硫酸钠并测定焦亚硫酸钠的纯度。回答下列问题:
常用作葡萄酒、果脯等食品的抗氧化剂,在空气中、受热时均易分解,某实验小组通过实验制备焦亚硫酸钠并测定焦亚硫酸钠的纯度。回答下列问题:
I.焦亚硫酸钠的制备
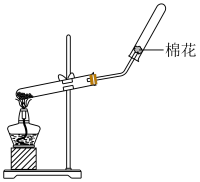
实验室制备少量 的装置如图所示。
的装置如图所示。 左右,向
左右,向 过饱和溶液中通入
过饱和溶液中通入 ,当溶液的
,当溶液的 为4.1时,停止通入
为4.1时,停止通入 ,
, 静置结晶,经减压抽滤、洗涤、
静置结晶,经减压抽滤、洗涤、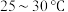 干燥,可获得
干燥,可获得 固体。
固体。
(1) 的VSEPR模型名称为
的VSEPR模型名称为__________ 。
(2)控制反应温度在 左右的原因是
左右的原因是_____________ 。
(3)装置 的作用是
的作用是__________ 。
(4)工业上亦可用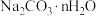 (固体)与
(固体)与 气体充分接触反应制备焦亚硫酸钠,此法常称为干法制备焦亚硫酸盐,写出反应的化学方程式:
气体充分接触反应制备焦亚硫酸钠,此法常称为干法制备焦亚硫酸盐,写出反应的化学方程式:_______________ 。
(5)因为 具有
具有_________ 性,所以产品 中不可避免地存在
中不可避免地存在 。检验产品中含有
。检验产品中含有 的方法是
的方法是_____________ 。
Ⅱ.焦亚硫酸钠纯度的测定
工业焦亚硫酸钠优质品要求焦亚硫酸钠的质量分数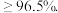 通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为
通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为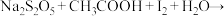
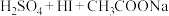 (未配平),
(未配平), 。
。
准确称取 样品,快速置于预先加入
样品,快速置于预先加入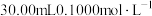 碘标准液及
碘标准液及 水的
水的 碘量瓶中,加入
碘量瓶中,加入 乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处
乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处 ,用
,用 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗 标准溶液
标准溶液 。
。
(6)滴定终点的现象是_____________ 。
(7)该样品中焦亚硫酸钠的质量分数为__________  ,
,__________ (填“是”或“不是”)优质品。
 常用作葡萄酒、果脯等食品的抗氧化剂,在空气中、受热时均易分解,某实验小组通过实验制备焦亚硫酸钠并测定焦亚硫酸钠的纯度。回答下列问题:
常用作葡萄酒、果脯等食品的抗氧化剂,在空气中、受热时均易分解,某实验小组通过实验制备焦亚硫酸钠并测定焦亚硫酸钠的纯度。回答下列问题:I.焦亚硫酸钠的制备
实验室制备少量
 的装置如图所示。
的装置如图所示。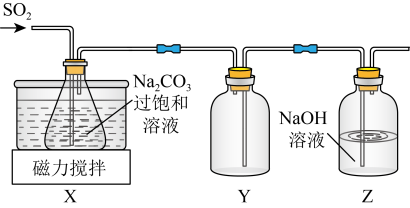
 左右,向
左右,向 过饱和溶液中通入
过饱和溶液中通入 ,当溶液的
,当溶液的 为4.1时,停止通入
为4.1时,停止通入 ,
, 静置结晶,经减压抽滤、洗涤、
静置结晶,经减压抽滤、洗涤、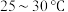 干燥,可获得
干燥,可获得 固体。
固体。(1)
 的VSEPR模型名称为
的VSEPR模型名称为(2)控制反应温度在
 左右的原因是
左右的原因是(3)装置
 的作用是
的作用是(4)工业上亦可用
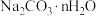 (固体)与
(固体)与 气体充分接触反应制备焦亚硫酸钠,此法常称为干法制备焦亚硫酸盐,写出反应的化学方程式:
气体充分接触反应制备焦亚硫酸钠,此法常称为干法制备焦亚硫酸盐,写出反应的化学方程式:(5)因为
 具有
具有 中不可避免地存在
中不可避免地存在 。检验产品中含有
。检验产品中含有 的方法是
的方法是Ⅱ.焦亚硫酸钠纯度的测定
工业焦亚硫酸钠优质品要求焦亚硫酸钠的质量分数
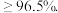 通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为
通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为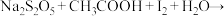
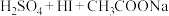 (未配平),
(未配平), 。
。准确称取
 样品,快速置于预先加入
样品,快速置于预先加入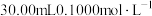 碘标准液及
碘标准液及 水的
水的 碘量瓶中,加入
碘量瓶中,加入 乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处
乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处 ,用
,用 标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗
标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗 标准溶液
标准溶液 。
。(6)滴定终点的现象是
(7)该样品中焦亚硫酸钠的质量分数为
 ,
,
您最近一年使用:0次
昨日更新
|
131次组卷
|
3卷引用:河北省保定市九校2024届高三下学期二模化学试题
名校
2 . 实验室制备纳米ZnO的步骤如下:
①称量10.0000g 固体于100mL小烧杯中,加50mL水溶解,配制成
固体于100mL小烧杯中,加50mL水溶解,配制成 溶液。再称量9.0000g
溶液。再称量9.0000g  固体于50mL小烧杯中,加入40mL水溶解,配制成草酸溶液。
固体于50mL小烧杯中,加入40mL水溶解,配制成草酸溶液。
②将上述两种溶液加入250mL烧杯中,搅拌2h,生成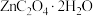 沉淀。
沉淀。
③过滤反应后的混合物,沉淀用蒸馏水洗涤干净后,在真空干燥箱中于110℃下干燥。
④干燥后的沉淀样品在氧气气氛中于350~450℃下焙烧2h,得到白色纳米ZnO。
上述实验中,下列仪器用不到的是
①称量10.0000g
 固体于100mL小烧杯中,加50mL水溶解,配制成
固体于100mL小烧杯中,加50mL水溶解,配制成 溶液。再称量9.0000g
溶液。再称量9.0000g  固体于50mL小烧杯中,加入40mL水溶解,配制成草酸溶液。
固体于50mL小烧杯中,加入40mL水溶解,配制成草酸溶液。②将上述两种溶液加入250mL烧杯中,搅拌2h,生成
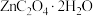 沉淀。
沉淀。③过滤反应后的混合物,沉淀用蒸馏水洗涤干净后,在真空干燥箱中于110℃下干燥。
④干燥后的沉淀样品在氧气气氛中于350~450℃下焙烧2h,得到白色纳米ZnO。
上述实验中,下列仪器用不到的是
A. | B. | C. | D. |
您最近一年使用:0次
昨日更新
|
46次组卷
|
2卷引用:河北省保定市名校协作体2024届高三下学期三模化学试题
名校
3 . 三氯化六氨合钴(III) 是一种重要的含钴配合物,由
是一种重要的含钴配合物,由 制备它的装置和步骤如下(夹持装置已省略):
制备它的装置和步骤如下(夹持装置已省略): 在溶液中较稳定,
在溶液中较稳定, 具有较强还原性。回答下列问题:
具有较强还原性。回答下列问题:
(1)向混合液加入 溶液与氨水时,应最先打开活塞
溶液与氨水时,应最先打开活塞_______ (填字母代号);加入所有试剂后,水浴的温度控制在55℃左右,反应约30分钟。球形干燥管中试剂为_______ 。
(2) 制备
制备 的总反应化学方程式为
的总反应化学方程式为_______ 。
(3)由滤渣获取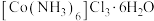 的步骤:向滤渣中加入80℃左右的热水,充分搅拌后,趁热过滤,向滤液加入少量甲,冷却结晶后过滤,用乙洗涤晶体2~3次,低温干燥。下列选项合理的是
的步骤:向滤渣中加入80℃左右的热水,充分搅拌后,趁热过滤,向滤液加入少量甲,冷却结晶后过滤,用乙洗涤晶体2~3次,低温干燥。下列选项合理的是_______ (填字母)。
A.甲为浓盐酸,乙为水 B.甲为乙醇,乙为浓盐酸 C.甲为浓盐酸,乙为乙醇
(4)称取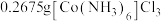 样品,加入盛有足量氢氧化钠溶液的烧瓶中并加热,将生成的氨气通入装有
样品,加入盛有足量氢氧化钠溶液的烧瓶中并加热,将生成的氨气通入装有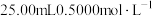 盐酸的锥形瓶中,充分吸收,向锥形瓶加入2~3滴甲基橙,用
盐酸的锥形瓶中,充分吸收,向锥形瓶加入2~3滴甲基橙,用 的NaOH滴定(杂质不反应)。
的NaOH滴定(杂质不反应)。
①达滴定终点时,共消耗NaOH溶液14.00mL,则样品的纯度为_______ (保留四位有效数字)。
②下列操作会使纯度测量值偏高的是_______ (填字母)。
A.滴定前,碱式滴定管未润洗
B.滴定前尖嘴处无气泡,滴定后有气泡
C.滴定终点时俯视滴定管刻度
D.滴定时选用酚酞为指示剂
(5)请指出该装置存在的缺陷:_______ 。
 是一种重要的含钴配合物,由
是一种重要的含钴配合物,由 制备它的装置和步骤如下(夹持装置已省略):
制备它的装置和步骤如下(夹持装置已省略):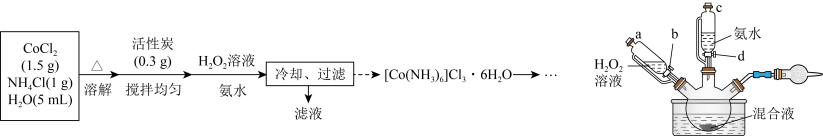
 在溶液中较稳定,
在溶液中较稳定, 具有较强还原性。回答下列问题:
具有较强还原性。回答下列问题:(1)向混合液加入
 溶液与氨水时,应最先打开活塞
溶液与氨水时,应最先打开活塞(2)
 制备
制备 的总反应化学方程式为
的总反应化学方程式为(3)由滤渣获取
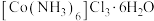 的步骤:向滤渣中加入80℃左右的热水,充分搅拌后,趁热过滤,向滤液加入少量甲,冷却结晶后过滤,用乙洗涤晶体2~3次,低温干燥。下列选项合理的是
的步骤:向滤渣中加入80℃左右的热水,充分搅拌后,趁热过滤,向滤液加入少量甲,冷却结晶后过滤,用乙洗涤晶体2~3次,低温干燥。下列选项合理的是A.甲为浓盐酸,乙为水 B.甲为乙醇,乙为浓盐酸 C.甲为浓盐酸,乙为乙醇
(4)称取
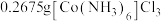 样品,加入盛有足量氢氧化钠溶液的烧瓶中并加热,将生成的氨气通入装有
样品,加入盛有足量氢氧化钠溶液的烧瓶中并加热,将生成的氨气通入装有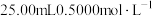 盐酸的锥形瓶中,充分吸收,向锥形瓶加入2~3滴甲基橙,用
盐酸的锥形瓶中,充分吸收,向锥形瓶加入2~3滴甲基橙,用 的NaOH滴定(杂质不反应)。
的NaOH滴定(杂质不反应)。①达滴定终点时,共消耗NaOH溶液14.00mL,则样品的纯度为
②下列操作会使纯度测量值偏高的是
A.滴定前,碱式滴定管未润洗
B.滴定前尖嘴处无气泡,滴定后有气泡
C.滴定终点时俯视滴定管刻度
D.滴定时选用酚酞为指示剂
(5)请指出该装置存在的缺陷:
您最近一年使用:0次
名校
4 . 下列实验设计和操作均正确且能达到实验目的的是
|
|
| A.中和反应反应热的测定 | B.实验室制备氨气 |
|
|
| C.制无水氯化钙 | D.验证酸性:乙酸 碳酸 碳酸 苯酚 苯酚 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 六氟磷酸锂(LiPF6)具有良好的导电性与电化学稳定性能,常作锂离子电池的电解质。LiPF6极易溶于水,可溶于乙醇等有机溶剂,极易吸水潮解,热稳定性差。实验室制备LiPF6的实验装置如图:
i.在氮气保护的手套箱中,准确称取26.0g干燥LiF固体以及过量PCl5固体,均倒入聚四氟乙烯材质的反应器中,再往其中逐渐加入乙腈,至PCl5充分溶解。
ii.往装置中通一段时间N2,以排出其中空气,关闭K1,加热NaHF2,将生成的HF气体通入反应器中,同时搅拌混合其中的物料。
iii.通过往反应器所处的冷浴槽中调控0~10℃的低温。6~8h后终止反应,继续通N2再关闭加热炉保持通N2一段时间。
iv.打开反应器,对反应后的物料进行过滤,滤液用一个聚乙烯材质的塑料瓶接收,密封后拿出手套箱,置于-18~5℃环境中低温结晶。在氮气保护下,过滤出结晶,经40~50℃真空干燥,最终得到产品140.6g。
回答下列问题:
(1)反应装置选用聚四氟乙烯材质容器,不能用玻璃容器,原因是______ (用化学方程式表示)。
(2)NaHF2加热分解的化学方程式为______ 。
(3)干燥塔的作用为______ 。
(4)NaOH溶液的作用为______ 。
(5)已知合成LiPF6的反应为 ,则生成PF5的化学方程式为
,则生成PF5的化学方程式为______ 。
(6)反应结束后,通入氮气的目的是______ 。
(7)本实验所得六氟磷酸锂的产率为______ %(保留三位有效数字)。

i.在氮气保护的手套箱中,准确称取26.0g干燥LiF固体以及过量PCl5固体,均倒入聚四氟乙烯材质的反应器中,再往其中逐渐加入乙腈,至PCl5充分溶解。
ii.往装置中通一段时间N2,以排出其中空气,关闭K1,加热NaHF2,将生成的HF气体通入反应器中,同时搅拌混合其中的物料。
iii.通过往反应器所处的冷浴槽中调控0~10℃的低温。6~8h后终止反应,继续通N2再关闭加热炉保持通N2一段时间。
iv.打开反应器,对反应后的物料进行过滤,滤液用一个聚乙烯材质的塑料瓶接收,密封后拿出手套箱,置于-18~5℃环境中低温结晶。在氮气保护下,过滤出结晶,经40~50℃真空干燥,最终得到产品140.6g。
回答下列问题:
(1)反应装置选用聚四氟乙烯材质容器,不能用玻璃容器,原因是
(2)NaHF2加热分解的化学方程式为
(3)干燥塔的作用为
(4)NaOH溶液的作用为
(5)已知合成LiPF6的反应为
 ,则生成PF5的化学方程式为
,则生成PF5的化学方程式为(6)反应结束后,通入氮气的目的是
(7)本实验所得六氟磷酸锂的产率为
您最近一年使用:0次
名校
解题方法
6 . 下列实验室药品的保存或实验安全应急措施错误的是
| A.漂白粉要避光、密封保存在阴凉处 |
| B.浓溴水沾在皮肤上,先用大量水冲洗,再用酒精擦拭 |
| C.AgNO3溶液应当保存在棕色细口瓶中 |
| D.浓硫酸沾到皮肤上,先用大量水冲洗,然后涂抹稀NaOH溶液 |
您最近一年使用:0次
名校
7 . 下列实验装置(夹持仪器已省略)及操作合理且能达到实验目的的是

A.用装置甲制备 | B.用装置乙测定醋酸浓度 |
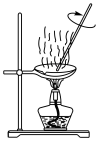
C.用装置丙制备并收集 | D.用装置丁比较 和 和 的热稳定性 的热稳定性 |
您最近一年使用:0次
名校
解题方法
8 . 不同的化学试剂需要采用不同的保存方法。实验室对下列药品的保存方法错误的是
| A.少量碳酸钙固体保存在广口瓶中 | B.碳酸钠溶液保存在带橡胶塞的细口瓶中 |
| C.少量浓硝酸保存在棕色细口瓶中 | D.保存液溴、白磷、金属钠要用水封 |
您最近一年使用:0次
名校
9 . 溴苯是一种化工原料,实验室合成溴苯的装置如图所示及有关数据如表所示:
查阅资料可知:加热条件下,溴苯不与氢氧化钠溶液发生反应。
回答下列问题:
(1)在仪器a中加入50 mL无水苯和少量铁屑。在仪器d中小心加入12.0 mL液态溴。在a中滴入几滴溴,可观察到有白雾产生,是因为生成HBr气体。继续滴加至液溴滴完。
①仪器d的名称为___________ 。
②滴加溴的过程中,冷却水的进出方向为___________ (填“b进c出”或“c进b出”),原因为___________ 。
(2)液溴滴完后,冷却至室温,经过下列步骤分离提纯:
①向仪器a中加入适量的水,然后进行分液操作,加水的目的为___________ 。
②下层滤液依次用适量的10%NaOH溶液、水洗涤。NaOH溶液洗涤时涉及的反应有NaOH+HBr=NaBr+H2O和___________ 。
③向分离后的粗溴苯中加入少量的无水氯化钙,静置、过滤。___________ (“能”或“不能”)用氧化钙代替无水氯化钙,进行相应的操作,判断的理由为___________ 。
(3)经以上分离操作后,粗溴苯中还含有的杂质主要为___________ (填化学名称),要进一步提纯,还需进行蒸馏操作。
(4)合成溴苯的实验中,最适合的a的容积是___________mL(填标号)。

| 苯 | 溴 | 溴苯 | |
| 密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点 | 80 | 59 | 156 |
| 水中溶解性 | 微溶 | 微溶 | 微溶 |
回答下列问题:
(1)在仪器a中加入50 mL无水苯和少量铁屑。在仪器d中小心加入12.0 mL液态溴。在a中滴入几滴溴,可观察到有白雾产生,是因为生成HBr气体。继续滴加至液溴滴完。
①仪器d的名称为
②滴加溴的过程中,冷却水的进出方向为
(2)液溴滴完后,冷却至室温,经过下列步骤分离提纯:
①向仪器a中加入适量的水,然后进行分液操作,加水的目的为
②下层滤液依次用适量的10%NaOH溶液、水洗涤。NaOH溶液洗涤时涉及的反应有NaOH+HBr=NaBr+H2O和
③向分离后的粗溴苯中加入少量的无水氯化钙,静置、过滤。
(3)经以上分离操作后,粗溴苯中还含有的杂质主要为
(4)合成溴苯的实验中,最适合的a的容积是___________mL(填标号)。
| A.100 | B.150 | C.250 | D.500 |
您最近一年使用:0次
解题方法
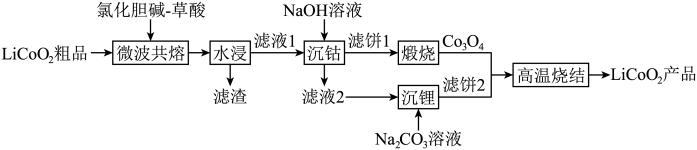
10 . 利用“微波辅助低共熔溶剂”浸取废旧锂离子电池中钴酸锂粗品制备LiCoO2产品,以实现资源的循环利用。主要工艺之流程如下:
②Co2+在溶液中常以[CoCl4]2-(蓝色)和[Co(H2O)6]2+(粉红色)形式存在;
③25℃时, Ksp[Co(OH)2]=1.6×10-15。
回答下列问题:
(1)LiCoO2中Co的化合价为__________ 。
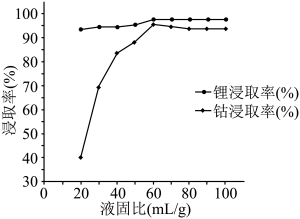
(2)“微波共熔”中氯化胆碱-草酸和LiCoO2粗品以不同的液固比在120℃下微波处理10 min后锂和钴的浸取率如图,则最佳液固比为______ mL/g,草酸的作用为_____________ 。________ 。
(4)25℃时,“沉钴”反应完成后溶液pH=10,此时c(Co2+)=______ mol/L。
(5)“滤饼2”在高温烧结前需要洗涤、干燥,洗涤沉淀的实验操作为__________ 。
(6)锂离子电池正极材料LiCoO2在多次充放电后结构发生改变生成Co3O4,导致电化学性能下降,使用LiOH和30%H2O2溶液可以实现LiCoO2的修复,则修复过程发生反应的化学方程式为__________ 。
②Co2+在溶液中常以[CoCl4]2-(蓝色)和[Co(H2O)6]2+(粉红色)形式存在;
③25℃时, Ksp[Co(OH)2]=1.6×10-15。
回答下列问题:
(1)LiCoO2中Co的化合价为
(2)“微波共熔”中氯化胆碱-草酸和LiCoO2粗品以不同的液固比在120℃下微波处理10 min后锂和钴的浸取率如图,则最佳液固比为
(4)25℃时,“沉钴”反应完成后溶液pH=10,此时c(Co2+)=
(5)“滤饼2”在高温烧结前需要洗涤、干燥,洗涤沉淀的实验操作为
(6)锂离子电池正极材料LiCoO2在多次充放电后结构发生改变生成Co3O4,导致电化学性能下降,使用LiOH和30%H2O2溶液可以实现LiCoO2的修复,则修复过程发生反应的化学方程式为
您最近一年使用:0次