河北省强基名校联盟2023-2024学年高二下学期高考一轮复习模底考试化学试题
河北
高三
阶段练习
2024-05-18
168次
整体难度:
适中
考查范围:
化学与STSE、常见无机物及其应用、化学反应原理、化学实验基础、有机化学基础、认识化学科学、物质结构与性质
河北省强基名校联盟2023-2024学年高二下学期高考一轮复习模底考试化学试题
河北
高三
阶段练习
2024-05-18
168次
整体难度:
适中
考查范围:
化学与STSE、常见无机物及其应用、化学反应原理、化学实验基础、有机化学基础、认识化学科学、物质结构与性质
一、单选题 添加题型下试题
1. “十四五”生态环保工作强调要落实“减污降碳”的总要求,下列说法错误的是
| A.开发太阳能、风能等新能源是践行低碳生活的有效途径 |
| B.煤气化技术的应用,可减少二氧化碳的排放利用 |
| C.对含酚废水进行回收利用和降解处理有利于保护环境 |
| D.聚乳酸(PLA)材料的应用能有效防止白色污染,是世界公认的环保材料 |
您最近一年使用:0次
2. 化学实验操作是进行科学实的基础。下列操作合理的是
|
|
| A.分离乙醇和水 | B.反应热的测定 |
|
|
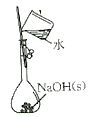
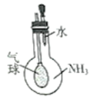
| C.配制一定物质的量浓度的NaOH溶液 | D.探究氨气在水中的溶解性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
3. 生物降解塑料能在微生物的作用下降解成二氧化碳和水,从而减少废分塑料对环境的污染。PHB就属于这种塑料,其结构简式为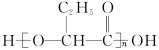 ,下列有关PHB的说法错误的是
,下列有关PHB的说法错误的是
| A.PHB是一种聚酯,没有有固定的熔点 |
| B.常温下,合成PHB的单体易溶于水 |
| C.合成PHB的单体是CH3CH2CH(OH)COOH |
| D.通过加聚反应可以制得PHB |
您最近一年使用:0次
单选题
|
适中(0.65)
4. 设NA为阿伏加德罗常教的值,下列说法正确的是
| A.标准状况22.4LCHCl3中含有的原子数为5NA |
| B.常温下,1 LpH=13的Ba(OH)2溶液中含OH-数为0.2 NA |
| C.12g金刚石晶体中含有的共价键数为2NA |
| D.常温需压下,28g乙烯和丙烯混合气体含有极性键数为2NA |
【知识点】 22.4L/mol适用条件解读 烯烃的通式解读 常见共价晶体的结构
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
5. 由苯甲醛制备重要的有机合成中间体的一种反应如下:
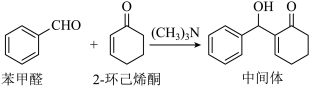
| A.该反应属于取代反应 |
| B.可用少量酸性高锰酸钾鉴别苯甲醛和2-环己烯酮 |
| C.2-环己烯酮中所有的原子可能共平面 |
D.中间体与足量 完全加成后所得分子中含有3个手性碳原子 完全加成后所得分子中含有3个手性碳原子 |
您最近一年使用:0次
2023-03-10更新
|
662次组卷
|
3卷引用:江苏省新高考基地学校2022-2023学年高三下学期3月大联考化学试题
单选题
|
适中(0.65)
解题方法
6. 下列叙述正确的是
| A.BeCl2分子中两个Be—Cl键间的夹角为180°,是由极性键构成的非极性分子 |
| B.H2O是一种非常稳定的化合物,这是由于氢键所致 |
| C.CH4和H2O的VSEPR模型分别为正四面体和V形 |
D. 和 和 的空间结构均为三角锥形 的空间结构均为三角锥形 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
7. (NH4)2Fe(SO4)2·6H2O广泛应用于实验室和工业领域,其晶体的部分结构如图所示。下列说法正确的是
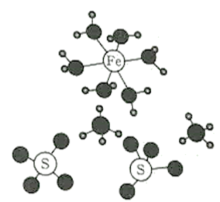
| A.电负性:O>S>Fe>H |
| B.基态Fe2+的外围电子排布式为3d44s2 |
| C.晶体中N和S原子的轨道杂化类型均为sp3 |
| D.晶体中存在的化学键有离子键、共价键、配位键和氢键 |
您最近一年使用:0次
8. 离子液体被广泛应用于化工生产的分离过程,也是许多反应的优良溶剂。某离子液体结构如图所示。W、X、Y、Z为原子序数依次增大的主族元素,W、X和Y的原子序数之和为14,Z是第四周期元素。下列说法错误的是
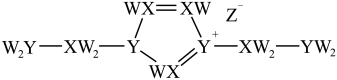
| A.X、Z的简单氢化物均可溶于水 |
| B.最高价氧化物的水化物酸性:Y>X |
| C.第一电离能:Y>X |
| D.X、Y、Z都位于元素周期表p区 |
您最近一年使用:0次
单选题
|
适中(0.65)
9. 下列实验操作能达到实验目的是
| 选项 | 实验目的 | 实验操作 |
| A | 除去甲烷气体中混有的乙烯 | 将混合气体通入盛有酸性KMnO4溶液的洗气瓶 |
| B | 比较氯和碳的非金属性强弱 | 将盐酸与NaHCO3溶液混合 |
| C | 检验溶液中的Fe3+ | 向待测液中滴加KSCN溶液 |
| D | 比较HClO和CH3COOH酸性强弱 | 用pH试纸测定等浓度HClO和CH3COOH溶液的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
10. 高铁酸钠(Na2FeO4)是一种新型绿色消毒制。 某化学兴趣小组用废铁屑(主要成分为Fe,杂质有Al、C及油脂)制备高铁酸钠的主要流程如下。下列说法错误的是
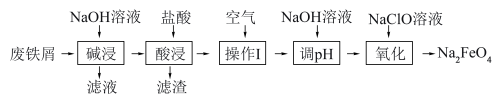
| A.“碱浸”可以除去废铁屑中的油脂 |
| B.“滤渣”的主要成分是Al和C |
| C.“操作I”通入空气发生反应的离子方程式为4Fe2+ +4H++O2=4Fe3++2H2O |
| D.高铁酸钠有强氧化性,消毒杀菌的同时产生胶体吸附杂质而净水 |
您最近一年使用:0次
单选题
|
较难(0.4)
名校
11. 朱砂(硫化汞)能降低大脑中枢神经的兴奋性,有镇静安眠作用。其立方晶系β型晶胞如图所示,晶胞参数为a nm,A原子的分数坐标为(0,0,0),阿伏加德罗常数的值为NA,下列说法正确的是
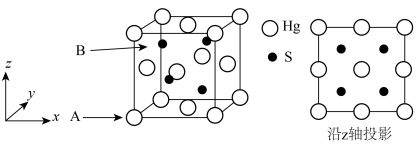
| A.S的配位数是8 |
B.晶胞中B原子分数坐标为( , ,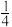 , , ) ) |
C.该晶体的密度ρ=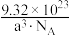 g/cm3 g/cm3 |
D.距离最近的两个Hg之间的距离为 a nm a nm |
您最近一年使用:0次
2024-06-06更新
|
118次组卷
|
2卷引用:河北省强基名校联盟2023-2024学年高二下学期高考一轮复习模底考试化学试题
单选题
|
适中(0.65)
解题方法
12. 室温下,某溶液初始时仅 A,同时发生两个反应:①A B+C;②A
B+C;②A B+D,反应①的速率可表示为v1=k1c(A),反应②的速率可表示为v2=k2c(A), (k1、k2为速率常数),图1为T2时,该体系中A、B、C、D的浓度随时间变化的曲线,图2为反应①和②的lnk—
B+D,反应①的速率可表示为v1=k1c(A),反应②的速率可表示为v2=k2c(A), (k1、k2为速率常数),图1为T2时,该体系中A、B、C、D的浓度随时间变化的曲线,图2为反应①和②的lnk— 曲线,下列说法正确的是
曲线,下列说法正确的是
 B+C;②A
B+C;②A B+D,反应①的速率可表示为v1=k1c(A),反应②的速率可表示为v2=k2c(A), (k1、k2为速率常数),图1为T2时,该体系中A、B、C、D的浓度随时间变化的曲线,图2为反应①和②的lnk—
B+D,反应①的速率可表示为v1=k1c(A),反应②的速率可表示为v2=k2c(A), (k1、k2为速率常数),图1为T2时,该体系中A、B、C、D的浓度随时间变化的曲线,图2为反应①和②的lnk— 曲线,下列说法正确的是
曲线,下列说法正确的是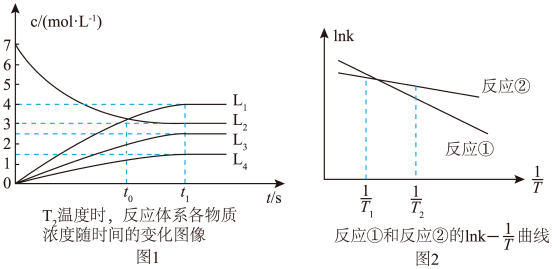
| A.L4表示B浓度随时间变化曲线 |
| B.t1≈2s时曲线L1表示的物质的化学反应速率为2 mol/(L·s) |
| C.T2温度时,反应①的活化能比反应②的活化能大 |
D.若图Ⅰ的温度降低,t0时刻体系中 值变小 值变小 |
您最近一年使用:0次
13. 以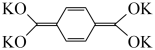 和N,N-二蒽醌-花酰二亚胺( PTCDI-DAQ)作电极的新型有机钾离子电池的综合性能达到了世界领先水平,该电池的工作原理如图。下列说法正确的是
和N,N-二蒽醌-花酰二亚胺( PTCDI-DAQ)作电极的新型有机钾离子电池的综合性能达到了世界领先水平,该电池的工作原理如图。下列说法正确的是
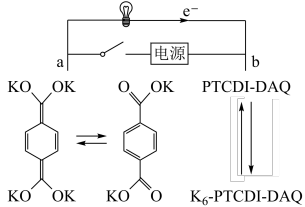
| A.放电时,a极为正极 |
B.放电时,a极电极反应式为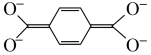 +2e-= +2e-=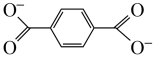 |
| C.充电时,K+由b极移向a极 |
| D.充电时,a极与电源正极相连 |
【知识点】 二次电池 电解原理的应用 原电池、电解池综合考查解读
您最近一年使用:0次
14. 25℃时,PbR(R2-为 或
或 )的沉淀溶解平衡关系如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法错误的是
)的沉淀溶解平衡关系如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法错误的是
 或
或 )的沉淀溶解平衡关系如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法错误的是
)的沉淀溶解平衡关系如图所示。已知Ksp(PbCO3)<Ksp(PbSO4),下列说法错误的是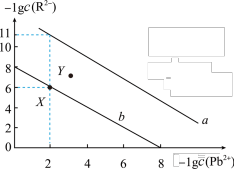
| A.b表示PbSO4的沉淀溶解平衡曲线 |
| B.Y点溶液是PbSO4的不饱和溶液 |
| C.X点对应的溶液中加入少量Pb(NO3)2固体,可转化为Y点对应的溶液 |
D.当PbSO4和PbCO3沉淀共存时,溶液中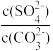 =1×105 =1×105 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
解题方法
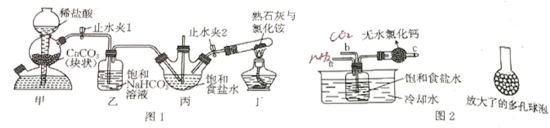
15. 化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献。模拟侯氏制碱法的主要过程如图1所示(夹持装置已略去)。__________ 。
(2)丙中进行反应时,应先通入_____ (填写化学式)气体, 发生反应的化学方程式为____________ 。
(3)丁中制备气体的反应物________ (填写“能”或“不能”)只使用氯化铵固体,原因是_____________ 。
(4)某化学兴趣小组选用图2装置进行实验室模拟侯氏制碱(夹持装置及其他装置已略去),并将多孔球泡连接到b管下端,这样设计的优点是_________ ,原因是____________ 。
(5)为使NH4Cl充分析出并分离,向析出NaHCO3后过滤得到的母液中加入NaCl粉末,发生NaCl(s)+NH4Cl(aq) NaCl(aq)+NH4Cl(s)过程。根据NaCl和NH4Cl溶解度曲线(图3),需采用的后续操作为
NaCl(aq)+NH4Cl(s)过程。根据NaCl和NH4Cl溶解度曲线(图3),需采用的后续操作为_______ 、_______ 、过滤 、洗涤、干燥。
(2)丙中进行反应时,应先通入
(3)丁中制备气体的反应物
(4)某化学兴趣小组选用图2装置进行实验室模拟侯氏制碱(夹持装置及其他装置已略去),并将多孔球泡连接到b管下端,这样设计的优点是
(5)为使NH4Cl充分析出并分离,向析出NaHCO3后过滤得到的母液中加入NaCl粉末,发生NaCl(s)+NH4Cl(aq)
 NaCl(aq)+NH4Cl(s)过程。根据NaCl和NH4Cl溶解度曲线(图3),需采用的后续操作为
NaCl(aq)+NH4Cl(s)过程。根据NaCl和NH4Cl溶解度曲线(图3),需采用的后续操作为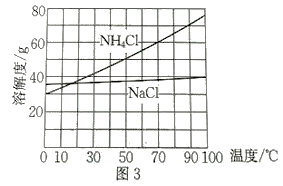
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
解题方法
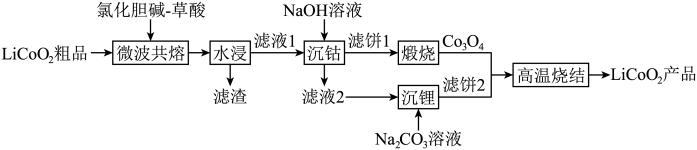
16. 利用“微波辅助低共熔溶剂”浸取废旧锂离子电池中钴酸锂粗品制备LiCoO2产品,以实现资源的循环利用。主要工艺之流程如下:
②Co2+在溶液中常以[CoCl4]2-(蓝色)和[Co(H2O)6]2+(粉红色)形式存在;
③25℃时, Ksp[Co(OH)2]=1.6×10-15。
回答下列问题:
(1)LiCoO2中Co的化合价为__________ 。
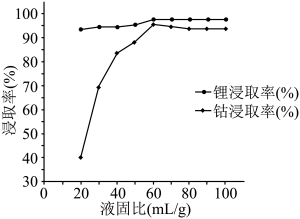
(2)“微波共熔”中氯化胆碱-草酸和LiCoO2粗品以不同的液固比在120℃下微波处理10 min后锂和钴的浸取率如图,则最佳液固比为______ mL/g,草酸的作用为_____________ 。________ 。
(4)25℃时,“沉钴”反应完成后溶液pH=10,此时c(Co2+)=______ mol/L。
(5)“滤饼2”在高温烧结前需要洗涤、干燥,洗涤沉淀的实验操作为__________ 。
(6)锂离子电池正极材料LiCoO2在多次充放电后结构发生改变生成Co3O4,导致电化学性能下降,使用LiOH和30%H2O2溶液可以实现LiCoO2的修复,则修复过程发生反应的化学方程式为__________ 。
②Co2+在溶液中常以[CoCl4]2-(蓝色)和[Co(H2O)6]2+(粉红色)形式存在;
③25℃时, Ksp[Co(OH)2]=1.6×10-15。
回答下列问题:
(1)LiCoO2中Co的化合价为
(2)“微波共熔”中氯化胆碱-草酸和LiCoO2粗品以不同的液固比在120℃下微波处理10 min后锂和钴的浸取率如图,则最佳液固比为
(4)25℃时,“沉钴”反应完成后溶液pH=10,此时c(Co2+)=
(5)“滤饼2”在高温烧结前需要洗涤、干燥,洗涤沉淀的实验操作为
(6)锂离子电池正极材料LiCoO2在多次充放电后结构发生改变生成Co3O4,导致电化学性能下降,使用LiOH和30%H2O2溶液可以实现LiCoO2的修复,则修复过程发生反应的化学方程式为
您最近一年使用:0次
17. CO2的转化利用对化解全球环境生态危机,实现全球碳达峰和碳中和有着重要的意义。
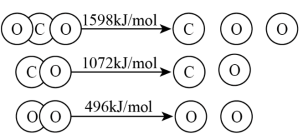
(1)以TiO2为催化剂的光热化学循环可以分解CO2生成CO和O2。已知气态分子中化学键完全断裂时的能量变化如图所示,则CO2分解的热化学方程式为_________ 。
ⅰ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-58. 6kJ/mol
CH3OH(g)+H2O(g) △H=-58. 6kJ/mol
ⅱ. CO2(g)+H2(g) CO(g)+H2O(g) △H=+41.2kJ/mol
CO(g)+H2O(g) △H=+41.2kJ/mol
①若在绝热条件下,将CO2(g)、H2(g)按体积比1:2充入恒容密闭容器中只发生反应ⅱ,下列能判断反应ⅱ达到平衡状态的是______
A.容器内混合气体的压强不变 B.容器内混合气体的密度不变
C.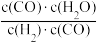 不变 D. v(CO2)=v(CO)
不变 D. v(CO2)=v(CO)
②若在一定温度下,向2 L恒容密闭容器中充入3molCO2和5mol H2,若只发生反应i,达到平衡时H2的转化率为60%,则平衡时CH3OH的浓度为________ ,该温度下,反应i的化学平衡常数K=___________ 。
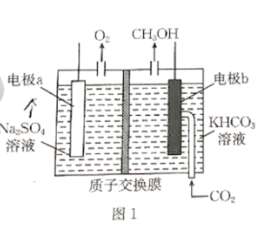
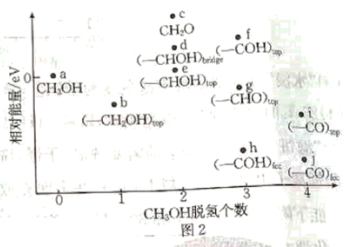
(3)电解法也可以将CO2转化为甲醇,原理如图1所示,则电极b为____ 极,电极a上的电极反应式为_____________ 。__________ (用b~j等代号表示)。
(1)以TiO2为催化剂的光热化学循环可以分解CO2生成CO和O2。已知气态分子中化学键完全断裂时的能量变化如图所示,则CO2分解的热化学方程式为
ⅰ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-58. 6kJ/mol
CH3OH(g)+H2O(g) △H=-58. 6kJ/molⅱ. CO2(g)+H2(g)
 CO(g)+H2O(g) △H=+41.2kJ/mol
CO(g)+H2O(g) △H=+41.2kJ/mol①若在绝热条件下,将CO2(g)、H2(g)按体积比1:2充入恒容密闭容器中只发生反应ⅱ,下列能判断反应ⅱ达到平衡状态的是
A.容器内混合气体的压强不变 B.容器内混合气体的密度不变
C.
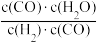 不变 D. v(CO2)=v(CO)
不变 D. v(CO2)=v(CO)②若在一定温度下,向2 L恒容密闭容器中充入3molCO2和5mol H2,若只发生反应i,达到平衡时H2的转化率为60%,则平衡时CH3OH的浓度为
(3)电解法也可以将CO2转化为甲醇,原理如图1所示,则电极b为
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
解题方法
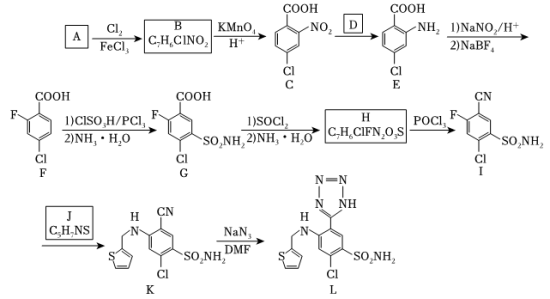
18. 阿佐塞米(化合物L)是一种可用于治疗心脏肝脏和肾脏病引起的水肿的药物。L的一种合成路线如图(部分试剂和条件略去)。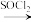 RCOCl
RCOCl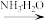 R-CONH2
R-CONH2
回答下列问题:
(1)A的化学名称是_______ 。
(2)由A生成B的化学方程式为___________ 。C的分子式为_________ 。
(3)C生成E的反应类型为___________ 。
(4)F中含氧官能团的名称是_________ 。
(5)化合物J的结构简式为__________ 。
(6)具有相同官能团的B的芳香族同分异构体还有_______ 种(不考虑立体异构,填标号)。
a.10 b.12 c.14 d.16
其中,核磁共振氢谱显示4组峰,且峰面积比为2:2:1:1的同分异构体结构简式为_______________ 。
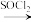 RCOCl
RCOCl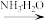 R-CONH2
R-CONH2回答下列问题:
(1)A的化学名称是
(2)由A生成B的化学方程式为
(3)C生成E的反应类型为
(4)F中含氧官能团的名称是
(5)化合物J的结构简式为
(6)具有相同官能团的B的芳香族同分异构体还有
a.10 b.12 c.14 d.16
其中,核磁共振氢谱显示4组峰,且峰面积比为2:2:1:1的同分异构体结构简式为
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学与STSE、常见无机物及其应用、化学反应原理、化学实验基础、有机化学基础、认识化学科学、物质结构与性质
试卷题型(共 18题)
题型
数量
单选题
14
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 处理污水的几种方法 高分子材料 绿色化学与可持续发展 新能源的开发 | |
| 2 | 0.65 | 氨与水的反应 中和热的测定与误差分析 配制一定物质的量浓度的溶液的步骤、操作 萃取和分液 | |
| 3 | 0.65 | 缩聚反应 缩聚物的单体、链节及聚合度的确定 多官能团有机物的结构与性质 | |
| 4 | 0.65 | 22.4L/mol适用条件 烯烃的通式 常见共价晶体的结构 | |
| 5 | 0.65 | 有机官能团的性质及结构 分子的手性 有机分子中原子共面的判断 醛基的加成反应 | |
| 6 | 0.65 | 价层电子对互斥理论的应用 极性分子和非极性分子 氢键对物质性质的影响 | |
| 7 | 0.65 | 电子排布式 元素性质与电负性的关系 共价键的形成及主要类型 利用杂化轨道理论判断化学键杂化类型 | |
| 8 | 0.65 | 元素非金属性强弱的比较方法 根据原子结构进行元素种类推断 电子排布式 电离能变化规律 | |
| 9 | 0.65 | 次氯酸及其性质 Fe3+的检验 乙烯与强氧化性物质的反应 元素非金属性强弱的比较方法 | |
| 10 | 0.65 | 胶体的性质和应用 有关铁及其化合物转化的流程题型 油脂在碱性条件下水解 物质分离、提纯综合应用 | |
| 11 | 0.4 | 晶胞的有关计算 | |
| 12 | 0.65 | 化学反应速率计算 活化能及其对反应速率的影响 外界条件对化学平衡影响的图像 | |
| 13 | 0.65 | 二次电池 电解原理的应用 原电池、电解池综合考查 | |
| 14 | 0.65 | 沉淀转化 溶度积规则及其应用 溶度积常数相关计算 | |
| 二、解答题 | |||
| 15 | 0.65 | 氨气的实验室制法 碳酸氢钠的不稳定性 物质制备的探究 纯碱的生产 | 实验探究题 |
| 16 | 0.65 | 溶度积常数相关计算 化学实验基础操作 物质分离、提纯综合应用 | 工业流程题 |
| 17 | 0.65 | 根据△H=反应物的键能之和-生成物的键能之和进行计算 化学平衡状态的判断方法 化学平衡常数的有关计算 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |
| 18 | 0.65 | 同分异构体的数目的确定 苯的同系物使高锰酸钾褪色的机理 羧酸化学性质 有机合成综合考查 | 有机推断题 |