名校
1 . 工业上采用Si与HCl在350℃左右反应生成 ,之后将其还原、结晶得到高纯度的单晶硅产品。已知
,之后将其还原、结晶得到高纯度的单晶硅产品。已知 的熔点为-128℃,沸点为33℃,且遇
的熔点为-128℃,沸点为33℃,且遇 和
和 均剧烈反应。现要在实验室中制取少量
均剧烈反应。现要在实验室中制取少量 ,其实验装置如下图所示,则下列说法正确的是
,其实验装置如下图所示,则下列说法正确的是
 ,之后将其还原、结晶得到高纯度的单晶硅产品。已知
,之后将其还原、结晶得到高纯度的单晶硅产品。已知 的熔点为-128℃,沸点为33℃,且遇
的熔点为-128℃,沸点为33℃,且遇 和
和 均剧烈反应。现要在实验室中制取少量
均剧烈反应。现要在实验室中制取少量 ,其实验装置如下图所示,则下列说法正确的是
,其实验装置如下图所示,则下列说法正确的是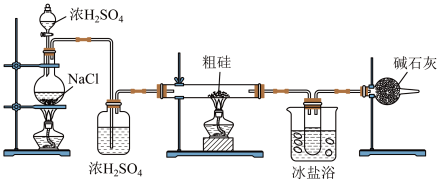
| A.反应时,应该先点燃“粗硅”处的酒精灯 |
B.冰盐浴的目的为降低收集容器的温度,使 冷凝头液体 冷凝头液体 |
C.可以用无水 替换干燥管中的碱石灰 替换干燥管中的碱石灰 |
D.使用浓 和NaCl混合加热制取HCl利用了浓 和NaCl混合加热制取HCl利用了浓 的脱水性和强酸性 的脱水性和强酸性 |
您最近一年使用:0次
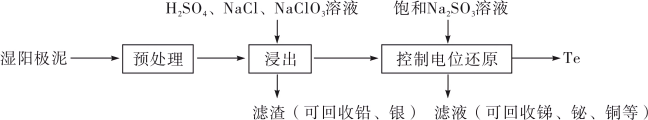
2 . 碲(Te)是一种重要的稀有分散元素,广泛应用于冶金、石油、化工、航空、电子等领域。以某冶炼厂的湿阳极泥(含水26%,主要含锑、砷、铅、铋、银和少量铜、碲等)为原料回收碲的流程如下:
请回答下列问题:
(1) 的基态原子的电子排布式为
的基态原子的电子排布式为___________ 。
(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是___________ ;氧化后的原料还需粉碎、过筛,目的是___________ 。
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为___________ 、___________ ;添加 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式___________ 。
(4)电解时为防止除Te以外的单质生成,需控制电位的范围为___________ ;加入饱和 溶液还原
溶液还原 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成___________ (填化学式)。
(5)碲可用于制备半导体材料碲化锌,其立方晶胞结构如图所示。以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。A点碲原子坐标为 ,C点锌原子坐标为
,C点锌原子坐标为 ,则B点锌原子坐标为
,则B点锌原子坐标为___________ 。若Te的原子半径为rpm,碲化锌晶胞中面心与顶点的碲原子相切,晶体的密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数
___________  (列出计算式)。
(列出计算式)。
| 物质 | 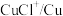 | 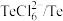 | 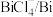 | 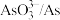 | 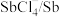 |
| 氧化还原电位(E)/V | 0.342 | 0.568 | 0.16 | 小于0.16 | 小于0.16 |
(1)
 的基态原子的电子排布式为
的基态原子的电子排布式为(2)原料预处理可采用干燥箱中加热氧化或自然堆放氧化(四天以上)两种方式,两相比较,后者的主要优点是
(3)浸出时,所得滤渣主要含铅、银的化合物,其化学式分别为
 可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出
可显著提高碲和铜的浸出率,说明预处理后的原料中仍存在低价态的碲和铜,写出 转化为
转化为 、
、 而被浸出的离子方程式
而被浸出的离子方程式(4)电解时为防止除Te以外的单质生成,需控制电位的范围为
 溶液还原
溶液还原 可减少电能消耗并防止阳极生成
可减少电能消耗并防止阳极生成(5)碲可用于制备半导体材料碲化锌,其立方晶胞结构如图所示。以晶胞参数为单位长度建立坐标系,可以表示晶胞中各原子的位置,称为原子坐标。A点碲原子坐标为
 ,C点锌原子坐标为
,C点锌原子坐标为 ,则B点锌原子坐标为
,则B点锌原子坐标为 ,则阿伏加德罗常数
,则阿伏加德罗常数
 (列出计算式)。
(列出计算式)。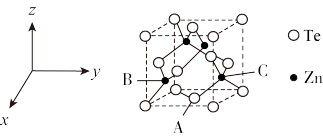
您最近一年使用:0次
解题方法
3 . 实验室里能用来直接加热的仪器是
| A.试管 | B.烧瓶 | C.烧杯 | D.量筒 |
您最近一年使用:0次
名校
4 . 有机物M(只含C、H、O三种元素)具有令人愉悦的牛奶香气,主要用于配制奶油、乳品、酸奶和草莓等型香精,是我国批准使用的香料产品,其沸点为148℃。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:
步骤一:将粗品用蒸馏法进行纯化。
(1)蒸馏装置如图1所示,图中虚线框内应选用右侧的___________ (填“仪器x”或“仪器y”),该仪器使用时冷水从___________ 口进 (填数字)。
元素分析是有机化合物的表征手段之一、按下图实验装置(部分装置略)对M进行C、H元素分析。___________ (a或者b),进行实验。
(3)c和d中的试剂分别是___________ 、___________ (填标号)。
A.CaCl2 B.NaCl C.碱石灰(CaO+NaOH) D.浓硫酸
(4)Pt坩埚中样品M反应完全后,熄灭燃煤气灯,继续通入氧气至石英管冷却至室温。
①整个过程中氧气的作用除氧化有机物外,还有的作用是___________ 、___________ (答出2点) 。
②取下c和d管称重。若样品M为0.88 g,实验结束后,c管增重0.72 g,d管增重1.76 g。
已知M的密度是同温同压下二氧化碳密度的2倍,则M的分子式为___________ 。
步骤三:确定M的结构简式。
(5)用核磁共振仪测出M的核磁共振氢谱如图2所示,图中峰面积之比为1∶3∶1∶3;利用红外光谱仪测得M的红外光谱如图3所示___________ (填键线式)。
(6)写出一种含有羧基的M的同分异构体G的结构简式:___________ 。
(7)下列方法中不能对鉴别M和G二者进行鉴别的是___________。
步骤一:将粗品用蒸馏法进行纯化。
(1)蒸馏装置如图1所示,图中虚线框内应选用右侧的

元素分析是有机化合物的表征手段之一、按下图实验装置(部分装置略)对M进行C、H元素分析。

(3)c和d中的试剂分别是
A.CaCl2 B.NaCl C.碱石灰(CaO+NaOH) D.浓硫酸
(4)Pt坩埚中样品M反应完全后,熄灭燃煤气灯,继续通入氧气至石英管冷却至室温。
①整个过程中氧气的作用除氧化有机物外,还有的作用是
②取下c和d管称重。若样品M为0.88 g,实验结束后,c管增重0.72 g,d管增重1.76 g。
已知M的密度是同温同压下二氧化碳密度的2倍,则M的分子式为
步骤三:确定M的结构简式。
(5)用核磁共振仪测出M的核磁共振氢谱如图2所示,图中峰面积之比为1∶3∶1∶3;利用红外光谱仪测得M的红外光谱如图3所示

(6)写出一种含有羧基的M的同分异构体G的结构简式:
(7)下列方法中不能对鉴别M和G二者进行鉴别的是___________。
| A.元素分析 | B.核磁共振氢谱 | C.红外光谱法 | D.原子光谱 |
您最近一年使用:0次
5 . 使用下图所示装置及试剂进行实验,能达到目的的是
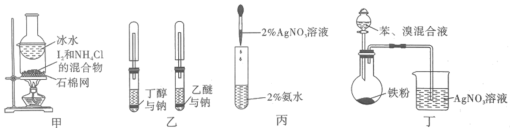
A.装置甲可用于分离提纯 |
B.装置乙可用于鉴别丁醇与乙醚( ) ) |
| C.装置丙可用于实验室配制银氨溶液 |
| D.装置丁可用于制备溴苯并验证有HBr产生 |
您最近一年使用:0次
2024-04-18更新
|
300次组卷
|
2卷引用:2024届”3+3+3“高考备考诊断性联考卷(二)理综试题-高中化学
解题方法
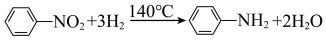
6 . 苯胺(有机碱,常温下为无色油状液体,易被氧化)在染料、医药、农药、香料等领域有广泛的应用。实验室以硝基苯为原料制备苯胺,反应原理如下:
实验步骤为:
①组装好实验装置(如图,部分夹持仪器已略去),并检查装置气密性。
②向三颈烧瓶中依次加入沸石及10mL硝基苯。
③打开活塞K,先通入H2一段时间。
④使三颈烧瓶内溶液保持140℃恒温,充分反应。
⑤反应结束后,关闭活塞K,向三颈烧瓶中加入干燥剂。
⑥继续加热,收集182~186℃馏分,将所得馏分进行二次纯化,最终得到较纯苯胺5.6g。
回答下列问题:___________ 。
(2)长颈漏斗内的试剂最好选用___________ 。
a.稀盐酸 b.稀硝酸 c.稀硫酸
(3)A装置是一个简易启普发生器,其优点是___________ ,若实验中未先通入H2一段时间,则可能产生的不良后果是___________ 。
(4)步骤⑤中干燥剂可选用___________ 。
a.浓硫酸 b.碱石灰 c.无水硫酸镁 d.五氧化二磷
(5)二次纯化并测定产率:
蒸馏所得苯胺中混有少量硝基苯杂质,可以采用如下方案除杂提纯:___________ ,“液相”是___________ (填“水层”或“有机层”)。
(6)苯胺与甲苯相对分子质量相近,但沸点相差较大,试从物质结构的角度说明原因___________ 。
(7)本实验的产率为___________ (保留一位小数)。
| 物质 | 相对分子质量 | 沸点/℃ | 密度g/mL | 溶解性 |
| 硝基苯 | 123 | 210.9 | 1.23 | 不溶于水,易溶于乙醇、乙醚 |
| 苯胺 | 93 | 184.4 | 1.02 | 微溶于水,易溶于乙醇、乙醚 |
| 甲苯 | 92 | 110.6 | 0.872 | 略 |
①组装好实验装置(如图,部分夹持仪器已略去),并检查装置气密性。
②向三颈烧瓶中依次加入沸石及10mL硝基苯。
③打开活塞K,先通入H2一段时间。
④使三颈烧瓶内溶液保持140℃恒温,充分反应。
⑤反应结束后,关闭活塞K,向三颈烧瓶中加入干燥剂。
⑥继续加热,收集182~186℃馏分,将所得馏分进行二次纯化,最终得到较纯苯胺5.6g。
回答下列问题:

(2)长颈漏斗内的试剂最好选用
a.稀盐酸 b.稀硝酸 c.稀硫酸
(3)A装置是一个简易启普发生器,其优点是
(4)步骤⑤中干燥剂可选用
a.浓硫酸 b.碱石灰 c.无水硫酸镁 d.五氧化二磷
(5)二次纯化并测定产率:
蒸馏所得苯胺中混有少量硝基苯杂质,可以采用如下方案除杂提纯:

(6)苯胺与甲苯相对分子质量相近,但沸点相差较大,试从物质结构的角度说明原因
(7)本实验的产率为
您最近一年使用:0次
7 . 下列做法不正确的是
| A.配制一定体积某浓度的稀硫酸,浓硫酸稀释后直接转移至容量瓶,所配溶液浓度偏大 |
| B.做焰色试验所用的铂丝应先蘸稀盐酸,再放在火焰上烧至无色 |
| C.实验剩余的钠单质应该放回到原试剂瓶中 |
D. 和 和 溶液分别与少量氯水反应,根据现象可判断溴与碘的非金属性强弱 溶液分别与少量氯水反应,根据现象可判断溴与碘的非金属性强弱 |
您最近一年使用:0次
8 . 如图所示的实验操作或装置正确的是
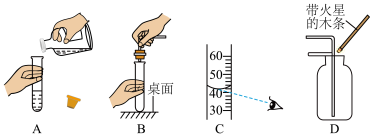

| A.倾倒液体 |
| B.把橡皮塞塞进试管口 |
| C.读取液体体积 |
| D.验满O2 |
您最近一年使用:0次
9 . 最近小明对水产生了浓厚的兴趣。

(1)在化学课堂上,老师进行了电解水的实验,揭示了水的组成。右图实验中试管1中得到的气体在点燃之前要先进行验纯的原因是_____ 。
(2)小明放学回家后,主动帮妈妈刷碗,发现自来水洗不掉碗碟上的油污,发现加入少许洗涤剂就可以洗干净,是因为洗涤剂有_____ 作用。
(3)周末他取村子里的河水于玻璃杯中,倒入少量肥皂水,用筷子搅拌后发现有大量浮渣漂浮在水面上,无泡沫产生,说明河水是_____ (选填“硬水”或“软水”)。硬水的危害很大,生活中将硬水软化的方法是_____ 。
(4)晚上,小明在电视上看到保护水资源的呼吁。下列做法中,你认为有利于防治水体污染的是_____。
(5)小明从课本学习到水常用作溶剂,实验室配制质量分数为0.9%的氯化钠溶液,小明用量筒量取蒸馏水读数时,仰视凹液面的最低处,会引起所配溶液的溶质质量分数_____ (选填“大于”、“小于”或“等于”)0.9%。

(1)在化学课堂上,老师进行了电解水的实验,揭示了水的组成。右图实验中试管1中得到的气体在点燃之前要先进行验纯的原因是
(2)小明放学回家后,主动帮妈妈刷碗,发现自来水洗不掉碗碟上的油污,发现加入少许洗涤剂就可以洗干净,是因为洗涤剂有
(3)周末他取村子里的河水于玻璃杯中,倒入少量肥皂水,用筷子搅拌后发现有大量浮渣漂浮在水面上,无泡沫产生,说明河水是
(4)晚上,小明在电视上看到保护水资源的呼吁。下列做法中,你认为有利于防治水体污染的是_____。
| A.使用节水型马桶 | B.生活污水任意排放 |
| C.合理施用农药和化肥 | D.工业废水处理达标后排放 |
(5)小明从课本学习到水常用作溶剂,实验室配制质量分数为0.9%的氯化钠溶液,小明用量筒量取蒸馏水读数时,仰视凹液面的最低处,会引起所配溶液的溶质质量分数
您最近一年使用:0次
10 . 如图是木炭与氧化铜反应的实验装置图,下列说法错误 的是
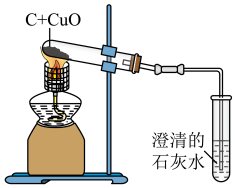

| A.进行实验前,应先检查装置的气密性 |
| B.实验过程中,可观察到试管里的黑色固体变为红色 |
| C.实验结束后,应先停止加热,再将导气管从澄清石灰水中撤出 |
D.加热时,试管中发生反应的化学方程式为C+2CuO 2Cu+CO2↑ 2Cu+CO2↑ |
您最近一年使用:0次



