名校
1 . 聚磷酸铵(APP)具有良好的水溶性(溶解性随温度升高显著增大)、改良土壤等特性,成为一种新型的含氮、磷复合肥。
回答下列问题:
(一)聚磷酸铵的制备
步骤1.将磷酸二氢铵 、尿素
、尿素 (熔点132℃,沸点196℃)等原料按照一定的比例加入到仪器
(熔点132℃,沸点196℃)等原料按照一定的比例加入到仪器 中进行搅拌混合,加热至140℃至物料全部熔化。
中进行搅拌混合,加热至140℃至物料全部熔化。
步骤2.继续升温到250℃进行聚合反应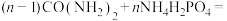
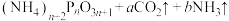 ,同时会发生尿素的水解。
,同时会发生尿素的水解。
步骤3.待聚合反应完成,进行一系列操作后洗涤干燥,最终得到全水溶性聚磷酸铵晶体(样品)。
(二)氮含量测定
用如图所示的装置进行氮含量测定(部分装置已省略): 样品(杂质不参与反应)加入过量试剂后,加热,蒸出的
样品(杂质不参与反应)加入过量试剂后,加热,蒸出的 通入盛有
通入盛有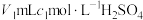 标准溶液的锥形瓶中。
标准溶液的锥形瓶中。
②滴定:将液封装置2中溶液倒入锥形瓶后,滴加几滴指示剂,用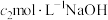 溶液滴定剩余的
溶液滴定剩余的 ,到达滴定终点时消耗
,到达滴定终点时消耗 溶液。
溶液。
(1)仪器 的名称为
的名称为_______ ;加热至140℃待物料全部熔化后再继续升温到250℃,若直接升高温度至250℃产生的影响为_______ 。
(2)聚合反应方程式中 为
为_______ (用含 的代数式表示);尿素发生水解反应的化学方程式为
的代数式表示);尿素发生水解反应的化学方程式为_______ 。
(3)步骤3中待聚合反应完成后进行的一系列操作为_______ 。
(4)氮含量测定实验中,液封装置1的作用是_______ 。
(5)滴定实验中使用的指示剂是_______ ,该复合肥含氮量为_______  (用含
(用含 、
、 、
、 、
、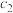 、x的代数式表示)。
、x的代数式表示)。
回答下列问题:
(一)聚磷酸铵的制备
步骤1.将磷酸二氢铵
 、尿素
、尿素 (熔点132℃,沸点196℃)等原料按照一定的比例加入到仪器
(熔点132℃,沸点196℃)等原料按照一定的比例加入到仪器 中进行搅拌混合,加热至140℃至物料全部熔化。
中进行搅拌混合,加热至140℃至物料全部熔化。步骤2.继续升温到250℃进行聚合反应
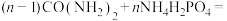
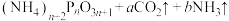 ,同时会发生尿素的水解。
,同时会发生尿素的水解。步骤3.待聚合反应完成,进行一系列操作后洗涤干燥,最终得到全水溶性聚磷酸铵晶体(样品)。
(二)氮含量测定
用如图所示的装置进行氮含量测定(部分装置已省略):
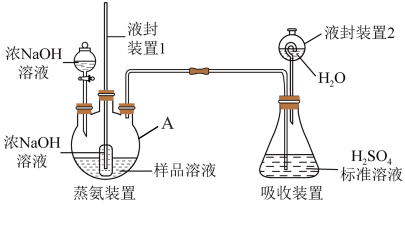
 样品(杂质不参与反应)加入过量试剂后,加热,蒸出的
样品(杂质不参与反应)加入过量试剂后,加热,蒸出的 通入盛有
通入盛有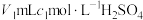 标准溶液的锥形瓶中。
标准溶液的锥形瓶中。②滴定:将液封装置2中溶液倒入锥形瓶后,滴加几滴指示剂,用
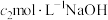 溶液滴定剩余的
溶液滴定剩余的 ,到达滴定终点时消耗
,到达滴定终点时消耗 溶液。
溶液。(1)仪器
 的名称为
的名称为(2)聚合反应方程式中
 为
为 的代数式表示);尿素发生水解反应的化学方程式为
的代数式表示);尿素发生水解反应的化学方程式为(3)步骤3中待聚合反应完成后进行的一系列操作为
(4)氮含量测定实验中,液封装置1的作用是
(5)滴定实验中使用的指示剂是
 (用含
(用含 、
、 、
、 、
、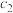 、x的代数式表示)。
、x的代数式表示)。
您最近一年使用:0次
2 . 苯与液溴在 催化下的取代反应是高中阶段重要的有机反应之一,请回答下列问题:
催化下的取代反应是高中阶段重要的有机反应之一,请回答下列问题:
(1)向苯与液溴反应后的橙红色溶液中滴加NaOH溶液,溶液逐渐褪色的化学方程式____________ ,但液体始终略带一些红褐色,试分析其原因:____________ 。
(2)为了进一步探究苯与液溴取代反应产物的相关性质,某实验小组用如图所示的处(夹持仪器略)进行实验。______ 。
②该装置中 的作用是
的作用是____________ ;该反应为取代反应的实验现象是__________________ 。
③反应结束后,向三颈烧瓶中加入蒸馏水进行水洗的目的是____________ 。
④为了观察到无色透明的溴苯,溴苯经过水洗后,将液体转移至分液漏斗中静置,溴苯从______ (填“上口倒出”或“下口放出”)至盛有 溶液的烧杯中,充分搅拌,
溶液的烧杯中,充分搅拌, 溶液的作用为
溶液的作用为______ (填离子方程式)。
 催化下的取代反应是高中阶段重要的有机反应之一,请回答下列问题:
催化下的取代反应是高中阶段重要的有机反应之一,请回答下列问题:(1)向苯与液溴反应后的橙红色溶液中滴加NaOH溶液,溶液逐渐褪色的化学方程式
(2)为了进一步探究苯与液溴取代反应产物的相关性质,某实验小组用如图所示的处(夹持仪器略)进行实验。
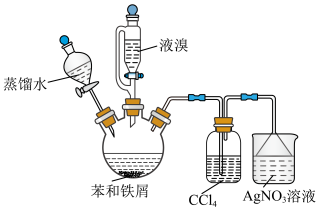
②该装置中
 的作用是
的作用是③反应结束后,向三颈烧瓶中加入蒸馏水进行水洗的目的是
④为了观察到无色透明的溴苯,溴苯经过水洗后,将液体转移至分液漏斗中静置,溴苯从
 溶液的烧杯中,充分搅拌,
溶液的烧杯中,充分搅拌, 溶液的作用为
溶液的作用为
您最近一年使用:0次
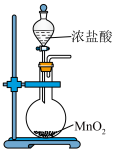
3 . 下列实验装置中能达到实验目的的是
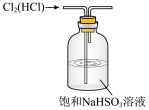 | 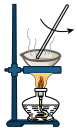 | 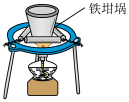 |  |
| A | B | C | D |
| A.除去Cl2中少量HCl | B.蒸干制备胆矾 | C.熔融纯碱 | D.制备Cl2 |
您最近一年使用:0次
7日内更新
|
246次组卷
|
2卷引用:安徽省合肥市2024届高三第三次教学质量检测化学试题
名校
4 . 过氧化锶(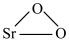 )通常用作分析试剂、氧化剂、漂白剂等。SrO2是一种白色粉末,加热条件下可与CO2、水蒸气反应,室温时在水中逐渐形成无色晶体SrO2·8H2O,与酸作用生成H2O2。
)通常用作分析试剂、氧化剂、漂白剂等。SrO2是一种白色粉末,加热条件下可与CO2、水蒸气反应,室温时在水中逐渐形成无色晶体SrO2·8H2O,与酸作用生成H2O2。
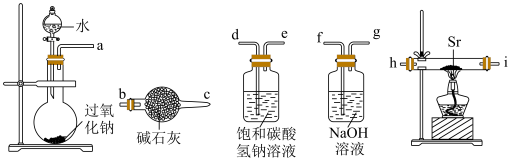
②SrO2在空气中会变质生成碳酸盐,写出该反应的化学方程式
③连接好装置进行实验,实验步骤如下,正确的操作顺序为
a、打开分液漏斗活塞,将水滴入烧瓶中b、检查装置气密性c、在相应装置中装入药品d、加热e、关闭分液漏斗活塞f、停止加热
(2)乙同学在通入氨气的条件下,在水溶液中可制备得到SrO2·8H2O,实验装置如图:
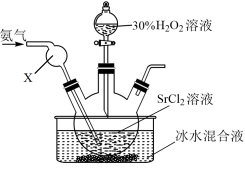
②写出该方法制备SrO2·8H2O的离子方程式
③实验结束后,得到SrO2·8H2O的操作为
(3)除SrO2·8H2O外,请选择下列试剂:FeCl2溶液、HCl溶液、HNO3溶液、KSCN溶液、H2O2溶液设计实验证明SrO2的氧化性比FeCl3的氧化性强:
您最近一年使用:0次
名校
解题方法
5 . 下列实验中,所选装置(可添加试剂,可重复使用)不合理的是
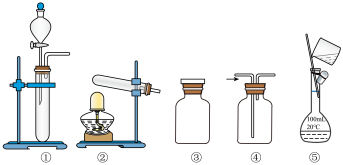
| A.配制100mL0.1mol/LNaOH溶液,选用⑤ |
| B.用KMnO4固体制备氧气,选用② |
| C.盛放Na2CO3溶液,选用③ |
| D.用大理石和盐酸制取CO2并比较碳酸和Na2SiO3的酸性强弱,选用①④ |
您最近一年使用:0次
6 . 课外实验可以帮助我们更好地学习化学知识。金属活动性强弱的探究过程如下,其中不正确的是(已知:白醋的水溶液显酸性,与稀盐酸的化学性质相似)
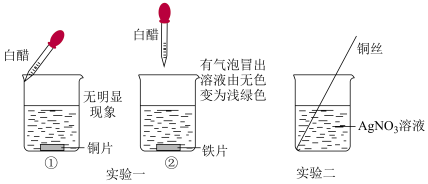
| A.实验一证明铁的金属活动性比铜强 |
| B.实验二的现象是铜丝不断减少,表面有银白色固体析出,无色溶液变为黄色 |
| C.实验一烧杯②中发生的是置换反应 |
| D.实验过程中存在不规范操作 |
您最近一年使用:0次
7 . 图中的实验方法或操作正确的是
|
|
| A.倾倒液体 | B.振荡试管 |
|
|
| C.稀释浓硫酸 | D.尾气处理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 焦亚硫酸钠( )可用作食品添加剂,其实验室制备的装置如下图所示。回答下列问题:
)可用作食品添加剂,其实验室制备的装置如下图所示。回答下列问题:___________ ,其作用为___________ 。
(2)圆底烧瓶中发生反应的化学方程式为___________ 。
(3)焦亚硫酸钠易被氧化而变质,选用下列试剂设计实验方案,检验焦亚硫酸钠样品氧化变质的程度。
试剂:稀盐酸、稀 、稀
、稀 、
、 溶液、酸性
溶液、酸性 溶液、
溶液、 溶液
溶液
(4)某小组利用下列装置测定空气中 的含量。
的含量。___________ (填A或B)连接到导管末端。
②已知:该反应的化学方程式为: ,若空气流速为
,若空气流速为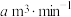 ,当观察到
,当观察到___________ 时,结束计时,测定耗时t min,假定样品中的 可被溶液充分吸收,该空气样品中
可被溶液充分吸收,该空气样品中 的含量是
的含量是___________ 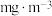 。
。
 )可用作食品添加剂,其实验室制备的装置如下图所示。回答下列问题:
)可用作食品添加剂,其实验室制备的装置如下图所示。回答下列问题: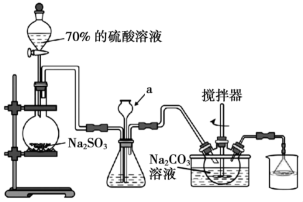
(2)圆底烧瓶中发生反应的化学方程式为
(3)焦亚硫酸钠易被氧化而变质,选用下列试剂设计实验方案,检验焦亚硫酸钠样品氧化变质的程度。
试剂:稀盐酸、稀
 、稀
、稀 、
、 溶液、酸性
溶液、酸性 溶液、
溶液、 溶液
溶液| 实验编号 | 实验步骤 | 现象 | 结论 |
| Ⅰ | 取少量样品,加入除氧蒸馏水,溶解完后平均分装到两支相同的小试管中 | 固体完全溶解得到无色溶液 | / |
| Ⅱ | 取实验I的溶液, | 出现白色沉淀 | 样品已氧化变质 |
| Ⅲ | 另取实验Ⅰ的溶液,加入酸性 溶液,充分振荡 溶液,充分振荡 | 溶液褪色 | 样品未完全氧化变质 |
 的含量。
的含量。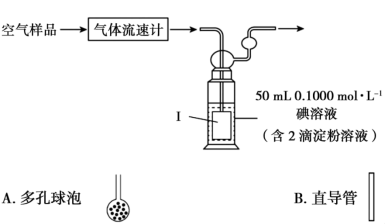
②已知:该反应的化学方程式为:
 ,若空气流速为
,若空气流速为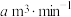 ,当观察到
,当观察到 可被溶液充分吸收,该空气样品中
可被溶液充分吸收,该空气样品中 的含量是
的含量是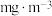 。
。
您最近一年使用:0次
9 . 下列实验装置及操作正确的是


| A.除去乙酸中的乙醇 | B.除去水中的苯酚 |
C.除去尾气中的 | D.除去溶在 中的 中的 |
您最近一年使用:0次
10 . 根据下列装置,回答问题:___________ 。
(2)实验室常用___________ (填药品名称)来制取二氧化碳气体,发生反应的化学方程式为___________ ;其发生装置可用A或B,与A装置相比,B装置的优点是___________ 。
(3)若用C装置加热高锰酸钾制取氧气,发生反应的化学方程式为___________ 。
(4)若用活泼金属单质和稀盐酸反应制取纯净、干燥的H2,请从这些装置中选择并连接成一套组合装置,按照气流从左到右的流向,写出所选装置接口的连接顺序:b→___________ 。
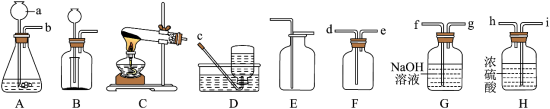
(2)实验室常用
(3)若用C装置加热高锰酸钾制取氧气,发生反应的化学方程式为
(4)若用活泼金属单质和稀盐酸反应制取纯净、干燥的H2,请从这些装置中选择并连接成一套组合装置,按照气流从左到右的流向,写出所选装置接口的连接顺序:b→
您最近一年使用:0次