某溶液中,可能含有下表所列离子中的某几种:
取少量该溶液,向其中加入某试剂X,产生沉淀的物质的量(n)与加入试剂X的体积(V)关系如下图所示:
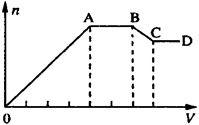
(1)若X是NaOH溶液,原溶液中一定含有的阴离子有___________ ;BC段反应的离子方程式为___________ 。
(2)若X是盐酸,则原溶液中一定含有的金属阳离子是___________ ;AB段发生反应的总离子方程式为___________ ;OA段生成沉淀的物质的量之比为___________ 。
| 阳离子 | Al3+、Mg2+、NH 、Na+ 、Na+ |
| 阴离子 | CO 、SiO 、SiO 、[Al(OH)4]-、Cl- 、[Al(OH)4]-、Cl- |

(1)若X是NaOH溶液,原溶液中一定含有的阴离子有
(2)若X是盐酸,则原溶液中一定含有的金属阳离子是
更新时间:2016-12-09 11:04:07
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】有一混合物水溶液,可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Fe3+、CO32—、SO42—,现各取100ml溶液三份进行如下实验:①向第一份加入AgNO3溶液,有白色沉淀产生②向第二份加入足量NaOH溶液后加热,收集到气体0.896L(标准状况)③向第三份加入足量BaCl2溶液,得到沉淀6.27克,沉淀经足量盐酸洗涤后,剩余2.33克。
试回答下列问题:
(1)肯定存在的离子有_____ ,肯定不存在的离子有_______ ,
(2)可能存在的离子是____________ ,
(3)试分别确定肯定存在的阳离子在原溶液中各自的物质的量浓度___________________ 。
试回答下列问题:
(1)肯定存在的离子有
(2)可能存在的离子是
(3)试分别确定肯定存在的阳离子在原溶液中各自的物质的量浓度
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】Ⅰ.为了除去KCl溶液中少量的Mg2+、SO42-,可选用Ba(OH)2、HCl和K2CO3三种试剂,按如下步骤操作:
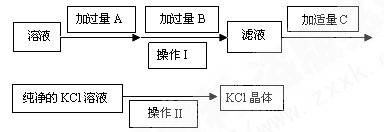
(1)上述试剂中,B是 ,C是 。
(2)操作Ⅱ的名称是 。
(3)加过量A时发生有关反应的离子方程式为 、 。
Ⅱ.一份溶液中可能含有K+、Al3+、H+、NH4+、Cl-、Br-、I-、ClO-、AlO2- 等离子中的若干种。为了确定溶液的组成,进行了如下操作:
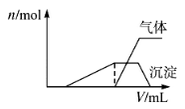
(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积关系如图所示;则该溶液中一定存在的离子是 ,一定不存在的离子是 。
(2)经检测后,该溶液中含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的氯气,则溶液中Cl-、Br-、I-与通入氯气的体积(标况下)关系如表所示,回答下列问题:
①则a为
②原溶液中Cl-、Br-、I-的物质的量浓度之比为

(1)上述试剂中,B是 ,C是 。
(2)操作Ⅱ的名称是 。
(3)加过量A时发生有关反应的离子方程式为 、 。
Ⅱ.一份溶液中可能含有K+、Al3+、H+、NH4+、Cl-、Br-、I-、ClO-、AlO2- 等离子中的若干种。为了确定溶液的组成,进行了如下操作:

(1)往该溶液中逐滴加入NaOH溶液并适当加热,产生沉淀和气体的物质的量(n)与加入NaOH溶液的体积关系如图所示;则该溶液中一定存在的离子是 ,一定不存在的离子是 。
(2)经检测后,该溶液中含有大量的Cl-、Br-、I-,若向1L该混合溶液中通入一定量的氯气,则溶液中Cl-、Br-、I-与通入氯气的体积(标况下)关系如表所示,回答下列问题:
| Cl2的体积(标况下) | 2.8L | 5.6L | 11.2L |
| n(Cl-) | 1.25mol | 1.5 mol | 2 mol |
| n(Br-) | 1.5 mol学] | 1.4mol | 0.9 mol |
| n(I-) | a mol | 0 | 0 |
②原溶液中Cl-、Br-、I-的物质的量浓度之比为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】化学是一门实验的科学,滴定法是一种常用的化学定量分析的方法。室温下,用 溶液分别滴定体积均为20.00mL、浓度均为
溶液分别滴定体积均为20.00mL、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
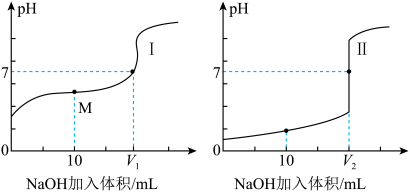
(1)滴定醋酸溶液的曲线是___________ 。(填“Ⅰ”或“Ⅱ”)。
(2)若采用氨水滴定醋酸,写出氨水与醋酸反应的离子反应方程式___________ 。
(3)滴定开始前,三种溶液中由水电离出的 最大的是
最大的是______ 。
A. 溶液 B.
溶液 B. 盐酸 C.
盐酸 C. 醋酸
醋酸
(4)该 溶液的pH为
溶液的pH为______ ;给该溶液加热,pH______ (填“变大”“变小”或“不变”)。
(5)在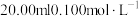 的盐酸中,滴加
的盐酸中,滴加 溶液后,此时溶液的pH=
溶液后,此时溶液的pH=___________ 。
(6)取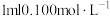 的盐酸稀释1000倍后,溶液pH=
的盐酸稀释1000倍后,溶液pH=___________ ,此时水电离出的 浓度为
浓度为___________ 。
(7)下列离子一定能大量共存的是___________。
(8)下列叙述正确的是___________。
(9)下列有关实验的说法,正确的是___________。
 溶液分别滴定体积均为20.00mL、浓度均为
溶液分别滴定体积均为20.00mL、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
的盐酸和醋酸溶液,得到滴定过程中溶液的pH随加入NaOH溶液体积而变化的两条滴定曲线。
(1)滴定醋酸溶液的曲线是
(2)若采用氨水滴定醋酸,写出氨水与醋酸反应的离子反应方程式
(3)滴定开始前,三种溶液中由水电离出的
 最大的是
最大的是A.
 溶液 B.
溶液 B. 盐酸 C.
盐酸 C. 醋酸
醋酸(4)该
 溶液的pH为
溶液的pH为(5)在
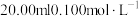 的盐酸中,滴加
的盐酸中,滴加 溶液后,此时溶液的pH=
溶液后,此时溶液的pH=(6)取
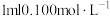 的盐酸稀释1000倍后,溶液pH=
的盐酸稀释1000倍后,溶液pH= 浓度为
浓度为(7)下列离子一定能大量共存的是___________。
A.甲基橙呈黄色的溶液中: 、 、 、 、 、 、 |
B.加入铝粉后产生大量氢气的溶液中: 、 、 、 、 、 、 |
C.石蕊呈蓝色的溶液中: 、 、 、 、 、 、 |
D.pH=1的溶液中: 、 、 、 、 、 、 |
(8)下列叙述正确的是___________。
A.无论是纯水,还是酸性、碱性或中性稀溶液,在常温下其 |
B.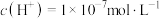 的溶液一定是中性溶液 的溶液一定是中性溶液 |
C.向水中加入少量固体 ,水的电离平衡逆向移动, ,水的电离平衡逆向移动, 减小 减小 |
D.将水加热, 增大,pH不变 增大,pH不变 |
(9)下列有关实验的说法,正确的是___________。
| A.测定HClO溶液pH时,用玻璃棒蘸取溶液,点在干燥pH试纸上 |
| B.等体积、等pH的硫酸与醋酸溶液分别与足量锌反应,醋酸产生的氢气多 |
| C.等体积、等浓度的盐酸和醋酸分别与相同大小的锌粒反应,醋酸初始反应速率快 |
| D.使用pH试纸测定溶液的pH时,若先润湿,则测得溶液的pH一定有误差 |
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】在Na+浓度为0.5mol·L-1的某澄清溶液中,还可能含有表中的若干种离子:
取该溶液100mL进行如下实验(气体体积在标准状况下测定):
试回答下列问题:
(1)实验I能确定一定不存在的阳离子是___________ 。
(2)通过实验I、II、III和计算,填写表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)
(3)判断K+是否存在______ (填“是”或“否”),若存在求其最小浓度,若不存在说明理由:_______ 。
| 阳离子 | K+、Ag+、Mg2+、Ba2+ |
| 阴离子 |  、 、 、 、 、 、 |
| 序号 | 实验内容 | 实验结果 |
| I | 向该溶液中加入足量稀HCl | 产生白色沉淀并放出0.56L气体 |
| II | 将I的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
| III | 在II的滤液中滴加BaCl2溶液 | 无明显现象 |
(1)实验I能确定一定不存在的阳离子是
(2)通过实验I、II、III和计算,填写表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)
| 阴离子 |  |  |  |  |
| c/(mol·L-1) |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】以含钒钢渣和钛白废酸为原料提取钒,实现“以废治废”。工艺流程如图:
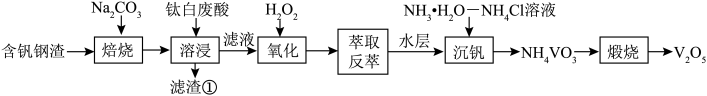
已知:含钒钢渣中主要含CaO、Fe2O3和少量SiO2、V2O3;钛白废酸中含H+、Fe2+、TiO2+、SO 等离子,回答下列问题。
等离子,回答下列问题。
(1)在空气中“焙烧”时,V2O3转化为NaVO3,写出反应的化学方程式:______ 。
(2)滤渣①主要成分是_____ 、______ 和H2TiO3。
(3)“溶浸”过程,有一部分VO 转化为VO2+,可能的原因是
转化为VO2+,可能的原因是______ 。
(4)“氧化”过程,VO2+被氧化成VO ,参与反应的VO2+与H2O2物质的量之比为
,参与反应的VO2+与H2O2物质的量之比为______ 。
(5)“萃取反萃”后溶液的pH不同,会造成钒的存在形态不同,有VO 、V2O
、V2O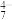 等,若升高溶液的pH,有利于
等,若升高溶液的pH,有利于______ (“VO ”或“V2O
”或“V2O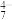 ”)的形成。
”)的形成。
(6)室温下,维持“沉钒”时溶液中NH3•H2O-NH4Cl的总浓度为cmol•L-1,pH=6。
①“沉钒”过程中,VO 转化为NH4VO3的离子方程式
转化为NH4VO3的离子方程式______ 。
②已知Kb(NH3•H2O)=a,Ksp(NH4VO3)=b,“沉钒”后溶液中c(VO )=
)=______ mol•L-1。(列计算式)
(7)NH4VO3经煅烧得到V2O5,其他产物可以返回______ 工艺,充分利用原料。

已知:含钒钢渣中主要含CaO、Fe2O3和少量SiO2、V2O3;钛白废酸中含H+、Fe2+、TiO2+、SO
 等离子,回答下列问题。
等离子,回答下列问题。(1)在空气中“焙烧”时,V2O3转化为NaVO3,写出反应的化学方程式:
(2)滤渣①主要成分是
(3)“溶浸”过程,有一部分VO
 转化为VO2+,可能的原因是
转化为VO2+,可能的原因是(4)“氧化”过程,VO2+被氧化成VO
 ,参与反应的VO2+与H2O2物质的量之比为
,参与反应的VO2+与H2O2物质的量之比为(5)“萃取反萃”后溶液的pH不同,会造成钒的存在形态不同,有VO
 、V2O
、V2O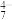 等,若升高溶液的pH,有利于
等,若升高溶液的pH,有利于 ”或“V2O
”或“V2O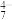 ”)的形成。
”)的形成。(6)室温下,维持“沉钒”时溶液中NH3•H2O-NH4Cl的总浓度为cmol•L-1,pH=6。
①“沉钒”过程中,VO
 转化为NH4VO3的离子方程式
转化为NH4VO3的离子方程式②已知Kb(NH3•H2O)=a,Ksp(NH4VO3)=b,“沉钒”后溶液中c(VO
 )=
)=(7)NH4VO3经煅烧得到V2O5,其他产物可以返回
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质。制备流程如图所示:
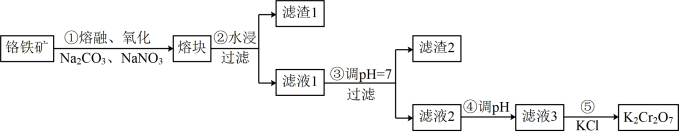
回答下列问题:
(1)步骤①的主要反应为:FeO·Cr2O3+Na2CO3+NaNO3 Na2CrO4+ Fe2O3+CO2+ NaNO2,上述反应配平后FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+ Fe2O3+CO2+ NaNO2,上述反应配平后FeO·Cr2O3与NaNO3的系数比为__________ 。该步骤不能使用陶瓷容器,原因是_________ 。
(2)滤渣1中含量最多的金属元素是_______ ,滤渣2的主要成分是__________ 及含硅杂质。
(3)步骤④调滤液2的pH使之变______ (填“大”或“小”),原因是___________________ (用离子方程式表示)。
(4)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体。冷却到___________ (填标号)得到的K2Cr2O7固体产品最多。
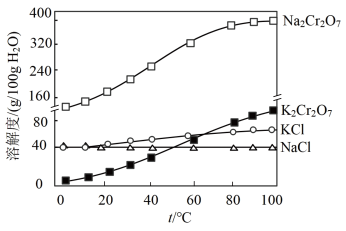
a.80℃ b.60℃ c.40℃ d.10℃
步骤⑤的反应类型是___________________ 。

回答下列问题:
(1)步骤①的主要反应为:FeO·Cr2O3+Na2CO3+NaNO3
 Na2CrO4+ Fe2O3+CO2+ NaNO2,上述反应配平后FeO·Cr2O3与NaNO3的系数比为
Na2CrO4+ Fe2O3+CO2+ NaNO2,上述反应配平后FeO·Cr2O3与NaNO3的系数比为(2)滤渣1中含量最多的金属元素是
(3)步骤④调滤液2的pH使之变
(4)有关物质的溶解度如图所示。向“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到K2Cr2O7固体。冷却到

a.80℃ b.60℃ c.40℃ d.10℃
步骤⑤的反应类型是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】现有一混合液,可能含有以下离子中的若干种: 、
、 、
、 、
、 、
、 、
、 、
、 ,现取三份100mL该混合溶液进行如下实验。
,现取三份100mL该混合溶液进行如下实验。
实验①:向第一份混合溶液中加入 溶液,有沉淀产生;
溶液,有沉淀产生;
实验②:向第二份混合溶液中滴加1.00mol/L的NaOH溶液,溶液中沉淀的质量与氢氧化钠的体积关系如图所示:

实验③:向第三份混合溶液中加入足量 溶液后,得到干燥的沉淀9.32g。
溶液后,得到干燥的沉淀9.32g。
(1)由实验①推断该混合溶液_______ (填“一定”或“不一定”)含有 。
。
(2)实验②中沉淀质量减少的离子方程式_______ 。
(3)实验③生成沉淀的物质的量是_______ mol。
(4)综合上述实验,你认为以下结论正确的是_______(填标号)。
(5)该实验中共需要240mLNaOH溶液,某化学实验小组欲用固体准确配制该浓度的溶液
①如图所示的仪器中配制溶液无需使用的是_______ (填字母),还缺少的玻璃仪器是_______ 。
A.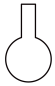 B.
B.  C.
C. 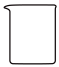 D.
D.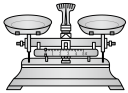 E.
E.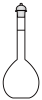 F.
F.
②若实验遇下列情况,导致所配溶液的物质的量浓度偏高的是_______ (填字母)。
A.定容时仰视刻度线 B.定容时水加多了用胶头滴管吸出
C.移液前,容量瓶内有蒸馏水 D.未冷却至室温就转移定容
 、
、 、
、 、
、 、
、 、
、 、
、 ,现取三份100mL该混合溶液进行如下实验。
,现取三份100mL该混合溶液进行如下实验。实验①:向第一份混合溶液中加入
 溶液,有沉淀产生;
溶液,有沉淀产生;实验②:向第二份混合溶液中滴加1.00mol/L的NaOH溶液,溶液中沉淀的质量与氢氧化钠的体积关系如图所示:

实验③:向第三份混合溶液中加入足量
 溶液后,得到干燥的沉淀9.32g。
溶液后,得到干燥的沉淀9.32g。(1)由实验①推断该混合溶液
 。
。(2)实验②中沉淀质量减少的离子方程式
(3)实验③生成沉淀的物质的量是
(4)综合上述实验,你认为以下结论正确的是_______(填标号)。
A.该混合溶液中一定含有 、 、 、 、 、 、 、 、 ,可能含 ,可能含 |
B.该混合溶液中一定含有 、 、 、 、 、 、 、 、 |
C.该混合溶液中一定含有 、 、 、 、 、 、 ,可能含 ,可能含 、 、 |
D.若要确定该混合溶液中是否含有 ,还需进行焰色反应来进行检验 ,还需进行焰色反应来进行检验 |
(5)该实验中共需要240mLNaOH溶液,某化学实验小组欲用固体准确配制该浓度的溶液
①如图所示的仪器中配制溶液无需使用的是
A.
 B.
B.  C.
C.  D.
D. E.
E. F.
F.
②若实验遇下列情况,导致所配溶液的物质的量浓度偏高的是
A.定容时仰视刻度线 B.定容时水加多了用胶头滴管吸出
C.移液前,容量瓶内有蒸馏水 D.未冷却至室温就转移定容
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】无水AlCl3易升华,可用作有机合成的催化剂等。工业上以铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
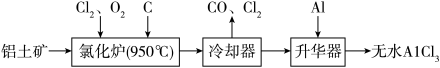
提示:2Fe(OH)3 Fe2O3+ 3H2O
Fe2O3+ 3H2O
(1)铝在空气中有强的抗腐蚀性,原因是___________________ 。
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式为________________________ 。
(3)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,反应完后溶液呈碱性,此反应的离子方程式为_____________________ 。
(4)为测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液中,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,得其质量为0.32 g。
①写出上述除杂过程中涉及的离子方程式:________________ 、________________ 。
②产品中AlCl3的质量分数为(只列出计算式,不计算结果)____________ 。

提示:2Fe(OH)3
 Fe2O3+ 3H2O
Fe2O3+ 3H2O(1)铝在空气中有强的抗腐蚀性,原因是
(2)氯化炉中Al2O3、Cl2和C反应的化学方程式为
(3)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,反应完后溶液呈碱性,此反应的离子方程式为
(4)为测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液中,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,得其质量为0.32 g。
①写出上述除杂过程中涉及的离子方程式:
②产品中AlCl3的质量分数为(只列出计算式,不计算结果)
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】铬系和非铬系铜镍电镀污泥均含有Cu(Ⅱ)、Ni(Ⅱ)、Fe(Ⅱ)、Al(Ⅲ)的氢氧化物,前者还含有Cr(Ⅲ)的氢氧化物,一种综合回收铜、镍的新工艺流程如下:
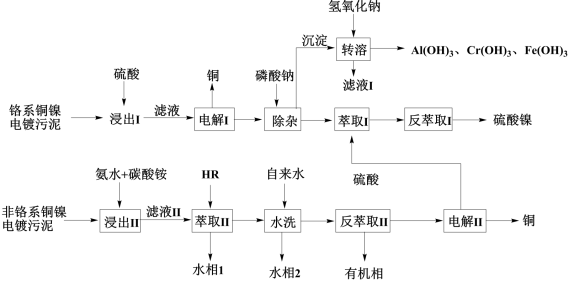
已知:
Ⅰ、FePO4、CrPO4、AlPO4、Ni3(PO4)2的Ksp依次为1.3×10−22、2.4×10−23、5.8×10−19、5.0×10−31。
Ⅱ.Cr及其化合物的性质与铝类似。
回答下列问题:
(1)“电解Ⅰ”时,需严格控制电压,除了回收铜之外,第二个目的是___________ ,可通过一种试剂证明第二个目的是否达成,该试剂为___________ (填化学式)。
(2)“除杂”时,若镍离子浓度为0.05mol·L−1,则应调整溶液中PO 浓度范围为
浓度范围为________ mol·L−1 (溶液中离子浓度≤10-5mol·L−1时,认为该离子沉淀完全;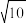 =3.2)。
=3.2)。
(3)“转溶”时,氢氧化钠加入量不宜过多,其原因为___________ (用离子方程式表示)。
(4)“浸出Ⅱ”时,采取了多次浸取的方式,其目的为___________ 。
(5)“萃取Ⅱ”时,发生的反应为Cu(NH3)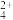 +2HR=CuR2+2NH
+2HR=CuR2+2NH +2NH3和Ni(NH3)
+2NH3和Ni(NH3) +2HR=NiR2+2NH
+2HR=NiR2+2NH +4NH3和,则“反萃取Ⅱ”时含铜微粒发生反应的离子方程式为
+4NH3和,则“反萃取Ⅱ”时含铜微粒发生反应的离子方程式为___________ 。
(6)“电解Ⅱ”时,若维持电流强度为0.5A,电流效率为90%,电解8min,理论上可获得铜___________ g.(已知:电流效率是指电解时电极上实际沉积与理论沉积物质的量之比,F=96500C·mol-1)
(7)流程中除了有机相之外,可以循环利用的物质还有___________ (填化学式)。

已知:
Ⅰ、FePO4、CrPO4、AlPO4、Ni3(PO4)2的Ksp依次为1.3×10−22、2.4×10−23、5.8×10−19、5.0×10−31。
Ⅱ.Cr及其化合物的性质与铝类似。
回答下列问题:
(1)“电解Ⅰ”时,需严格控制电压,除了回收铜之外,第二个目的是
(2)“除杂”时,若镍离子浓度为0.05mol·L−1,则应调整溶液中PO
 浓度范围为
浓度范围为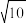 =3.2)。
=3.2)。(3)“转溶”时,氢氧化钠加入量不宜过多,其原因为
(4)“浸出Ⅱ”时,采取了多次浸取的方式,其目的为
(5)“萃取Ⅱ”时,发生的反应为Cu(NH3)
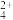 +2HR=CuR2+2NH
+2HR=CuR2+2NH +2NH3和Ni(NH3)
+2NH3和Ni(NH3) +2HR=NiR2+2NH
+2HR=NiR2+2NH +4NH3和,则“反萃取Ⅱ”时含铜微粒发生反应的离子方程式为
+4NH3和,则“反萃取Ⅱ”时含铜微粒发生反应的离子方程式为(6)“电解Ⅱ”时,若维持电流强度为0.5A,电流效率为90%,电解8min,理论上可获得铜
(7)流程中除了有机相之外,可以循环利用的物质还有
您最近一年使用:0次



