名校
解题方法
1 . 框图中甲、乙为单质,其余均为化合物,B为常见液态化合物,A为淡黄色固体,F、G所含元素相同且均为氯化物,G遇KSCN溶液显红色。
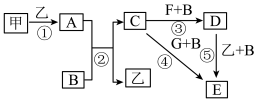
请问答下列问题:
(1)反应①-⑤中,既属于氧化还原反应又属于化合反应的是___________ (填序号)。
(2)反应⑤的化学方程式为___________ 。
(3)在实验室将C溶液滴入F溶液中,观察到的现象是___________ 。
(4)在F溶液中加入等物质的量的A,发生反应的总的离子方程式为:___________ 。
(5)已知:酚酞在c(OH-)为1.0×10-4mol/L~2.5mol/L时呈红色,且半分钟内不褪色。向3.9g A和50g B混合后的溶液中滴入2滴酚酞试液,溶液变红色,片刻红色褪去(假设过程中液体体积不变)。
①甲同学认为“红色迅速褪去”是由于溶液中c(OH-)过大造成的,上述观点是否正确______ 。
②乙同学认为“红色迅速褪去”是由于A + B = 碱 + H2O2 ,H2O2具有氧化性和漂白性导致的,设计实验证明烧瓶内溶液中含H2O2,简述实验方法___________ 。

请问答下列问题:
(1)反应①-⑤中,既属于氧化还原反应又属于化合反应的是
(2)反应⑤的化学方程式为
(3)在实验室将C溶液滴入F溶液中,观察到的现象是
(4)在F溶液中加入等物质的量的A,发生反应的总的离子方程式为:
(5)已知:酚酞在c(OH-)为1.0×10-4mol/L~2.5mol/L时呈红色,且半分钟内不褪色。向3.9g A和50g B混合后的溶液中滴入2滴酚酞试液,溶液变红色,片刻红色褪去(假设过程中液体体积不变)。
①甲同学认为“红色迅速褪去”是由于溶液中c(OH-)过大造成的,上述观点是否正确
②乙同学认为“红色迅速褪去”是由于A + B = 碱 + H2O2 ,H2O2具有氧化性和漂白性导致的,设计实验证明烧瓶内溶液中含H2O2,简述实验方法
您最近一年使用:0次
2 . A、B、C、D几种纯净物至少含一种共同的元素,它们之间有如下转化关系(部分条件和产物省略)。

回答下列问题:
(1)若A为金属单质,C为浅黄色粉末,Y为液态氧化物(常温常压),则B的化学式为___________ 。C→D的离子方程式为___________ 。
(2)若A是酸性氧化物,向空气中大量排放A,会加剧温室效应的形成,强碱X的焰色呈黄色,则B的化学式为___________ ,X的电离方程式为___________ 。
(3)若A是非金属单质,C是光合作用的原料,A和C在高温下生成B,该反应中氧化产物、还原产物的质量之比为___________ 。
(4)若A为黄绿色气体,X为金属单质,B为X在A中燃烧生成的棕褐色烟,为探究C中阳离子具有还原性,设计如下方案:
取适量的C固体溶于水,将溶液分成甲、乙、丙三份,进行如下实验:
①能证明C中阳离子具有还原性的实验是___________ (填代号)。
②丙实验中溶液由无色变红色的原因是___________ (用离子方程式表示)。

回答下列问题:
(1)若A为金属单质,C为浅黄色粉末,Y为液态氧化物(常温常压),则B的化学式为
(2)若A是酸性氧化物,向空气中大量排放A,会加剧温室效应的形成,强碱X的焰色呈黄色,则B的化学式为
(3)若A是非金属单质,C是光合作用的原料,A和C在高温下生成B,该反应中氧化产物、还原产物的质量之比为
(4)若A为黄绿色气体,X为金属单质,B为X在A中燃烧生成的棕褐色烟,为探究C中阳离子具有还原性,设计如下方案:
取适量的C固体溶于水,将溶液分成甲、乙、丙三份,进行如下实验:
| 实验 | 操作 | 现象 |
| 甲 | 加入镁粉 | 溶液颜色逐渐变为无色 |
| 乙 | 依次滴加KSCN溶液、新制氯水 | 开始不变色,后变红色 |
| 丙 | 先滴加KSCN溶液,后滴加酸化的双氧水 | 开始不变色,后变红色 |
②丙实验中溶液由无色变红色的原因是
您最近一年使用:0次
3 . 已知A、B、C、D、E、F、G、H可以发生如图所示的转化关系,反应中部分生成物已略去。其中,A、G为同一主族元素形成的单质,B、C、H在通常情况下为气体,E是水晶的主要成分,化合物C是一种形成酸雨的大气污染物。
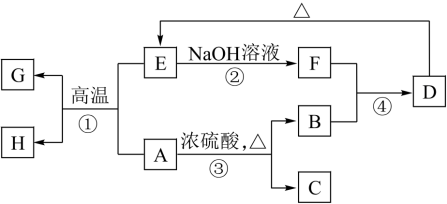
(1)C的化学式___________ ,F的名称___________ 。
(2)反应①的化学方程式是___________ 。反应②的离子方程式是___________ 。
(3)写出G的一种用途是___________ ,其与氢氧化钠溶液反应的化学方程式为___________ 。
(4)反应③的化学方程式是___________ 。
(5)下列溶液中能用来区分B和C气体的是___________ (填序号)。
①澄清石灰水 ②H2S溶液 ③酸性KMnO4溶液 ④氯水 ⑤品红溶液 ⑥紫色石蕊溶液
(6) 的酸性
的酸性___________  的酸性(填“强于”或“弱于”),请用离子方程式予以证明:
的酸性(填“强于”或“弱于”),请用离子方程式予以证明:___________ 。

(1)C的化学式
(2)反应①的化学方程式是
(3)写出G的一种用途是
(4)反应③的化学方程式是
(5)下列溶液中能用来区分B和C气体的是
①澄清石灰水 ②H2S溶液 ③酸性KMnO4溶液 ④氯水 ⑤品红溶液 ⑥紫色石蕊溶液
(6)
 的酸性
的酸性 的酸性(填“强于”或“弱于”),请用离子方程式予以证明:
的酸性(填“强于”或“弱于”),请用离子方程式予以证明:
您最近一年使用:0次
2023-05-10更新
|
337次组卷
|
2卷引用:江西省全南中学2022-2023学年高一下学期教学质量验收化学试题
名校
解题方法
4 . I.A经如图所示的过程可转化为D。已知D为强酸或强碱,请回答下列问题。
A B
B C
C D
D
(1)若常温下C是红棕色的气体,A是碱性气体。则:
①A的化学式是_____ ,C→D的过程中,氧化剂和还原剂的质量之比为_____ 。
②D的稀溶液在常温下可与Cu反应,请写出该反应的离子方程式_____ 。
(2)若A为金属单质,C为淡黄色固体,则C→D的化学反应方程式_____ 。
II.可利用如图装置来证明酸性:H2CO3>H2SiO3。

(3)方法是:在A中加入的试剂是_____ (填编号,下同),B中加入的试剂是_____ ,C中加入的试剂是_____ ;如果在C中看到白色沉淀生成,即可证明酸性:H2CO3>H2SiO3。
供选择的试剂:①稀盐酸 ②稀硫酸 ③碳酸钙 ④Na2SiO3溶液 ⑤碳酸钠
A
 B
B C
C D
D(1)若常温下C是红棕色的气体,A是碱性气体。则:
①A的化学式是
②D的稀溶液在常温下可与Cu反应,请写出该反应的离子方程式
(2)若A为金属单质,C为淡黄色固体,则C→D的化学反应方程式
II.可利用如图装置来证明酸性:H2CO3>H2SiO3。

(3)方法是:在A中加入的试剂是
供选择的试剂:①稀盐酸 ②稀硫酸 ③碳酸钙 ④Na2SiO3溶液 ⑤碳酸钠
您最近一年使用:0次
5 . A、B、C、D、E五种物质中均含有同一种非金属元素,它们能发生如图所示的转化关系。若该元素用R表示,则A为R的氧化物,D为R的单质,且D与NaOH溶液反应生成C和H2。
(1)写出对应物质的化学式:A_______ ;C_______ ;E________ 。
(2)反应①的化学方程式为__________ 。
(3)反应④的离子方程式为__________ 。
(4)H2CO3的酸性强于E的酸性,请用离子方程式予以证明:________ 。
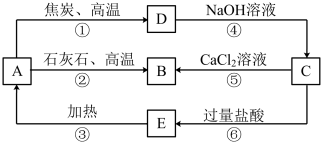
(1)写出对应物质的化学式:A
(2)反应①的化学方程式为
(3)反应④的离子方程式为
(4)H2CO3的酸性强于E的酸性,请用离子方程式予以证明:
您最近一年使用:0次
2020-09-24更新
|
635次组卷
|
8卷引用:江西省贵溪市实验中学2020-2021学年高一上学期期末考试化学(A)试题
解题方法
6 . 下图中,A、C是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,H、G是正四面体结构的非极性分子,H是一种重要的能源,J是一种耐高温材料,K是由两种常见元素组成的化合物(图中部分反应物或生成物没有列出)。
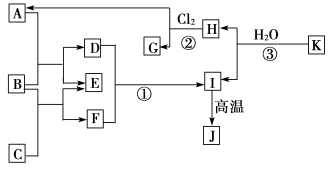
请按要求回答下列问题:
⑴写出B元素在周期表中的位置__________ K的化学式________________ 。
⑵反应①的离子方程式为______________________ 。
⑶将D的溶液蒸干且将所得的固体物质灼烧得到___________ 固体(写化学式),若要由D得溶液得到无水的D的固体,请简述其处理方法______________
⑷反应②进行的条件通常是___________ ,H和Cl2反应产物中有一种产物M的结构能证明G一定为正四面体结构请写出M的电子式________________ 。
⑸J与焦炭在高温的情况下可以生成K和二氧化碳,请写出该反应的方程式__________________ ;在此反应中氧化剂与还原剂的质量之比为____________

请按要求回答下列问题:
⑴写出B元素在周期表中的位置
⑵反应①的离子方程式为
⑶将D的溶液蒸干且将所得的固体物质灼烧得到
⑷反应②进行的条件通常是
⑸J与焦炭在高温的情况下可以生成K和二氧化碳,请写出该反应的方程式
您最近一年使用:0次
9-10高三下·西藏拉萨·阶段练习
解题方法
7 . U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
⑴.V的单质分子的结构式为_______________ ;XW的电子式为____________ ;U元素在周期表中的位置是_____________ 。
⑵.U元素形成的同素异形体的晶体类型可能是(填序号)__________ 。
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
⑶.U、V、W形成的10电子氢化物中,U、V、W的氢化物沸点最高的是(写化学式)____________ ;V、W的氢化物分子结合H+能力较强的是(写化学式)______________ ,用一个离子方程式加以证明___________________________________________ 。
请回答下列问题:
⑴.V的单质分子的结构式为
⑵.U元素形成的同素异形体的晶体类型可能是(填序号)
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
⑶.U、V、W形成的10电子氢化物中,U、V、W的氢化物沸点最高的是(写化学式)
您最近一年使用:0次
解题方法
8 . 下图为氮、硫及其部分化合物的价类二维图,有关说法正确的是
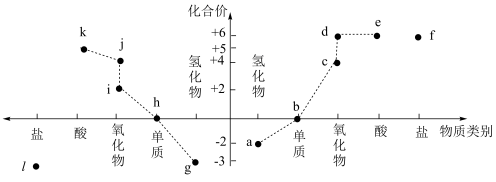
| A.g与e反应产物可以属于f或l | B.e的浓溶液不能干燥a、c、g、i |
| C.将k转化为j必须选用合适还原剂才能实现 | D.除f和l外,上述物质中是电解质的还有2种 |
您最近一年使用:0次
9 . 某元素常见物质的“价类”二维图,其中d为红棕色气体,f和g均为正盐且焰色反应(试验)火焰为黄色。下列说法错误的是

| A.常温下,e的浓溶液可以用铝槽车运输 |
| B.气体a、c均可用浓硫酸干燥 |
C.1 mol d与足量水反应转移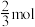 电子 电子 |
| D.d可与NaOH溶液反应生成f和g |
您最近一年使用:0次
2022-10-06更新
|
305次组卷
|
6卷引用:江西省宜春市丰城市东煌学校2022-2023学年高三上学期期中考试化学试卷
江西省宜春市丰城市东煌学校2022-2023学年高三上学期期中考试化学试卷江西省宜春市丰城市第九中学2023-2024学年高一下学期第一次月考化学试题山西省2022-2023学年高三上学期9月质量检测化学试题湖南省邵阳市部分校2022-2023学年高三上学期第一次联考化学试题河南省部分重点中学环际大联考圆梦计划2022-2023学年高三上学期期中考试化学试题(已下线)查补易混易错01 元素化合物部分-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)
名校
10 . 钴是一种重要的过渡金属元素,实验室利用 固体进行如下实验。下列说法错误的是
固体进行如下实验。下列说法错误的是

 固体进行如下实验。下列说法错误的是
固体进行如下实验。下列说法错误的是
A.固体 为 为 ,气体 ,气体 为 为 | B.上述所涉及的反应均为氧化还原反应 |
C.酸性条件下还原性: | D.溶解过程中理论可得 |
您最近一年使用:0次
2023-09-07更新
|
186次组卷
|
3卷引用:江西省百师联盟2024届高三上学期一轮复习联考化学试题



