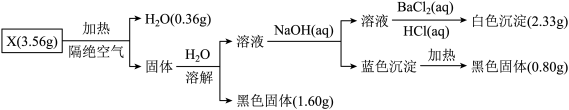
下图中,A、C是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,H、G是正四面体结构的非极性分子,H是一种重要的能源,J是一种耐高温材料,K是由两种常见元素组成的化合物(图中部分反应物或生成物没有列出)。
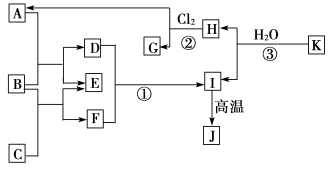
请按要求回答下列问题:
⑴写出B元素在周期表中的位置__________ K的化学式________________ 。
⑵反应①的离子方程式为______________________ 。
⑶将D的溶液蒸干且将所得的固体物质灼烧得到___________ 固体(写化学式),若要由D得溶液得到无水的D的固体,请简述其处理方法______________
⑷反应②进行的条件通常是___________ ,H和Cl2反应产物中有一种产物M的结构能证明G一定为正四面体结构请写出M的电子式________________ 。
⑸J与焦炭在高温的情况下可以生成K和二氧化碳,请写出该反应的方程式__________________ ;在此反应中氧化剂与还原剂的质量之比为____________

请按要求回答下列问题:
⑴写出B元素在周期表中的位置
⑵反应①的离子方程式为
⑶将D的溶液蒸干且将所得的固体物质灼烧得到
⑷反应②进行的条件通常是
⑸J与焦炭在高温的情况下可以生成K和二氧化碳,请写出该反应的方程式
更新时间:2016/12/09 16:54:02
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】下图是一些中学常见的物质之间的转化关系(其中部分反应产物省略),其中A和B常温下都是气体,且水溶液都有漂白性;I是一种金属单质;F、M、N均为白色沉淀,其中M和N不溶于稀硝酸,C和D是两种常见的强酸。请回答下列问题:
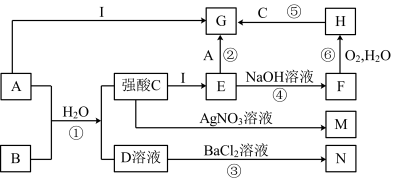
(1)写出①的化学方程式___________ 。
(2)在①→⑥中,属于氧化还原反应的有___________ (填编号)。
(3)将NaOH溶液加入到E中的现象为___________ 。
(4)写出反应⑥的化学反应方程式___________ 。

(1)写出①的化学方程式
(2)在①→⑥中,属于氧化还原反应的有
(3)将NaOH溶液加入到E中的现象为
(4)写出反应⑥的化学反应方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】下列关系图中,X 是一种正盐,E 是强酸,当 Y 无论是强酸或强碱都有如下反应关系:友情提示:当 Y 无论是强酸或强碱,X、A、B、C、D、E 均为同种元素对应的不同的化合物或单质。
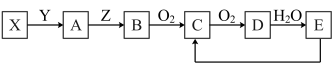
回答下列问题:
(1)X 是_____
(2)当 Y 是稀盐酸溶液时,B 为黄色固体单质
①由 C 生成 D 的化学方程式为:________________
②一定质量的 Zn 与 100mL 12.0mol/L 的 E 的浓溶液充分反应,反应后称量剩余的过量的锌发现质量减少了 65.0g。则产生的 SO2 和 H2 的体积分别为(标况下)________
(3)当 Y 是浓氢氧化钠溶液时,B 为空气中含量最高的气态单质
①C、D 都是大气污染物,它们对环境造成的危害表现在_____
A.引起酸雨 B.引起温室效应
C.形成光化学烟雾 D.造成臭氧层的破坏
②1.92g 铜投入一定的 E 浓溶液中,铜完全溶解,共收集到 672mL 气体(标准状况)。将盛有此气体的容器倒扣在水中,通入标准状况下一定体积的 O2,恰好使气体完全溶于水中,则通入 O2的体积为________ mL
③铜和铁的混合物 4.8g,溶解在过量的某浓度的 E 溶液中,完全反应后得到标准状况下2 .24LNO 气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是_______

回答下列问题:
(1)X 是
(2)当 Y 是稀盐酸溶液时,B 为黄色固体单质
①由 C 生成 D 的化学方程式为:
②一定质量的 Zn 与 100mL 12.0mol/L 的 E 的浓溶液充分反应,反应后称量剩余的过量的锌发现质量减少了 65.0g。则产生的 SO2 和 H2 的体积分别为(标况下)
(3)当 Y 是浓氢氧化钠溶液时,B 为空气中含量最高的气态单质
①C、D 都是大气污染物,它们对环境造成的危害表现在
A.引起酸雨 B.引起温室效应
C.形成光化学烟雾 D.造成臭氧层的破坏
②1.92g 铜投入一定的 E 浓溶液中,铜完全溶解,共收集到 672mL 气体(标准状况)。将盛有此气体的容器倒扣在水中,通入标准状况下一定体积的 O2,恰好使气体完全溶于水中,则通入 O2的体积为
③铜和铁的混合物 4.8g,溶解在过量的某浓度的 E 溶液中,完全反应后得到标准状况下2 .24LNO 气体。若向反应后的溶液中加入足量的烧碱,则可生成沉淀的质量是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐1】中学常见物质A~L的转化关系如下图:(无关产物已略去)

①A、B、H均为单质,A、B有金属光泽,A可以在常温下溶于L的浓溶液,H为黄色固体,向由A、B粉未组成的均匀混合物中加入无色纯液体C(少量)后,产生大量紫色蒸气。
②D、E、F、I、L都是无色溶液,G是无色气体。
③K是一种白色沉淀,J是一种黄色沉淀,将G通入E后可以产生一种黑色沉淀和L。
(1)写出下列物质的名称:B________ H_________
(2)写出试题中出现的几种沉淀的化学式:黄色沉淀_______ ;黑色沉淀_________ 。
(3)写出B和G反应的离子方程式__________________________ 。
(4)写出电解E溶液的电极反应式: 阳极:_______________ ;阴极:________________ 。

①A、B、H均为单质,A、B有金属光泽,A可以在常温下溶于L的浓溶液,H为黄色固体,向由A、B粉未组成的均匀混合物中加入无色纯液体C(少量)后,产生大量紫色蒸气。
②D、E、F、I、L都是无色溶液,G是无色气体。
③K是一种白色沉淀,J是一种黄色沉淀,将G通入E后可以产生一种黑色沉淀和L。
(1)写出下列物质的名称:B
(2)写出试题中出现的几种沉淀的化学式:黄色沉淀
(3)写出B和G反应的离子方程式
(4)写出电解E溶液的电极反应式: 阳极:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期。A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍。同时含有A、B、D三种元素的化合物M是一种居室污染气体,其分子中所有的原子共平面。A、B两种元素组成的原子个数比为1︰1的化合物N是常见的有机溶剂。E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同。
请回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)下列叙述正确的是___________ (填字母)。
a.M易溶于水,是因为M与水分子间能形成氢键,且M是极性分子;N不溶于水,是因为N是非极性分子
b.M和二氧化碳分子中的中心原子均采用sp2杂化
c.N分子中含有6个σ键和3个π键
d.BD2晶体的熔沸点都比二氧化硅晶体的低
(2)金属E的晶胞是面心立方结构(如图),则E晶体的1个晶胞中E原子数为:______ ,E原子的配位数为:_______ 。

(3)E的一种氧化物化学式为EO2,广泛用于制造高级白色油漆,也是许多反应的催化剂。工业上用含E的矿石[主要成分为FeEO3(不溶于水) ]作原料制取EO2。矿石经过硫酸溶液浸泡,生成含EO2+的溶液,再经稀释得EO2·xH2O,写出这两步反应的离子方程式__________________________ ,___________________ 。
(4)X和Y分别是B和C的氢化物,这两种氢化物都含有18电子。X和Y的化学式分别是______ 、______ 。两者沸点的关系为X___ Y(>,或<),原因是_____________________________________________________ 。
请回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)下列叙述正确的是
a.M易溶于水,是因为M与水分子间能形成氢键,且M是极性分子;N不溶于水,是因为N是非极性分子
b.M和二氧化碳分子中的中心原子均采用sp2杂化
c.N分子中含有6个σ键和3个π键
d.BD2晶体的熔沸点都比二氧化硅晶体的低
(2)金属E的晶胞是面心立方结构(如图),则E晶体的1个晶胞中E原子数为:

(3)E的一种氧化物化学式为EO2,广泛用于制造高级白色油漆,也是许多反应的催化剂。工业上用含E的矿石[主要成分为FeEO3(不溶于水) ]作原料制取EO2。矿石经过硫酸溶液浸泡,生成含EO2+的溶液,再经稀释得EO2·xH2O,写出这两步反应的离子方程式
(4)X和Y分别是B和C的氢化物,这两种氢化物都含有18电子。X和Y的化学式分别是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】W、X、Y、Z均为短周期元素,X、W可形成两种液态化合物甲和乙,其原子个数比分别为1∶1(甲)和2∶1(乙),且分子中电子总数分别为18(甲)和10(乙)。X与Z能形成一种极易溶于水的碱性气体丙X与Y能形成极易溶于水的酸性气体丁,丁分子中的电子数为18。X、Y、Z能形成一种离子化合物,其水溶液呈弱酸性。请写出:
(1)W的元素符号___ ,其核外共有___ 种运动状态不同的电子。
(2)甲物质的结构式为___ ;乙物质的空间构型为___ 。
(3)Z元素核外共有___ 种能量不同的电子,碱性气体甲的电子式为___ 。
(4)用离子方程式解释X、Y、Z形成的化合物水溶液呈弱酸性的原因是___ 。
(5)铋元素跟Y元素能形成化合物(BiY3),其水解生成难溶于水的BiOY。
①BiY3水解反应的化学方程式为___ 。
②把适量的BiY3溶于含有少量丁的水中,能得到澄清溶液,试分析可能的原因___ 。
③医药上把BiOY叫做“次某酸铋”,分析这种叫法的不合理之处,为什么。___ 。
(1)W的元素符号
(2)甲物质的结构式为
(3)Z元素核外共有
(4)用离子方程式解释X、Y、Z形成的化合物水溶液呈弱酸性的原因是
(5)铋元素跟Y元素能形成化合物(BiY3),其水解生成难溶于水的BiOY。
①BiY3水解反应的化学方程式为
②把适量的BiY3溶于含有少量丁的水中,能得到澄清溶液,试分析可能的原因
③医药上把BiOY叫做“次某酸铋”,分析这种叫法的不合理之处,为什么。
您最近一年使用:0次