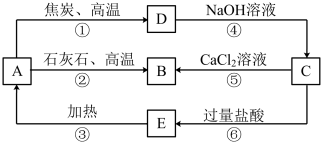
A、B、C、D、E五种物质中均含有同一种非金属元素,它们能发生如图所示的转化关系。若该元素用R表示,则A为R的氧化物,D为R的单质,且D与NaOH溶液反应生成C和H2。
(1)写出对应物质的化学式:A_______ ;C_______ ;E________ 。
(2)反应①的化学方程式为__________ 。
(3)反应④的离子方程式为__________ 。
(4)H2CO3的酸性强于E的酸性,请用离子方程式予以证明:________ 。
(1)写出对应物质的化学式:A
(2)反应①的化学方程式为
(3)反应④的离子方程式为
(4)H2CO3的酸性强于E的酸性,请用离子方程式予以证明:
16-17高一上·广东肇庆·期末 查看更多[8]
更新时间:2020-09-24 11:11:23
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D四种物质之间有下图所示的转化关系。
已知:A是气体单质,C 是红棕色气体。

回答下列问题:
(1)写出C的化学式:________ ;
(2)在上图D→B的过程中,D表现出强_____ (填“氧化性”或“还原性”);
(3)写出C→D转化的化学方程式__________________________________
(4)D→B的离子方程式_____________________________________________
(5)C 是红棕色气体,若A是气态氢化物,则A的电子式为___________
已知:A是气体单质,C 是红棕色气体。

回答下列问题:
(1)写出C的化学式:
(2)在上图D→B的过程中,D表现出强
(3)写出C→D转化的化学方程式
(4)D→B的离子方程式
(5)C 是红棕色气体,若A是气态氢化物,则A的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D四种元素是元素周期表中前20号元素,其原子序数依次增大,A是元素周期表中原子半径最小的元素,B的最外层电子数是次外层电子数的3倍,A的单质在C的单质中燃烧,发出苍白色火焰,D的原子核外N层电子数是K层电子数的一半。(第1题每空1分,其余每空2分,共16分)
(1)A为____ ;B为_____ ;C为______ ;D为________ ;(填元素符号)
(2)C离子的离子结构示意图为___________________
(3)A单质的结构式__________________________
(4) C在元素周期表中第________ 周期,___________ 族。
(5)写出D与水反应的化学方程式:_________________________________ ,所得溶液的pH__________ 7。
(1)A为
(2)C离子的离子结构示意图为
(3)A单质的结构式
(4) C在元素周期表中第
(5)写出D与水反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下图是中学常见物质间的转化关系。已知:
a.A为淡黄色固体,B为导致“温室效应”的主要物质;
b.E为常见金属,J为红褐色沉淀;
c.G在实验室中常用于检验B的存在;
d.L是一种重要的工业原料,常用于制造炸药,浓溶液常呈黄色。
回答下列问题:

(1)A的电子式____________ 。
(2)反应①的化学方程式为___________ ,反应②的离子方程式为______________ ,
(3)若参加反应的A的质量为39g,则消耗CO2的体积(标况下)为__________ L。
a.A为淡黄色固体,B为导致“温室效应”的主要物质;
b.E为常见金属,J为红褐色沉淀;
c.G在实验室中常用于检验B的存在;
d.L是一种重要的工业原料,常用于制造炸药,浓溶液常呈黄色。
回答下列问题:

(1)A的电子式
(2)反应①的化学方程式为
(3)若参加反应的A的质量为39g,则消耗CO2的体积(标况下)为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】以废旧催化剂(主要成分为 、
、 ,还含有少量的
,还含有少量的 、
、 )为主要原料制备
)为主要原料制备 、
、 的工艺流程如图所示:
的工艺流程如图所示:
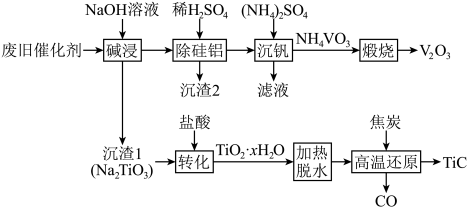
回答下列问题:
(1)“碱浸”后溶液中含钒元素的溶质是_______ (填化学式),实验室中将“沉渣1”从“碱浸”所得的悬浊液中分离出来所需玻璃仪器的名称为_______ 。
(2)“沉渣2”中含有两种成分,它们的化学式为_______ 。
(3)“转化”时发生反应的化学方程式为_______ 。
(4)“煅烧”时生成一种刺激性气味的气体,检验该气体常使用的试纸为_______ 。
(5)“高温还原”时 发生反应的化学方程式为
发生反应的化学方程式为_______ ,若生成30g还原产物,则转移电子的物质的量为_______ 。
 、
、 ,还含有少量的
,还含有少量的 、
、 )为主要原料制备
)为主要原料制备 、
、 的工艺流程如图所示:
的工艺流程如图所示:
回答下列问题:
(1)“碱浸”后溶液中含钒元素的溶质是
(2)“沉渣2”中含有两种成分,它们的化学式为
(3)“转化”时发生反应的化学方程式为
(4)“煅烧”时生成一种刺激性气味的气体,检验该气体常使用的试纸为
(5)“高温还原”时
 发生反应的化学方程式为
发生反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示物质的转化关系中,A是一种固体单质,E是一种白色沉淀.请回答下列问题:
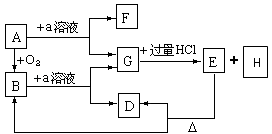
(1)B的化学式是___ , 目前B已被用作___ 的主要原料.
(2)B和a溶液反应的离子方程式是___ .
(3)A和a溶液反应的离子方程式是___ .
(4)C和过量的盐酸反应的离子方程式是___ .

(1)B的化学式是
(2)B和a溶液反应的离子方程式是
(3)A和a溶液反应的离子方程式是
(4)C和过量的盐酸反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】高纯硅是现代信息。半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:_______ 。
(2)还原炉中发生的化学反应方程式为_______ 。
(3)上述工艺生产中循环使用的物质除Si、 外,还有
外,还有_______ 。
(4)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为_______ 。
(5)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:_______ 。
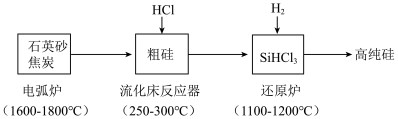
(2)还原炉中发生的化学反应方程式为
(3)上述工艺生产中循环使用的物质除Si、
 外,还有
外,还有(4)工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为
(5)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:

(1)若B是气态氢化物。C、D是氧化物且会造成光化学烟雾污染。写③反应的化学方程式_________ 。
(2)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写④反应离子方程式_________________________________ 。
(3)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中除钠、氧外的元素均为同一主族,且溶液均显碱性。写出②反应的化学方程式_____________________________ 。
(4)若A是当今应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式____________________________________ 。

(1)若B是气态氢化物。C、D是氧化物且会造成光化学烟雾污染。写③反应的化学方程式
(2)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写④反应离子方程式
(3)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中除钠、氧外的元素均为同一主族,且溶液均显碱性。写出②反应的化学方程式
(4)若A是当今应用最广泛的金属。④反应用到A,②⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硅是带来人类文明的重要元素之一,在传统材料发展到信息材料的过程中创造了一个又一个奇迹。
(1)新型陶瓷Si3N4的熔点高、硬度大、化学性质稳定。工业上可以采用化学气相沉积法,在H2的作用下,使SiCl4与N2反应生成Si3N4沉积在石墨表面,该反应的化学方程式为________________________________________________________________________ 。
(2)一种用工业硅(含少量铁、铜的单质及化合物)和氮气(含少量氧气)合成氮化硅的工艺主要流程如下:
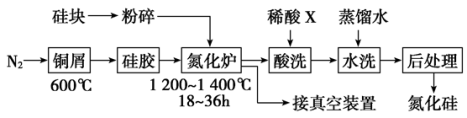
已知硅的熔点是1 420 ℃,高温下氧气及水蒸气能明显腐蚀氮化硅。
①N2净化时,铜屑的作用是:__________________________ ;
硅胶的作用是_______________________________________ 。
②在氮化炉中反应为3Si(s)+2N2(g)===Si3N4(s) ΔH=-727.5 kJ/mol,开始时须严格控制氮气的流速以控制温度的原因是_____________________________________________________ 。
③X可能是________ (选填“盐酸”、“硝酸”、“硫酸”或“氢氟酸”)。
(3)工业上可以通过如下图所示的流程制取纯硅:
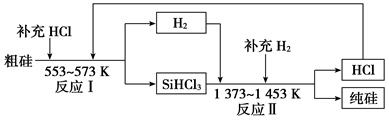
①整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应,该反应的化学方程式为_______________________________ 。
②假设每一轮次制备1 mol纯硅,且生产过程中硅元素没有损失,反应Ⅰ中HCl的利用率为90%,反应Ⅱ中H2的利用率为93.75%。则在第二轮次的生产中,补充投入HCl和H2的物质的量之比是________ 。
(1)新型陶瓷Si3N4的熔点高、硬度大、化学性质稳定。工业上可以采用化学气相沉积法,在H2的作用下,使SiCl4与N2反应生成Si3N4沉积在石墨表面,该反应的化学方程式为
(2)一种用工业硅(含少量铁、铜的单质及化合物)和氮气(含少量氧气)合成氮化硅的工艺主要流程如下:

已知硅的熔点是1 420 ℃,高温下氧气及水蒸气能明显腐蚀氮化硅。
①N2净化时,铜屑的作用是:
硅胶的作用是
②在氮化炉中反应为3Si(s)+2N2(g)===Si3N4(s) ΔH=-727.5 kJ/mol,开始时须严格控制氮气的流速以控制温度的原因是
③X可能是
(3)工业上可以通过如下图所示的流程制取纯硅:

①整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应,该反应的化学方程式为
②假设每一轮次制备1 mol纯硅,且生产过程中硅元素没有损失,反应Ⅰ中HCl的利用率为90%,反应Ⅱ中H2的利用率为93.75%。则在第二轮次的生产中,补充投入HCl和H2的物质的量之比是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】工业上可用粗硅(含铁、铝、硼、磷等杂质)与干燥的HCl气体反应制得SiHCl3:Si+3HCl=SiHCl3+H2,SiHCl3与过量的H2在1000℃~1100℃反应制得纯硅。
有关物质的物理常数见下表:
(1)粗硅与HCl反应完全后,经冷凝得到的SiHCl3中含有少量SiCl4,提纯SiHCl3可采用
___________ 的方法
(2)实验室也可用SiHCl3与过量干燥的H2反应制取纯硅,装置如下图所示(加热和夹持装置略去):
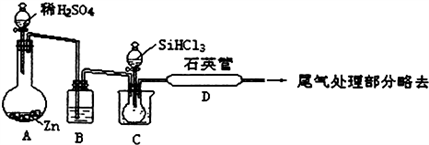
①装置B中的试剂是___________ ,装置C需水浴加热,目的是 ____________________ 。
②反应一段时间后,装置D中可观察到有晶体硅生成,装置D不能采用普通玻璃管的原因是_____________ 。
有关物质的物理常数见下表:
| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | SiHCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | — | 315 | 33.0 | — |
| 熔点/℃ | -70.0 | -107.2 | — | — | -126.5 | — |
| 升华温度/℃ | — | — | 180 | 300 | 162 |
(2)实验室也可用SiHCl3与过量干燥的H2反应制取纯硅,装置如下图所示(加热和夹持装置略去):

①装置B中的试剂是
②反应一段时间后,装置D中可观察到有晶体硅生成,装置D不能采用普通玻璃管的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】 是锂离子电池中广泛应用的电解质。某工厂用LiF、
是锂离子电池中广泛应用的电解质。某工厂用LiF、 为原料,低温反应制备
为原料,低温反应制备 ,其流程如下:
,其流程如下:
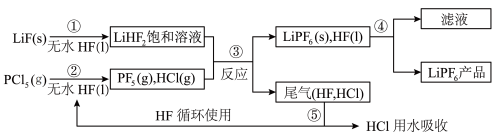
已知:HCl的沸点是-85.0℃,HF的沸点是19.5℃。
(1)第①步反应中无水HF的作用是做反应物和___________ 。反应设备不能用玻璃材质的原因是___________ (用化学方程式表示)。无水HF有腐蚀性和毒性,工厂安全手册提示:如果不小心将HF沾到皮肤上,可立即用2%的___________ 溶液冲洗。
(2)该流程需在无水条件下进行,第②步反应中 极易水解,其产物为两种酸,写出
极易水解,其产物为两种酸,写出 水解的化学方程式:
水解的化学方程式:___________ 。
(3)第④步分离采用的方法是___________ ;第⑤步分离尾气中HF、HCl采用的方法是___________ 。
(4) 产品中通常混有少量LiF.取样品w g,测得Li的物质的量为n mol,则该样品中
产品中通常混有少量LiF.取样品w g,测得Li的物质的量为n mol,则该样品中 的物质的量为
的物质的量为___________ mol(用含有w、n的代数式表示)。
 是锂离子电池中广泛应用的电解质。某工厂用LiF、
是锂离子电池中广泛应用的电解质。某工厂用LiF、 为原料,低温反应制备
为原料,低温反应制备 ,其流程如下:
,其流程如下:
已知:HCl的沸点是-85.0℃,HF的沸点是19.5℃。
(1)第①步反应中无水HF的作用是做反应物和
(2)该流程需在无水条件下进行,第②步反应中
 极易水解,其产物为两种酸,写出
极易水解,其产物为两种酸,写出 水解的化学方程式:
水解的化学方程式:(3)第④步分离采用的方法是
(4)
 产品中通常混有少量LiF.取样品w g,测得Li的物质的量为n mol,则该样品中
产品中通常混有少量LiF.取样品w g,测得Li的物质的量为n mol,则该样品中 的物质的量为
的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W为四种短周期元素。X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价的代数和为6;Z在地壳中的含量仅次于氧;Y、Z、W同周期,W的最低负化合价为-2。回答下列问题:
(1)Y-的结构示意图为____________ 。
(2)写出含有10个中子的X原子的原子符号_____________ 。
(3)Z的最高价氧化物与Z同主族的单质A能发生置换反应,这个反应在工业上是获得Z的一步重要反应。写出该步反应的化学方程式,并用单线桥法标出电子转移的方向与数目________________ 。
(4)向WX2溶液中加入足量的NaOH溶液,反应的离子方程式为___________ 。
(5)Y的气态氢化物与氨气在空气中相遇有白烟生成,该反应的化学方程式为_____________ 。
(6)ZX2与NaOH溶液反应的化学方程式为_____________________ 。
(1)Y-的结构示意图为
(2)写出含有10个中子的X原子的原子符号
(3)Z的最高价氧化物与Z同主族的单质A能发生置换反应,这个反应在工业上是获得Z的一步重要反应。写出该步反应的化学方程式,并用单线桥法标出电子转移的方向与数目
(4)向WX2溶液中加入足量的NaOH溶液,反应的离子方程式为
(5)Y的气态氢化物与氨气在空气中相遇有白烟生成,该反应的化学方程式为
(6)ZX2与NaOH溶液反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】高锰酸钾是一种用途广泛的常见氧化剂,主要用于化工、防腐及制药工业等。
I.某课外小组设计以锰酸钾制备高锰酸钾的方案如下:
i.锰酸钾的制备:
(1)将二氧化锰、氨酸钾和氢氧化钾固体放入___ (填字母)中熔融制锰酸钾。
A. 烧杯 B. 瓷坩埚 C. 蒸发皿 D. 铁坩埚
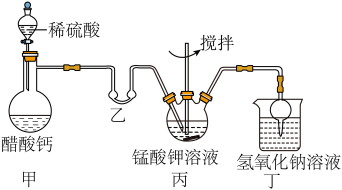
ii.高锰酸钾的制备(装置如图所示,加热及夹持装置省略):
将i中制得的锰酸钾加少量蒸馏水溶解,得墨绿色溶液,倒入三颈烧瓶中。打开甲装置中的分液漏斗活塞加入稀硫酸,加热,使生成的乙酸进入乙装置中并水浴加热。搅拌丙装置中的溶液,锰酸钾在酸性条件下反应生成高锰酸钾和二氧化锰。
(2)检验该装置气密性的方法:连接好装置,___ 。
(3)乙装置的作用是__ ;丁装置中NaOH溶液的作用是________ 。
(4)将三颈烧瓶中所得产物进行过滤,将滤液倒入蒸发皿中,_____ 、_____ 、抽滤,得到针状的高锰酸钾晶体。高锰酸钾晶体只能低温烘干,其原因为_____ 。
II.利用氧化还原滴定法测定高锰酸钾的纯度
(5)量取一定体积的高锰酸钾溶液需使用滴定管____ (填字母)。
A. B.
B. 
(6)若在实验过程中存在下列操作,会使所测KMnO4浓度偏高的是____ (填字母)。
A. 锥形瓶用水洗之后未用待测液润洗
B. 盛草酸溶液的滴定管滴定前尖嘴部分有气泡,滴定终点时无气泡
C. 滴定时,草酸溶液洒落瓶外
D. 盛装KMnO4溶液的滴定管用水洗后,未用KMnO4溶液润洗
I.某课外小组设计以锰酸钾制备高锰酸钾的方案如下:
i.锰酸钾的制备:
(1)将二氧化锰、氨酸钾和氢氧化钾固体放入
A. 烧杯 B. 瓷坩埚 C. 蒸发皿 D. 铁坩埚
ii.高锰酸钾的制备(装置如图所示,加热及夹持装置省略):
将i中制得的锰酸钾加少量蒸馏水溶解,得墨绿色溶液,倒入三颈烧瓶中。打开甲装置中的分液漏斗活塞加入稀硫酸,加热,使生成的乙酸进入乙装置中并水浴加热。搅拌丙装置中的溶液,锰酸钾在酸性条件下反应生成高锰酸钾和二氧化锰。

(2)检验该装置气密性的方法:连接好装置,
(3)乙装置的作用是
(4)将三颈烧瓶中所得产物进行过滤,将滤液倒入蒸发皿中,
II.利用氧化还原滴定法测定高锰酸钾的纯度
(5)量取一定体积的高锰酸钾溶液需使用滴定管
A.
 B.
B. 
(6)若在实验过程中存在下列操作,会使所测KMnO4浓度偏高的是
A. 锥形瓶用水洗之后未用待测液润洗
B. 盛草酸溶液的滴定管滴定前尖嘴部分有气泡,滴定终点时无气泡
C. 滴定时,草酸溶液洒落瓶外
D. 盛装KMnO4溶液的滴定管用水洗后,未用KMnO4溶液润洗
您最近一年使用:0次



