X、Y、Z、W为四种短周期元素。X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价的代数和为6;Z在地壳中的含量仅次于氧;Y、Z、W同周期,W的最低负化合价为-2。回答下列问题:
(1)Y-的结构示意图为____________ 。
(2)写出含有10个中子的X原子的原子符号_____________ 。
(3)Z的最高价氧化物与Z同主族的单质A能发生置换反应,这个反应在工业上是获得Z的一步重要反应。写出该步反应的化学方程式,并用单线桥法标出电子转移的方向与数目________________ 。
(4)向WX2溶液中加入足量的NaOH溶液,反应的离子方程式为___________ 。
(5)Y的气态氢化物与氨气在空气中相遇有白烟生成,该反应的化学方程式为_____________ 。
(6)ZX2与NaOH溶液反应的化学方程式为_____________________ 。
(1)Y-的结构示意图为
(2)写出含有10个中子的X原子的原子符号
(3)Z的最高价氧化物与Z同主族的单质A能发生置换反应,这个反应在工业上是获得Z的一步重要反应。写出该步反应的化学方程式,并用单线桥法标出电子转移的方向与数目
(4)向WX2溶液中加入足量的NaOH溶液,反应的离子方程式为
(5)Y的气态氢化物与氨气在空气中相遇有白烟生成,该反应的化学方程式为
(6)ZX2与NaOH溶液反应的化学方程式为
更新时间:2018-04-24 21:27:24
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】氮化铝(AlN)是一种新型无机材料,工业上由氧化铝与焦炭在氮气流中高温制得,产品中常含有Al4C3、C和Al2O3等杂质。某实验小组为测定a g工业氮化铝样品中AlN的质量及Al4C3的质量分数,设计了如下装置,已知装置B、C、D中的药品均足量。

已知:①AlN和Al4C3均能与水反应,分别生成NH3和CH4。②CH4能与CuO发生反应:CH4+4CuO 4Cu+CO2+2H2O。
4Cu+CO2+2H2O。
(1)写出锥形瓶中发生反应的化学方程式。AlN与H2O反应:__________ ;Al4C3与H2O反应:____________ 。
(2)有下列操作步骤:①缓缓鼓入一定量的N2;②称量C和D(酒精灯和铁架台等除外)的质量,按顺序组装仪器,检查装置的气密性,将样品放入锥形瓶中;③点燃D处酒精灯;④再次称量C和D的质量;⑤从分液漏斗缓缓滴入水,直到不再产生气体时为止;⑥再次缓缓鼓入一定量的N2。正确的操作顺序是_________ 。
(3)C的作用是吸收氨气,则C中所盛试剂的最佳选择是________ (填代号)。
A.蒸馏水 B.浓硝酸C.浓盐酸 D.浓硫酸
(4)A中反应结束后,还要通入一段时间的N2至D中固体恢复到室温,其目的是_______ (写两条)。
(5)实验结束后,测得反应后D中固体质量减少m g,C中增加n g,则a g样品中AlN的质量为________ g,Al4C3的质量分数为________ ×100%。

已知:①AlN和Al4C3均能与水反应,分别生成NH3和CH4。②CH4能与CuO发生反应:CH4+4CuO
 4Cu+CO2+2H2O。
4Cu+CO2+2H2O。(1)写出锥形瓶中发生反应的化学方程式。AlN与H2O反应:
(2)有下列操作步骤:①缓缓鼓入一定量的N2;②称量C和D(酒精灯和铁架台等除外)的质量,按顺序组装仪器,检查装置的气密性,将样品放入锥形瓶中;③点燃D处酒精灯;④再次称量C和D的质量;⑤从分液漏斗缓缓滴入水,直到不再产生气体时为止;⑥再次缓缓鼓入一定量的N2。正确的操作顺序是
(3)C的作用是吸收氨气,则C中所盛试剂的最佳选择是
A.蒸馏水 B.浓硝酸C.浓盐酸 D.浓硫酸
(4)A中反应结束后,还要通入一段时间的N2至D中固体恢复到室温,其目的是
(5)实验结束后,测得反应后D中固体质量减少m g,C中增加n g,则a g样品中AlN的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】钼酸钠(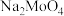 )是制造阻燃剂的原料和无公害型冷水系统的金属腐蚀抑制剂。一种以辉钼矿(主要成分为
)是制造阻燃剂的原料和无公害型冷水系统的金属腐蚀抑制剂。一种以辉钼矿(主要成分为 ,还有少量
,还有少量 、
、 和CuS)为原料制备
和CuS)为原料制备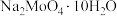 的工艺流程如下:
的工艺流程如下:
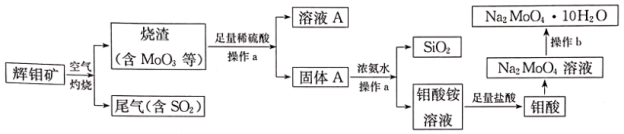
已知:① 不溶于稀酸,不溶于水,能溶于浓氨水和强碱;
不溶于稀酸,不溶于水,能溶于浓氨水和强碱;
②钼酸( )不溶于水,溶于碱。
)不溶于水,溶于碱。
回答下列问题:
(1)操作a的名称是___________ ,溶液A中溶质(除硫酸外)的化学式为___________ 。
(2)写出灼烧过程中 发生反应的化学方程式:
发生反应的化学方程式:___________ 。
(3)尾气中的 可以用
可以用 溶液吸收,写出反应的离子方程式:
溶液吸收,写出反应的离子方程式:___________ 。
(4)固体A中加入浓氨水发生反应的化学方程式为___________ 。
(5)已知钼酸钠的溶解度曲线如图,获得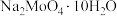 的操作b为蒸发浓缩、
的操作b为蒸发浓缩、___________ 、结晶、过滤。

(6)测量产品中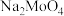 的含量可以采用沉淀法,操作如下:取m1g产品加水溶解,加入足量
的含量可以采用沉淀法,操作如下:取m1g产品加水溶解,加入足量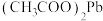 溶液,生成钼酸铅沉淀,在一定温度下干燥沉淀至恒重,称量钼酸铅沉淀的质量为m2g。
溶液,生成钼酸铅沉淀,在一定温度下干燥沉淀至恒重,称量钼酸铅沉淀的质量为m2g。
①为减少测量误差,加入足量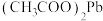 溶液时,应缓慢匀速滴加并同时用玻璃棒搅拌,不能快速滴加,否则会使测量结果
溶液时,应缓慢匀速滴加并同时用玻璃棒搅拌,不能快速滴加,否则会使测量结果___________ (填“偏高”“偏低”或“无影响”)。
②产品中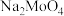 含量为
含量为___________ ×100%。
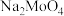 )是制造阻燃剂的原料和无公害型冷水系统的金属腐蚀抑制剂。一种以辉钼矿(主要成分为
)是制造阻燃剂的原料和无公害型冷水系统的金属腐蚀抑制剂。一种以辉钼矿(主要成分为 ,还有少量
,还有少量 、
、 和CuS)为原料制备
和CuS)为原料制备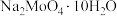 的工艺流程如下:
的工艺流程如下:
已知:①
 不溶于稀酸,不溶于水,能溶于浓氨水和强碱;
不溶于稀酸,不溶于水,能溶于浓氨水和强碱;②钼酸(
 )不溶于水,溶于碱。
)不溶于水,溶于碱。回答下列问题:
(1)操作a的名称是
(2)写出灼烧过程中
 发生反应的化学方程式:
发生反应的化学方程式:(3)尾气中的
 可以用
可以用 溶液吸收,写出反应的离子方程式:
溶液吸收,写出反应的离子方程式:(4)固体A中加入浓氨水发生反应的化学方程式为
(5)已知钼酸钠的溶解度曲线如图,获得
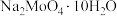 的操作b为蒸发浓缩、
的操作b为蒸发浓缩、
(6)测量产品中
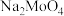 的含量可以采用沉淀法,操作如下:取m1g产品加水溶解,加入足量
的含量可以采用沉淀法,操作如下:取m1g产品加水溶解,加入足量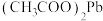 溶液,生成钼酸铅沉淀,在一定温度下干燥沉淀至恒重,称量钼酸铅沉淀的质量为m2g。
溶液,生成钼酸铅沉淀,在一定温度下干燥沉淀至恒重,称量钼酸铅沉淀的质量为m2g。①为减少测量误差,加入足量
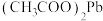 溶液时,应缓慢匀速滴加并同时用玻璃棒搅拌,不能快速滴加,否则会使测量结果
溶液时,应缓慢匀速滴加并同时用玻璃棒搅拌,不能快速滴加,否则会使测量结果②产品中
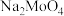 含量为
含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】蛋白质含量是食品营养价值的重要指标之一。凯氏定氮法是测量蛋白质中含氮量的常用方法。实验室测定蛋白质中含氮量的具体流程如下:奶粉样品(质量ag) (NH4)2SO4
(NH4)2SO4 NH3
NH3 (NH4)2B4O7
(NH4)2B4O7 结果处理。回答下列问题:
结果处理。回答下列问题:
(1)“消化”的目的是_______ 。
(2)“蒸馏”和“吸收”操作装置如下图所示(加热及夹持装置略去)。

实验步骤:
①组装好仪器后,向水蒸气发生器内加蒸馏水,并加入数粒玻璃珠。加入玻璃珠的作用是_______ 。
②清洗仪器:打开K1,关闭K2。加热烧瓶使水蒸气充满管路,停止加热,关闭K1。烧杯中蒸馏水倒吸进入反应室,原因是_______ ;打开K2放掉洗涤水,重复操作2~3次。
③向烧杯中加入硼酸溶液及指示剂。消化液由样液入口注入反应室,并注入一定量的氢氧化钠溶液,用蒸馏水冲洗后,封闭样液入口。反应室内反应的离子方程式为_______ ,烧杯中发生反应的化学方程式为_______ 。
④反应装置使用了双层玻璃,其作用是_______ 。
⑤检验蒸馏操作中氨已完全蒸出的方法是_______ 。
(3)“蒸馏”后用cmol·L-1的盐酸标准溶液滴定烧杯内液体,发生的反应为(NH4)2B4O7+2HCl+5H2O=2NH4Cl+4H3BO3,终点时消耗盐酸平均体积为vmL。则该奶粉样品中氮的质量分数为_______ 。
 (NH4)2SO4
(NH4)2SO4 NH3
NH3 (NH4)2B4O7
(NH4)2B4O7 结果处理。回答下列问题:
结果处理。回答下列问题:(1)“消化”的目的是
(2)“蒸馏”和“吸收”操作装置如下图所示(加热及夹持装置略去)。

实验步骤:
①组装好仪器后,向水蒸气发生器内加蒸馏水,并加入数粒玻璃珠。加入玻璃珠的作用是
②清洗仪器:打开K1,关闭K2。加热烧瓶使水蒸气充满管路,停止加热,关闭K1。烧杯中蒸馏水倒吸进入反应室,原因是
③向烧杯中加入硼酸溶液及指示剂。消化液由样液入口注入反应室,并注入一定量的氢氧化钠溶液,用蒸馏水冲洗后,封闭样液入口。反应室内反应的离子方程式为
④反应装置使用了双层玻璃,其作用是
⑤检验蒸馏操作中氨已完全蒸出的方法是
(3)“蒸馏”后用cmol·L-1的盐酸标准溶液滴定烧杯内液体,发生的反应为(NH4)2B4O7+2HCl+5H2O=2NH4Cl+4H3BO3,终点时消耗盐酸平均体积为vmL。则该奶粉样品中氮的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】2022年1月,南太平洋岛国汤加境内发生了“21世纪至今最剧烈的火山喷发”,对该国造成了严重的破坏。火山喷发过程所涉及的转化关系如下:

(1)在上述转化关系中所列出的物质,能与碱反应的氧化物有_______ (填化学式),属于酸的有_______ (填化学式),属于氧化还原反应的是_______ (填序号)。
(2)火山口有淡黄色的硫黄附着,是由于发生了反应④,请写出相应的化学方程式:_______ 。
(3)煤燃烧也会产生的SO2,SO2是形成酸雨的重要原因之一,工业上可采用多种方法减少SO2的排放。利用“双碱法”除去烟气中的SO2,先将SO2通入NaOH溶液,再加入CaO可使NaOH再生。
 ,写出过程①的离子方程式:
,写出过程①的离子方程式:_______ 。
(4)可用酸性高锰酸钾溶液检验脱硫废气中是否含有SO2,若观察到紫色的KMnO4褪色,生成无色的MnSO4,则废气中仍有SO2的存在。请写出此反应的化学方程式:_______ 。

(1)在上述转化关系中所列出的物质,能与碱反应的氧化物有
(2)火山口有淡黄色的硫黄附着,是由于发生了反应④,请写出相应的化学方程式:
(3)煤燃烧也会产生的SO2,SO2是形成酸雨的重要原因之一,工业上可采用多种方法减少SO2的排放。利用“双碱法”除去烟气中的SO2,先将SO2通入NaOH溶液,再加入CaO可使NaOH再生。

 ,写出过程①的离子方程式:
,写出过程①的离子方程式:(4)可用酸性高锰酸钾溶液检验脱硫废气中是否含有SO2,若观察到紫色的KMnO4褪色,生成无色的MnSO4,则废气中仍有SO2的存在。请写出此反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】浓硫酸是中学中常见的一种化学试剂,某学校实验小组为探究浓硫酸与金属的反应并检验生成的气体设计了相关实验。

(1)常温下,将铝片插入浓H2SO4中未发现有明显的变化,其原因为_______ 。
(2)在加热的条件下,浓H2SO4可将铜氧化,写出该反应的化学方程式:_______ 。
(3)实验中使用可抽动的铜丝,其优点是_______ 。
(4)实验中可观察到B中品红溶液的现象为_______ 。
(5)浸有NaOH溶液的棉团的作用_______

(1)常温下,将铝片插入浓H2SO4中未发现有明显的变化,其原因为
(2)在加热的条件下,浓H2SO4可将铜氧化,写出该反应的化学方程式:
(3)实验中使用可抽动的铜丝,其优点是
(4)实验中可观察到B中品红溶液的现象为
(5)浸有NaOH溶液的棉团的作用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】吊白块(NaHSO2•HCHO•2H2O,次硫酸氢钠甲醛)是易溶于水的白色块状或结晶性粉状固体,在印染工业中被用作拔染剂和还原剂。可由Na2S2O5 (焦亚硫酸钠)、甲醛及锌粉反应制取,回答下列问题:
(1)已知在pH=4.1时的过饱和NaHSO3溶液将自动脱水生成Na2S2O5,制备原料Na2S2O5的装置如下。
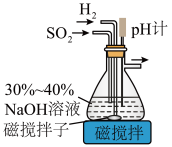
①通入H2的目的是______ 。
②吸滤瓶中先后发生的反应为_______ 、2NaHSO3=Na2S2O5↓+H2O。
③从环境保护和安全考虑,下列尾气处理方法正确的是________ (填标号)。
④实验室用稀NaOH溶液不能制得Na2S2O5,是因为_______ 。
(2)制备吊白块的装置(夹持及加热装置已略)如图:
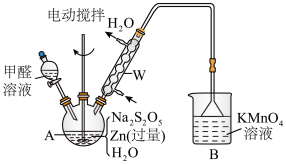
①仪器A的名称是_________ 。
②制备反应需在950C下进行,合适的加热方式是_____ ,A中发生反应的化学方程式为_____ (Zn转化为等物质的量的ZnO和Zn(OH)2)。
③从A中的悬浊液中得到产品吊白块的实验操作是_________ 及干燥。
(1)已知在pH=4.1时的过饱和NaHSO3溶液将自动脱水生成Na2S2O5,制备原料Na2S2O5的装置如下。

①通入H2的目的是
②吸滤瓶中先后发生的反应为
③从环境保护和安全考虑,下列尾气处理方法正确的是

④实验室用稀NaOH溶液不能制得Na2S2O5,是因为
(2)制备吊白块的装置(夹持及加热装置已略)如图:

①仪器A的名称是
②制备反应需在950C下进行,合适的加热方式是
③从A中的悬浊液中得到产品吊白块的实验操作是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】粉煤灰是火电厂的大宗固废。以某电厂的粉煤灰为原料(主要含 、
、 和CaO等)提铝的工艺流程如下:
和CaO等)提铝的工艺流程如下:

回答下列问题:
(1)“浸出”时适当升温的主要目的是___________ , 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)“浸渣”的主要成分有___________ 。
(3)“沉铝”时,体系中三种物质的溶解度曲线如图所示,加入 沉铝的目的是
沉铝的目的是___________ 。

(4)“焙烧”时,主要反应的化学方程式为___________ 。
(5)“水浸”后得到的“滤液2”可返回___________ 工序循环使用。
(6)实验测得,5.0g粉煤灰( 的质量分数为30%)经浸出、干燥后得到3.0g“浸渣”(
的质量分数为30%)经浸出、干燥后得到3.0g“浸渣”( 的质量分数为8%),
的质量分数为8%), 的浸出率为
的浸出率为___________ 。
 、
、 和CaO等)提铝的工艺流程如下:
和CaO等)提铝的工艺流程如下:
回答下列问题:
(1)“浸出”时适当升温的主要目的是
 发生反应的离子方程式为
发生反应的离子方程式为(2)“浸渣”的主要成分有
(3)“沉铝”时,体系中三种物质的溶解度曲线如图所示,加入
 沉铝的目的是
沉铝的目的是
(4)“焙烧”时,主要反应的化学方程式为
(5)“水浸”后得到的“滤液2”可返回
(6)实验测得,5.0g粉煤灰(
 的质量分数为30%)经浸出、干燥后得到3.0g“浸渣”(
的质量分数为30%)经浸出、干燥后得到3.0g“浸渣”( 的质量分数为8%),
的质量分数为8%), 的浸出率为
的浸出率为
您最近一年使用:0次
【推荐2】纳米级 复合材料被认为是一种理想的钠离子电池负极材料,以钼精矿[主要成分
复合材料被认为是一种理想的钠离子电池负极材料,以钼精矿[主要成分 ,以及
,以及 、
、 、
、 、
、 、
、 等杂质]为原料生产纳米级
等杂质]为原料生产纳米级 的工业流程如下:
的工业流程如下:

已知:i. 不溶于水和常见的酸碱,“烧熔”时可转化为酸性氧化物
不溶于水和常见的酸碱,“烧熔”时可转化为酸性氧化物 ;
;
ii. 经“烧熔”后可与沸盐酸反应。
经“烧熔”后可与沸盐酸反应。
(1)“粉碎”的目的为___________ 。
(2)滤液②中含有的金属离子为___________ ;滤渣②的成分为___________ 。
(3)“碱浸”时发生反应的化学方程式为___________ ;用 溶液代替氨水的不足之处为
溶液代替氨水的不足之处为___________ 。
(4)已知“硫代”一步生成了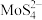 ,则“沉钼”中加入盐酸生成
,则“沉钼”中加入盐酸生成 的离子方程式为
的离子方程式为___________ 。
(5)用 “加热还原”
“加热还原” ,实际操作时需注意的问题为
,实际操作时需注意的问题为___________ 。
(6)分析化学上,常利用“沉钼”反应测定钼的含量,若称量54.0g钼精矿,“沉钼”时得到28.8g ,则钼精矿中钼的百分含量为
,则钼精矿中钼的百分含量为___________ (转化工艺中钼的损失不计,保留三位有效数字)。
 复合材料被认为是一种理想的钠离子电池负极材料,以钼精矿[主要成分
复合材料被认为是一种理想的钠离子电池负极材料,以钼精矿[主要成分 ,以及
,以及 、
、 、
、 、
、 、
、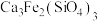 等杂质]为原料生产纳米级
等杂质]为原料生产纳米级 的工业流程如下:
的工业流程如下:
已知:i.
 不溶于水和常见的酸碱,“烧熔”时可转化为酸性氧化物
不溶于水和常见的酸碱,“烧熔”时可转化为酸性氧化物 ;
;ii.
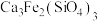 经“烧熔”后可与沸盐酸反应。
经“烧熔”后可与沸盐酸反应。(1)“粉碎”的目的为
(2)滤液②中含有的金属离子为
(3)“碱浸”时发生反应的化学方程式为
 溶液代替氨水的不足之处为
溶液代替氨水的不足之处为(4)已知“硫代”一步生成了
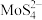 ,则“沉钼”中加入盐酸生成
,则“沉钼”中加入盐酸生成 的离子方程式为
的离子方程式为(5)用
 “加热还原”
“加热还原” ,实际操作时需注意的问题为
,实际操作时需注意的问题为(6)分析化学上,常利用“沉钼”反应测定钼的含量,若称量54.0g钼精矿,“沉钼”时得到28.8g
 ,则钼精矿中钼的百分含量为
,则钼精矿中钼的百分含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】工业上冶炼铝的原料是铝土矿( 主要成分是Al2O3,杂质为Fe2O3、SiO2等)。某研究小组设计的提纯Al2O3的方案如下:
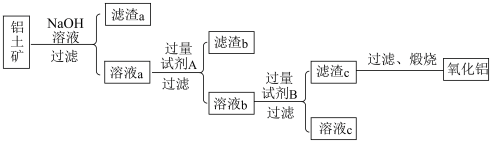
(1)滤渣a中除含泥沙外,一定含有____ ,分离溶液a和滤渣a的操作需要的玻璃仪器为__________________ 。
(2)溶液a中含铝元素的溶质与过量试剂A反应的离子方程式为_______________ ,溶液a与过量试剂A反应生成滤渣b的离子方程式为__________________ 。
(3)溶液b与过量试剂B反应生成滤渣c的离子方程式为_______________________ 。
(4)加热滤渣c得到氧化铝的操作需要使用的仪器除了酒精灯、三角架、泥三角,还有________ (填主要仪器名称),实验室里还常往NaAlO2溶液中通入过量的_______ 来制取A1(OH)3。

(1)滤渣a中除含泥沙外,一定含有
(2)溶液a中含铝元素的溶质与过量试剂A反应的离子方程式为
(3)溶液b与过量试剂B反应生成滤渣c的离子方程式为
(4)加热滤渣c得到氧化铝的操作需要使用的仪器除了酒精灯、三角架、泥三角,还有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4。请回答下列问题:
(1)Y的元素名称是______ 。
(2)W在周期表中的位置是______ 。
(3)写出化合物Z2R的电子式______ 。
(4)写出化合物X2Y2的结构式______ 。
(5)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是______ (用元素的离子符号表示)。
(6)下列说法能证明非金属性Q强于R的是______ (填序号)。
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性: Q>R
(7)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是______ 。
(1)Y的元素名称是
(2)W在周期表中的位置是
(3)写出化合物Z2R的电子式
(4)写出化合物X2Y2的结构式
(5)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(6)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性: Q>R
(7)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】位于前四周期的6种主族元素A、B、C、D、E、F原子序数依次增大,其中B、D同主族, D、E同周期。A、B、C在周期表中相邻,且三种元素的原子最外层电子数之和为18。F是其所在周期中最活泼的金属元素。根据推断回答下列问题:
(1)A在周期表中的位置_______________ ;写出D与F形成的最简单离子化合物的电子式____________________ 。
(2)用“>”或“<”填空:
(3)—定条件,在水溶液中1molE—、EBx—(x=1,2,3,4)的能量(KJ)相对大小如图所示。
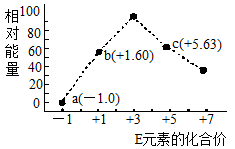
①d点对应的微粒是__________ (填离子符号)。
②b→a+c反应的离子方程式为________________ ,该反应是_________ 反应(填“吸热”或“放热”)
(1)A在周期表中的位置
(2)用“>”或“<”填空:
| 离子半径 | 非金属性 | 酸性 | 沸点 |
| F+ | A | D的最高价氧化物的水化物 | C的氢化物 |
(3)—定条件,在水溶液中1molE—、EBx—(x=1,2,3,4)的能量(KJ)相对大小如图所示。

①d点对应的微粒是
②b→a+c反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】已知X、Y、Z、W均为元素周期表中的短周期元素,它们具有如下特征:
请使用化学用语回答下列问题:
(1)写出Y的两种气体单质的化学式为_______ ,这两种单质的关系是互为_______ ,W的原子结构示意图_______ 。
(2)按从大到小顺序排列X、Y、Z、W的简单离子半径_______ 。
(3)元素Y、Z形成的化合物能与水反应生成Y的气体单质,生成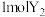 时该反应转移的电子数为
时该反应转移的电子数为_______ ,该化合物阴阳离子个数比为_______ 。元素X、Y形成的化合物也能反应生成Y的气体单质,写出该反应的化学方程式_______ , 该化合物中含有离子数目为
该化合物中含有离子数目为_______ 。
(4)与Z元素同周期的一种金属元素U和一种非金属元素V,它们的最高价氧化物的水化物两两之间可以反应,Z的最高价氧化物的水化物可以检验溶液中是否含有U的离子,写出检验时的实验现象:_______ ,非金属元素V的单质在常温常压下是气体,写出V的单质与Z的最高价氧化物的水化物溶液反应的离子方程式:_______ 。
| 元素 | 特征 |
| X | 在元素周期表中,原子半径最小 |
| Y | 常温下,有 、 、 型两种气体单质存在 型两种气体单质存在 |
| Z | 其原子内层电子数与最外层电子数之比为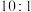 |
| W | 最高化合价为+6价 |
(1)写出Y的两种气体单质的化学式为
(2)按从大到小顺序排列X、Y、Z、W的简单离子半径
(3)元素Y、Z形成的化合物能与水反应生成Y的气体单质,生成
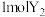 时该反应转移的电子数为
时该反应转移的电子数为 该化合物中含有离子数目为
该化合物中含有离子数目为(4)与Z元素同周期的一种金属元素U和一种非金属元素V,它们的最高价氧化物的水化物两两之间可以反应,Z的最高价氧化物的水化物可以检验溶液中是否含有U的离子,写出检验时的实验现象:
您最近一年使用:0次



