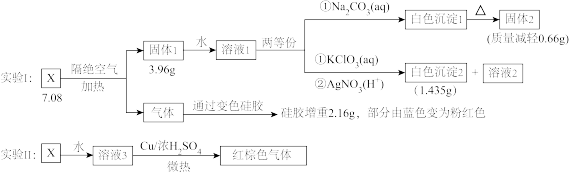
现有中学化学常见的金属单质A、B、C和气体甲、乙、丙、丁以及物质D、E、F、G、H、X,其中气体乙为黄绿色气体,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
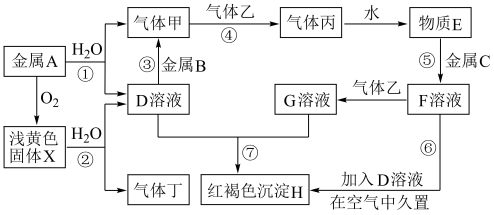
请根据以上信息完成下列各题:
(1)写出反应①的离子方程式:___________ 。
(2)写出反应②的化学方程式:___________ ,该反应的氧化剂是_____ 。
(3)写出反应③的化学方程式:___________ 。
(4)写出反应⑥的化学方程式:___________ 。

请根据以上信息完成下列各题:
(1)写出反应①的离子方程式:
(2)写出反应②的化学方程式:
(3)写出反应③的化学方程式:
(4)写出反应⑥的化学方程式:
更新时间:2024-02-02 17:52:08
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】下图是中学化学中常见物质的转化关系,部分物质和反应条件略去.
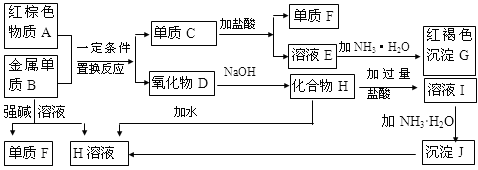
(1)单质F的化学式是________ ,写出物质A的一种用途________ ;
(2)写出单质B与强碱溶液反应的离子方程式________ ,写出由沉淀J生成 H溶液的离子方程式________ ;
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:________ ,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式________ ;
(4)溶液I中所含金属离子是________ 。

(1)单质F的化学式是
(2)写出单质B与强碱溶液反应的离子方程式
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:
(4)溶液I中所含金属离子是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C为为中学常见单质。通常状况下,A为固体,B为黄绿色气体,C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体。它们之间转化关系如图所示(其中某些反应条件和部分反应物已略去)。请回答下列问题:
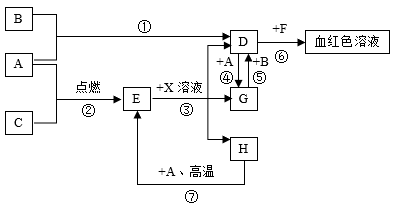
(1)写出下列物质的化学式:A___ 、X___ 。
(2)反应⑦的化学方程式是__ 。
(3)检验D的溶液中是否含有G中阳离子的方法是__ 。
(4)A的一种含氧酸根AO 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是__ 。
(5)在一定量A的氧化物中加入45mL4mol/L硫酸溶液恰好完全反应,所得溶液中A2+能恰好被标准状况下672mL氯气氧化。则该铁的氧化物的化学式为__ ,该氧化物与酸反应的离子方程式为__ 。

(1)写出下列物质的化学式:A
(2)反应⑦的化学方程式是
(3)检验D的溶液中是否含有G中阳离子的方法是
(4)A的一种含氧酸根AO
 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是(5)在一定量A的氧化物中加入45mL4mol/L硫酸溶液恰好完全反应,所得溶液中A2+能恰好被标准状况下672mL氯气氧化。则该铁的氧化物的化学式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】(1)下列A、B、C、D是中学常见的混合物分离或提纯的基本装置。
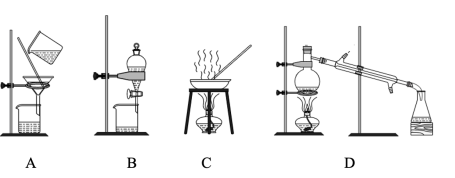
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
①从碘水中提取碘___________ ;
②除去Ca(OH)2溶液中悬浮的CaCO3___________ ;
③用自来水制取蒸馏水___________ ;
④与海水晒盐原理相符的是___________ 。
(2)某校学生课外活动小组为测定钠元素的相对原子质量,设计的装置如图所示,该装置(包括水和干燥剂)的总质量为ag,从实验室取出bg(不足量)钠放入水中,塞紧瓶塞,完全反应后再称量此装置的总质量为cg。试回答:
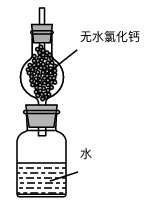
①此干燥管的作用是___________ ;若此钠块有极少量被氧化,则测出的相对原子质量会比实际相对原子质量___________ (填“偏大”、“偏小”或“不变”)。
②有甲同学建议在图中干燥管上再连一同样干燥管,其目的是___________ ,计算钠的相对原子质量的表达式为___________ 。
③有乙同学为避免由于行动不够迅速产生偏差,又建议在集气瓶中再加入一定量煤油,其目的是___________ 。

请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。
①从碘水中提取碘
②除去Ca(OH)2溶液中悬浮的CaCO3
③用自来水制取蒸馏水
④与海水晒盐原理相符的是
(2)某校学生课外活动小组为测定钠元素的相对原子质量,设计的装置如图所示,该装置(包括水和干燥剂)的总质量为ag,从实验室取出bg(不足量)钠放入水中,塞紧瓶塞,完全反应后再称量此装置的总质量为cg。试回答:

①此干燥管的作用是
②有甲同学建议在图中干燥管上再连一同样干燥管,其目的是
③有乙同学为避免由于行动不够迅速产生偏差,又建议在集气瓶中再加入一定量煤油,其目的是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】Ⅰ.探究金属钠与水反应实验过程中,某课外小组同学记录了如下实验现象和实验结论:
①有碱生成;②溶液变红;③钠四处游动;④钠浮在水面上;⑤有气体产生;⑥钠的密度比水小;⑦钠熔成光亮的小球;⑧反应放热,钠熔点低。
(1)请填写下表中的空格(从①~⑧中选择,填序号):
(2)写出钠与水反应的离子方程式:________ 。
Ⅱ.某课外活动小组设计下列装置,验证二氧化碳跟过氧化钠反应时,需要与水接触。
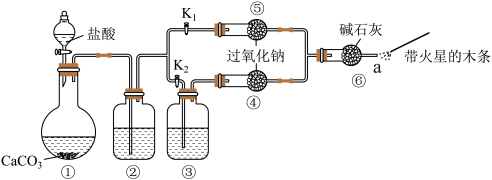
【装置分析】
(3)装置①中反应的离子方程式是________ 。
(4)已知盐酸具有挥发性。装置②中的试剂是________ ,②中反应的离子方程式是________ 。
(5)装置③中的试剂是________ 。
【进行实验】
步骤1:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
步骤2:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
(6)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是________ 、________ 。
(7)写出过氧化钠跟二氧化碳反应的化学方程式并标出反应过程中的电子转移方向和数目:________ 。
Ⅲ.欲探究 和
和 稳定性的相对强弱,两同学分别设计以下两组装置:
稳定性的相对强弱,两同学分别设计以下两组装置:
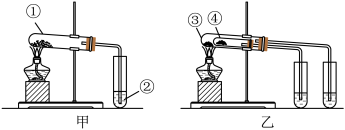
(8)如甲图所示,分别用 和
和 做实验,试管②中的试剂是
做实验,试管②中的试剂是________ 。试管①中发生反应的化学方程式是________ 。
(9)如乙图所示,试管④中装入的固体应该是________ (填化学式)。
(10)通过上述实验,得出的结论是; 比
比 的稳定性
的稳定性________ (填“强”或“弱”)。
(11)向浓度相等、体积均为50mL的A、B两份NaOH溶液中,分别通入一定量的 后,均稀释至100mL。向稀释后的溶液中,逐滴滴加0.1mol/L盐酸,产生
后,均稀释至100mL。向稀释后的溶液中,逐滴滴加0.1mol/L盐酸,产生 的体积(已折合至标准状况)与所加盐酸的体积关系如图所示。
的体积(已折合至标准状况)与所加盐酸的体积关系如图所示。
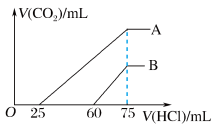
①A曲线表明,原溶液通入 后,所得溶质与盐酸反应产生
后,所得溶质与盐酸反应产生 的最大体积为
的最大体积为________ mL(标准状况)。
②B曲线表明,原溶液通入 后,所得溶液中溶质的化学式为
后,所得溶液中溶质的化学式为________ 。
③原NaOH溶液的物质的量浓度为________ 。
①有碱生成;②溶液变红;③钠四处游动;④钠浮在水面上;⑤有气体产生;⑥钠的密度比水小;⑦钠熔成光亮的小球;⑧反应放热,钠熔点低。
(1)请填写下表中的空格(从①~⑧中选择,填序号):
实验现象 | ⑦ | ③ | ||
实验结论 | ⑥ | ① |
Ⅱ.某课外活动小组设计下列装置,验证二氧化碳跟过氧化钠反应时,需要与水接触。

【装置分析】
(3)装置①中反应的离子方程式是
(4)已知盐酸具有挥发性。装置②中的试剂是
(5)装置③中的试剂是
【进行实验】
步骤1:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。步骤2:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。
,打开分液漏斗活塞加入盐酸,将带火星的木条放在处。(6)步骤1和步骤2中,a处带火星的木条产生的实验现象分别是
(7)写出过氧化钠跟二氧化碳反应的化学方程式并标出反应过程中的电子转移方向和数目:
Ⅲ.欲探究
 和
和 稳定性的相对强弱,两同学分别设计以下两组装置:
稳定性的相对强弱,两同学分别设计以下两组装置:
(8)如甲图所示,分别用
 和
和 做实验,试管②中的试剂是
做实验,试管②中的试剂是(9)如乙图所示,试管④中装入的固体应该是
(10)通过上述实验,得出的结论是;
 比
比 的稳定性
的稳定性(11)向浓度相等、体积均为50mL的A、B两份NaOH溶液中,分别通入一定量的
 后,均稀释至100mL。向稀释后的溶液中,逐滴滴加0.1mol/L盐酸,产生
后,均稀释至100mL。向稀释后的溶液中,逐滴滴加0.1mol/L盐酸,产生 的体积(已折合至标准状况)与所加盐酸的体积关系如图所示。
的体积(已折合至标准状况)与所加盐酸的体积关系如图所示。
①A曲线表明,原溶液通入
 后,所得溶质与盐酸反应产生
后,所得溶质与盐酸反应产生 的最大体积为
的最大体积为②B曲线表明,原溶液通入
 后,所得溶液中溶质的化学式为
后,所得溶液中溶质的化学式为③原NaOH溶液的物质的量浓度为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A___________ 、B___________ 、C____________ 、
F___________ 、H___________ 、乙____________ 。
(2)写出下列反应离子方程式:
反应①______________________
反应⑥_____________________

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A
F
(2)写出下列反应离子方程式:
反应①
反应⑥
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】下图是元素周期表的一部分,表中列出了①〜⑨种元素的位置,请根据要求回答问题。
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为________________ 。
(2)②与④形成的化合物的电子式可表示为_________________________________________ 。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是____________________ (填化学式)。
(4)写出⑤与氢氧化钠溶液反应的化学方程式:_____________________________________ 。
族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | VIA | ⅦA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ |
(2)②与④形成的化合物的电子式可表示为
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
(4)写出⑤与氢氧化钠溶液反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】镁在空气里点燃可以燃烧,放出大量的热并发出耀眼的白光,生成白色的氧化镁,同时,镁在这样的高温条件下,还可与空气中的另一种主要成分反应,生成少量的物质A,已知A可发生如图的一系列变化:
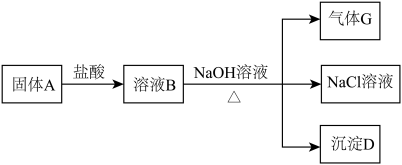
(1)写出A、C、D的化学式:A_____ 、C_____ 、D______ 。
(2)写出下列变化的化学方程式:
①固体A+盐酸:______ 。
②溶液B+NaOH溶液:______ 。

(1)写出A、C、D的化学式:A
(2)写出下列变化的化学方程式:
①固体A+盐酸:
②溶液B+NaOH溶液:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】已知:A、F为金属单质,D、E为气体单质,E是黄绿色气体,其余均为化合物,其中B为黑色粉末,C的焰色试验呈黄色,金属单质F既可以与C溶液反应,也可以与G溶液反应,且均产生D气体。各物质间的转化关系如图所示。(部分生成物已略去)
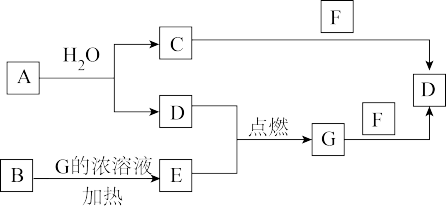
回答下列问题:
(1)单质A为___________ ,D在E中燃烧的实验现象___________ 。
(2)B与G的浓溶液反应时,每生成标准状况下33.6L E气体,被氧化的G的物质的量为___________ 。
(3)写出C溶液与F反应的化学方程式___________ 。
(4)相同质量的两份F,分别放入足量的G和C溶液中,产生的D气体在同温同压下的体积之比为___________ 。
(5)将5.4gF投入到1L1mol/L的G溶液中,向其中滴入2mol/L的C溶液,当沉淀的质量为7.8g时,加入的C溶液的体积为___________

回答下列问题:
(1)单质A为
(2)B与G的浓溶液反应时,每生成标准状况下33.6L E气体,被氧化的G的物质的量为
(3)写出C溶液与F反应的化学方程式
(4)相同质量的两份F,分别放入足量的G和C溶液中,产生的D气体在同温同压下的体积之比为
(5)将5.4gF投入到1L1mol/L的G溶液中,向其中滴入2mol/L的C溶液,当沉淀的质量为7.8g时,加入的C溶液的体积为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀,W溶液中滴加KSCN溶液出现血红色。

(1)物质A的化学式为___ ,F化学式为___ ;
(2)B和R在溶液中反应生成F的离子方程式为___ ;
(3)H在潮湿空气中变成M的实验现象是___ ,化学方程式为___ 。
(4)A和水反应生成B和C的离子方程式为___ ,由此反应可知A有作为___ 的用途。
(5)M投入盐酸中的离子方程式___ 。

(1)物质A的化学式为
(2)B和R在溶液中反应生成F的离子方程式为
(3)H在潮湿空气中变成M的实验现象是
(4)A和水反应生成B和C的离子方程式为
(5)M投入盐酸中的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】某些金属氧化物跟熔融烧碱反应可生成盐,根据图中化学反应方框图填空:
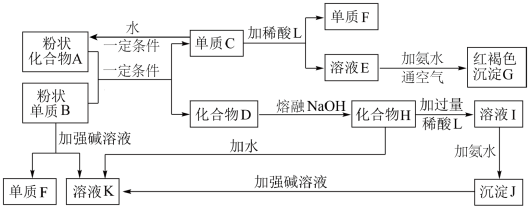
(1)单质F是________ ;
(2)写出由E生成G的离子方程式(或化学方程式)_______ ;
(3)溶液I中所含金属离子是________ ;
(4)由C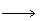 E+F若改用浓酸,则不能选用的浓酸是(写分子式)
E+F若改用浓酸,则不能选用的浓酸是(写分子式)________ 。
(5)写出单质C转化为A的化学方程式:___________________________________ 。
(6)化合物A与盐酸反应的离子方程式为:___________________________________ 。

(1)单质F是
(2)写出由E生成G的离子方程式(或化学方程式)
(3)溶液I中所含金属离子是
(4)由C
 E+F若改用浓酸,则不能选用的浓酸是(写分子式)
E+F若改用浓酸,则不能选用的浓酸是(写分子式)(5)写出单质C转化为A的化学方程式:
(6)化合物A与盐酸反应的离子方程式为:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】A、B、C为中学常见单质,其中一种为金属;通常情况下A为固体,B为黄绿色气体,C为无色气体;D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种无氧强酸溶液,E为黑色固体,H在常温下为液体,它们之间的转化关系如图所示(其中某些反应条件和部分反应产物已略去):

(1)写出下列物质的化学式:D___________ ;X___________
(2)在反应①~⑦中,不属于氧化还原反应的是___________ (填序号)。
(3)往G溶液中加入NaOH溶液观察到的现象是___________
(4)反应⑦的化学方程式为___________ ,该反应中每消耗0.3mol的A,可转移电子___________ mol。
(5)反应③的离子方程式___________

(1)写出下列物质的化学式:D
(2)在反应①~⑦中,不属于氧化还原反应的是
(3)往G溶液中加入NaOH溶液观察到的现象是
(4)反应⑦的化学方程式为
(5)反应③的离子方程式
您最近一年使用:0次

 、
、 、
、 外,还有
外,还有

