某些金属氧化物跟熔融烧碱反应可生成盐,根据图中化学反应方框图填空:
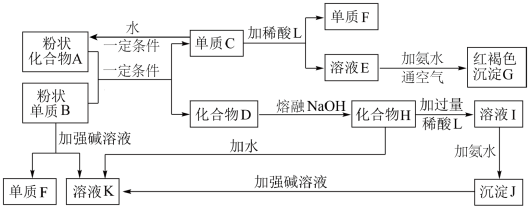
(1)单质F是________ ;
(2)写出由E生成G的离子方程式(或化学方程式)_______ ;
(3)溶液I中所含金属离子是________ ;
(4)由C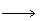 E+F若改用浓酸,则不能选用的浓酸是(写分子式)
E+F若改用浓酸,则不能选用的浓酸是(写分子式)________ 。
(5)写出单质C转化为A的化学方程式:___________________________________ 。
(6)化合物A与盐酸反应的离子方程式为:___________________________________ 。

(1)单质F是
(2)写出由E生成G的离子方程式(或化学方程式)
(3)溶液I中所含金属离子是
(4)由C
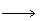 E+F若改用浓酸,则不能选用的浓酸是(写分子式)
E+F若改用浓酸,则不能选用的浓酸是(写分子式)(5)写出单质C转化为A的化学方程式:
(6)化合物A与盐酸反应的离子方程式为:
11-12高一上·辽宁沈阳·期中 查看更多[1]
(已下线)2011-2012学年辽宁省沈阳东北育才学校高一上学期期中考试化学试卷
更新时间:2016/12/09 02:30:57
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】下列框图中的A~J是中学化学中常见的八种物质,所有物质均由短周期元素组成,已知常温、常压下D为无色液体, C、E、G均为气体单质,B为金属,I是由3个原子组成的一元含氧弱酸分子, A~J可发生如下转化:

请填写下列空白:
(1)G的名称为_______ ,F的电子式为_______ 。
(2)15.6gA与D完全反应,转移的电子的物质的量为_______ 。
(3)常温下,A为一种_______ 色的固体,它的一种重要用途是_______ 。
(4)写出D、G反应转化为I和J的离子方程式_______ 。

请填写下列空白:
(1)G的名称为
(2)15.6gA与D完全反应,转移的电子的物质的量为
(3)常温下,A为一种
(4)写出D、G反应转化为I和J的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】金属单质及其化合物在生产生活中应用非常广泛,废旧金属的回收利用是重要研究课题。某学习小组在实验室中模拟利用含铜废料(主要成分为Cu和CuO,还有少量的Al、Fe及其氧化物)生产胆矾,其实验方案如下:

(1)上述流程中,将废铜料研磨的目的是_______
(2)碱浸的化学方程式_______
(3)酸溶后所得溶液中的溶质主要有_______ ;
(4)请写出酸溶过程中单质铜发生反应的化学方程式:_______ ;
(5)试剂X可以是_______ ;操作2所得的滤渣是_______
(6)操作3是一系列操作。其操作为_______ 、冷却结晶、过滤、_______ 、干燥。

(1)上述流程中,将废铜料研磨的目的是
(2)碱浸的化学方程式
(3)酸溶后所得溶液中的溶质主要有
(4)请写出酸溶过程中单质铜发生反应的化学方程式:
(5)试剂X可以是
(6)操作3是一系列操作。其操作为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】下图表示有关物质之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物(反应条件图中已省略)

(1)A,D代表的物质分别为:________ ,________ (填化学式);
(2)反应①中的C,D均过量,该反应的化学方程式是____________________________________ ;
(3)反应②中,若B与F物质的量之比为4∶3,G,H分别是_______ ,_______ (填化学式);其物质的量之比为__________ .
(4)反应③产物中K的化学式为____________ ;④的离子方程式为_____________________________ .

(1)A,D代表的物质分别为:
(2)反应①中的C,D均过量,该反应的化学方程式是
(3)反应②中,若B与F物质的量之比为4∶3,G,H分别是
(4)反应③产物中K的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
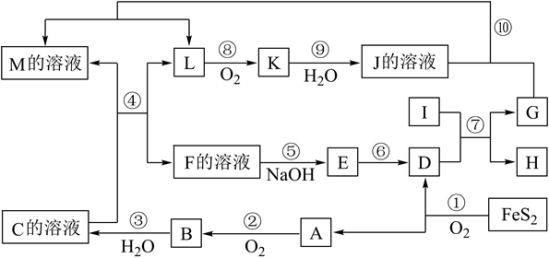
请填写下来空白:
(1)在周期表中,组成单质G的元素位于第______ 周期第________ 族。
(2)反应⑦的化学反应方程式为________________
(3)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是_______ (填写序号)
(4)反应④的离子方程式是:____________________
(5)将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是:_____________________

请填写下来空白:
(1)在周期表中,组成单质G的元素位于第
(2)反应⑦的化学反应方程式为
(3)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是
(4)反应④的离子方程式是:
(5)将化合物D与KNO3、KOH共融,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:
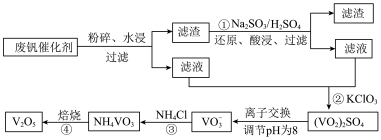
部分含钒物质在水中的溶解性如下:
回答下列问题:
(1)工业由V2O5冶炼金属钒常用铝热剂法,写出该反应的化学方程式______________ 。
(2)滤液中含钒的主要成分为_______ (写化学式)。
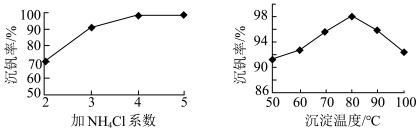
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式__________________________ ;沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度。根据下图判断最佳控制氯化铵系数和温度为_______ 、_______ 。
(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,反应的离子方程式为VO2+ +H2C2O4+□_____ =VO2++CO2↑+H2O,试将其配平。
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为VO2+ +V2++2H+ VO2++H2O+V3+,电池充电时阳极的电极反应式为
VO2++H2O+V3+,电池充电时阳极的电极反应式为______________________ 。

部分含钒物质在水中的溶解性如下:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
(1)工业由V2O5冶炼金属钒常用铝热剂法,写出该反应的化学方程式
(2)滤液中含钒的主要成分为
(3)该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式

(4)用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,反应的离子方程式为VO2+ +H2C2O4+□
(5)全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为VO2+ +V2++2H+
 VO2++H2O+V3+,电池充电时阳极的电极反应式为
VO2++H2O+V3+,电池充电时阳极的电极反应式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】图中X、Y、Z为单质,其他为化合物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁,E是不溶于水的酸性氧化物,能与氢氟酸反应。
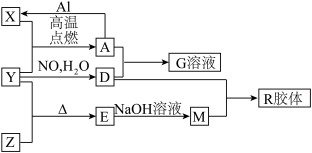
回答下列问题:
(1)组成单质Z的元素在周期表中的位置是________ ;M中存在的化学键类型为________ ;R的化学式是______________ 。
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为____________ 。
(3)已知A与1 mol Al反应转化为X时(所有物质均为固体),放出a kJ热量。写出该反应的热化学方程式:_____________________________________________________________ 。
(4)写出A和D的稀溶液反应生成G的离子方程式:__________________________________ 。

回答下列问题:
(1)组成单质Z的元素在周期表中的位置是
(2)一定条件下,Z与H2反应生成ZH4,ZH4的电子式为
(3)已知A与1 mol Al反应转化为X时(所有物质均为固体),放出a kJ热量。写出该反应的热化学方程式:
(4)写出A和D的稀溶液反应生成G的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】某混合物 A,含有 KAl(SO4)2、Al2O3 和 Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
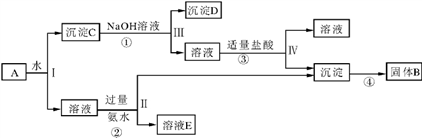
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是__________ 。
(2)根据上述框图反应关系,写出下列B、C、D 所含物质的化学式(提示:可为混合物)。
固体 B_________ ;沉淀 C__________ ;沉淀 D _________ ;
(3)写出①、②反应离子方程式。
①___________________________________________ ;
②___________________________________________ ;
(4)步骤③较难操作,如何将实验方案进行改进?_______________________________ 。

据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是
(2)根据上述框图反应关系,写出下列B、C、D 所含物质的化学式(提示:可为混合物)。
固体 B
(3)写出①、②反应离子方程式。
①
②
(4)步骤③较难操作,如何将实验方案进行改进?
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】请回答下列问题:
(1)取少量红棕色的氧化铁粉末溶于适量盐酸中,得到棕黄色的氯化铁溶液。反应的离子方程式为_______ 。
(2)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴上述氯化铁溶液,继续煮沸至溶液呈红褐色,停止加热,可制得氢氧化铁胶体。发生反应的离子方程式是_______ 。
(3)向上述制得的 胶体中逐滴滴入过量盐酸,出现的现象是
胶体中逐滴滴入过量盐酸,出现的现象是_______ ,发生反应的离子方程式为_______ 。
(4)某无色澄清的溶液,其中可能含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种,且各离子的数目相等。作了如下实验,以确定这些离子是否存在。
中的若干种,且各离子的数目相等。作了如下实验,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2mL该溶液用 溶液和稀硝酸进行检验,结果生成了白色沉淀。
溶液和稀硝酸进行检验,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用 溶液和稀硝酸进行检验,结果又生成了白色沉淀。
溶液和稀硝酸进行检验,结果又生成了白色沉淀。
实验②中发生反应的离子方程式为_______ ,原溶液中一定存在的离子有_______ ;原溶液中 的存在情况为
的存在情况为_______ 。
A.一定存在 B.一定不存在 C.无法确定
(1)取少量红棕色的氧化铁粉末溶于适量盐酸中,得到棕黄色的氯化铁溶液。反应的离子方程式为
(2)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴上述氯化铁溶液,继续煮沸至溶液呈红褐色,停止加热,可制得氢氧化铁胶体。发生反应的离子方程式是
(3)向上述制得的
 胶体中逐滴滴入过量盐酸,出现的现象是
胶体中逐滴滴入过量盐酸,出现的现象是(4)某无色澄清的溶液,其中可能含有
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种,且各离子的数目相等。作了如下实验,以确定这些离子是否存在。
中的若干种,且各离子的数目相等。作了如下实验,以确定这些离子是否存在。①用石蕊试液检测该溶液时,溶液显红色。
②取2mL该溶液用
 溶液和稀硝酸进行检验,结果生成了白色沉淀。
溶液和稀硝酸进行检验,结果生成了白色沉淀。③对②中所得的混合物充分静置后,取其上层澄清的液体用
 溶液和稀硝酸进行检验,结果又生成了白色沉淀。
溶液和稀硝酸进行检验,结果又生成了白色沉淀。实验②中发生反应的离子方程式为
 的存在情况为
的存在情况为A.一定存在 B.一定不存在 C.无法确定
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
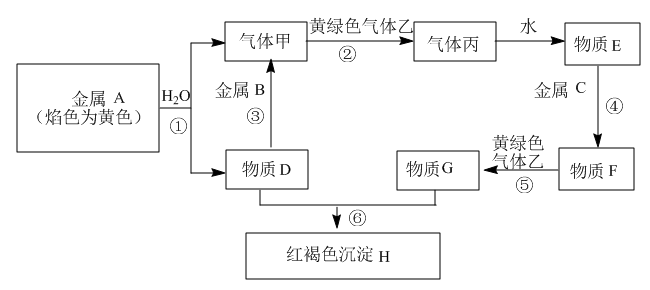
【推荐3】几种中学化学常见的单质及其化合物相互转化的关系图如下:
①甲、乙、丙、丁为单质,其余为化合物。
②A由X和Y两种元素组成,其原子个数比为1∶2,元素质量之比为7∶8。
③B气体是引起酸雨的主要物质,H常温下为无色无味的液体,E常用作红色油漆和涂料。
试根据上述信息回答下列问题:
(1)A的化学式为_______ ,每反应1molA转移的电子数为_______ mol;
(2)F与丁单质也可以化合生成G,试写出该反应的离子方程式_______ ;
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③。_______ ;
(4)化合物M与H组成元素相同,可以将G氧化为F,且不引进新的离子。试写出M在酸性环境下将G氧化为F的离子方程式:_______ 。
①甲、乙、丙、丁为单质,其余为化合物。
②A由X和Y两种元素组成,其原子个数比为1∶2,元素质量之比为7∶8。
③B气体是引起酸雨的主要物质,H常温下为无色无味的液体,E常用作红色油漆和涂料。
试根据上述信息回答下列问题:
(1)A的化学式为
(2)F与丁单质也可以化合生成G,试写出该反应的离子方程式
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③。

(4)化合物M与H组成元素相同,可以将G氧化为F,且不引进新的离子。试写出M在酸性环境下将G氧化为F的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
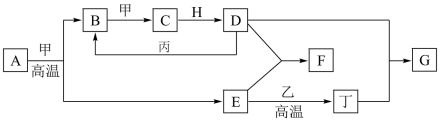
【推荐1】已知A为单质,与某物质反应生成气体与B,有以下物质相互转化:
(1)写出B的化学式____ ,D的化学式________ 。
(2)写出由E转变成F的化学方程式______ 。
(3)写出用KSCN鉴别G溶液的离子方程式__ ,向G溶液加入A的有关离子反应方程式__ 。

(1)写出B的化学式
(2)写出由E转变成F的化学方程式
(3)写出用KSCN鉴别G溶液的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
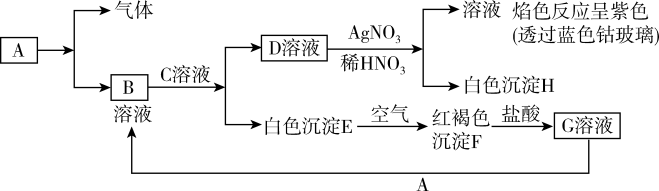
【推荐2】现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。
请回答下列问题:
(1)写出下列物质的化学式:丙_________ 、乙_________ 。
(2)图中反应①②③④⑤⑥中属于氧化还原反应的有:_____________________ ,属于置换反应反应的有:_______________ 。
(3)写出反应⑤的离子方程式:_____________________ ;
(4)写出反应①的化学方程式_______________________________ ,当得到标准状况 下的甲气体2.24L,则参加反应的金属A____________ g。

请回答下列问题:
(1)写出下列物质的化学式:丙
(2)图中反应①②③④⑤⑥中属于氧化还原反应的有:
(3)写出反应⑤的离子方程式:
(4)写出反应①的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】碳酸亚铁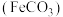 难溶于水,常用于制取铁或补血剂。一种
难溶于水,常用于制取铁或补血剂。一种 的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得
的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得 沉淀。
沉淀。
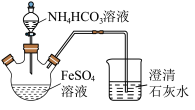
(1)恰好完全反应后,检验三颈烧瓶内溶液中阳离子的方法是___________ 。
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是___________ 。
(3) 在潮湿的空气中先转化为
在潮湿的空气中先转化为 ,最终变为
,最终变为 ,并进一步转化为
,并进一步转化为 。写出
。写出 在潮湿的空气中转化为
在潮湿的空气中转化为 的化学方程式:
的化学方程式:___________ 。
(4)某 固体被部分氧化,为测定其中
固体被部分氧化,为测定其中 的质量分数,现进行如下实验:称取
的质量分数,现进行如下实验:称取 固体样品,加足量盐酸充分溶解,将溶液稀释至
固体样品,加足量盐酸充分溶解,将溶液稀释至 。量取
。量取 该溶液,加入
该溶液,加入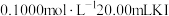 溶液,两者正好完全反应。已知实验过程中发生反应如下:
溶液,两者正好完全反应。已知实验过程中发生反应如下: 。计算
。计算 固体样品中
固体样品中 的质量分数,写出计算过程
的质量分数,写出计算过程___________ 。
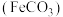 难溶于水,常用于制取铁或补血剂。一种
难溶于水,常用于制取铁或补血剂。一种 的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得
的制备装置如下图所示。实验中观察到三颈烧瓶中有大量白色沉淀产生,烧杯中溶液变浑浊,恰好完全反应时,三颈烧瓶内溶液中只含一种溶质。过滤后可得 沉淀。
沉淀。
(1)恰好完全反应后,检验三颈烧瓶内溶液中阳离子的方法是
(2)反应后所得沉淀需进行过滤、洗涤。检验沉淀已经洗涤干净的方法是
(3)
 在潮湿的空气中先转化为
在潮湿的空气中先转化为 ,最终变为
,最终变为 ,并进一步转化为
,并进一步转化为 。写出
。写出 在潮湿的空气中转化为
在潮湿的空气中转化为 的化学方程式:
的化学方程式:(4)某
 固体被部分氧化,为测定其中
固体被部分氧化,为测定其中 的质量分数,现进行如下实验:称取
的质量分数,现进行如下实验:称取 固体样品,加足量盐酸充分溶解,将溶液稀释至
固体样品,加足量盐酸充分溶解,将溶液稀释至 。量取
。量取 该溶液,加入
该溶液,加入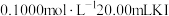 溶液,两者正好完全反应。已知实验过程中发生反应如下:
溶液,两者正好完全反应。已知实验过程中发生反应如下: 。计算
。计算 固体样品中
固体样品中 的质量分数,写出计算过程
的质量分数,写出计算过程
您最近一年使用:0次



