下图是中学化学中常见物质的转化关系,部分物质和反应条件略去.
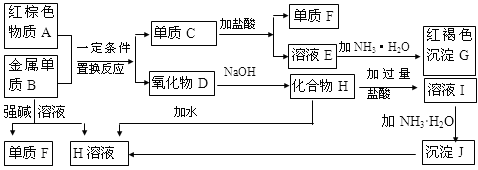
(1)单质F的化学式是________ ,写出物质A的一种用途________ ;
(2)写出单质B与强碱溶液反应的离子方程式________ ,写出由沉淀J生成 H溶液的离子方程式________ ;
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:________ ,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式________ ;
(4)溶液I中所含金属离子是________ 。

(1)单质F的化学式是
(2)写出单质B与强碱溶液反应的离子方程式
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式:
(4)溶液I中所含金属离子是
更新时间:2016-12-09 11:19:07
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】A、B、C、D均为中学化学中常见的物质,它们之间转化关系如图(部分产物已略去):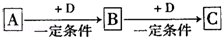
试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为________ (填元素符号)
(2)若D是金属,C溶液在储存时应加入少量D,其理由是_______________ (用离子方程式表示)
(3)若A、B、C为含同一种金属元素的无机化合物且B不溶于水,在溶液中A和C反应生成B.请写出B转化为C的所有可能的离子方程式_____________________ ,___________________ ,A与C反应的离子方程式:___________________
(4)化合物B经过一系列反应可以得到单质E,将一定质量的Mg和E 的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则固体混合物中Mg的质量为______ ;NaOH溶液的物质的量浓度为______
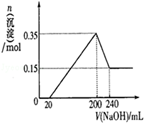
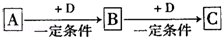
试回答:
(1)若D是具有氧化性的单质,则属于主族的金属A为
(2)若D是金属,C溶液在储存时应加入少量D,其理由是
(3)若A、B、C为含同一种金属元素的无机化合物且B不溶于水,在溶液中A和C反应生成B.请写出B转化为C的所有可能的离子方程式
(4)化合物B经过一系列反应可以得到单质E,将一定质量的Mg和E 的混合物投入500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则固体混合物中Mg的质量为

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为FeSO4溶液,G为CuSO4溶液,它们之间存在如图所示关系:

(1)推测下列物质的化学式A_______ ,B_________ ,F______________ 。
(2)写出A→C转化的化学方程式_________________ 。
(3)写出C+G→D+F转化的离子方程式_____________________ 。

(1)推测下列物质的化学式A
(2)写出A→C转化的化学方程式
(3)写出C+G→D+F转化的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】I.下图是100mgCaC2O4~H2O受热分解时,所得固体产物的质量随温度变化的曲线。试利用图中信息结合所学的知识,回答下列各问题:
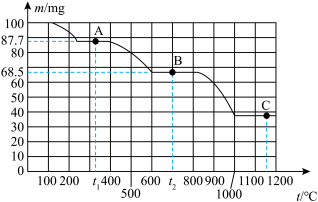
(1)温度分别为t1和t2时,固体产物的化学式A是_____ ,B是_____ 。
(2)由A得到B的化学方程式为_____ 。
(3)由图计算并推断C的合理的化学式:_____ 。
II.测定亚氯酸钠的含量:
实验步骤:
①准确称取所得亚氯酸钠样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液配成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用cmoL·-1Na2S2O3标准溶液滴定至终点,重复2次,测得消耗Na2S2O3标准溶液体积的平均值为VmL。(已知: 、
、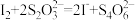 )
)
(4)达到滴定终点时的现象为_____ 。
(5)该样品中NaC1O2的质量分数为_____ %(用含m、c、V的代数式表示)。在滴定操作正确的情况下,此实验测得结果偏高,可能原因为_____ (用离子方程式表示)。

(1)温度分别为t1和t2时,固体产物的化学式A是
(2)由A得到B的化学方程式为
(3)由图计算并推断C的合理的化学式:
II.测定亚氯酸钠的含量:
实验步骤:
①准确称取所得亚氯酸钠样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液配成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用cmoL·-1Na2S2O3标准溶液滴定至终点,重复2次,测得消耗Na2S2O3标准溶液体积的平均值为VmL。(已知:
 、
、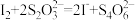 )
)(4)达到滴定终点时的现象为
(5)该样品中NaC1O2的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A___________ 、B___________ 、C____________ 、
F___________ 、H___________ 、乙____________ 。
(2)写出下列反应离子方程式:
反应①______________________
反应⑥_____________________

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A
F
(2)写出下列反应离子方程式:
反应①
反应⑥
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】近两年我国电动汽车发展迅速。电动汽车的动力锂离子电池常用磷酸亚铁锂( )作电极材料。该类废旧电极(含杂质Al、石墨粉)回收处理和资源再利用的工艺流程如下:
)作电极材料。该类废旧电极(含杂质Al、石墨粉)回收处理和资源再利用的工艺流程如下:
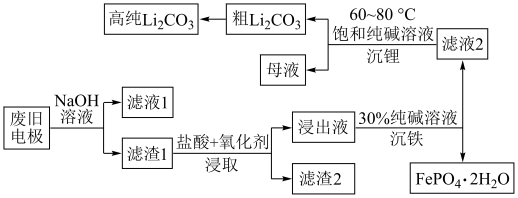
已知碳酸锂的溶解度与温度的变化曲线如下:
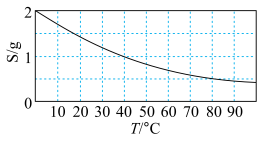
回答下列问题:
(1)滤液1中的溶质除了NaOH外还有___________ ;滤渣2的主要成分为___________ 。
(2)为确定“浸取”阶段应选择的氧化剂,用不同氧化剂分别进行浸取实验,使用相同原料,控制pH=1.5,浸取1.5h后,实验结果见下表:
实验2中溶液pH和氧化剂浓度控制不好会产生黄绿色气体,综合考虑 的浸出率、安全环保因素,选择的氧化剂最好是
的浸出率、安全环保因素,选择的氧化剂最好是___________ ,理由为___________ 。
(3)“沉铁”时,浸出液中加入30%的 溶液速度不能过快,并要及时搅拌,否则得到磷酸铁晶体中含有较多的红褐色物质,该红褐色物质是
溶液速度不能过快,并要及时搅拌,否则得到磷酸铁晶体中含有较多的红褐色物质,该红褐色物质是___________ ,产生的原因是___________ 。
(4)“沉锂”后获得粗碳酸锂的一系列操作为___________ 。
(5)粗碳酸锂中可能含有铁的化合物,请你设计检验杂质有铁的化合物的方案:___________ 。
(6)工业上将回收的 和
和 粉碎,再加入足量炭黑混合高温煅烧再生制备
粉碎,再加入足量炭黑混合高温煅烧再生制备 ,实现了物质的循环利用,请写出反应中生成
,实现了物质的循环利用,请写出反应中生成 的化学方程式
的化学方程式___________ 。
 )作电极材料。该类废旧电极(含杂质Al、石墨粉)回收处理和资源再利用的工艺流程如下:
)作电极材料。该类废旧电极(含杂质Al、石墨粉)回收处理和资源再利用的工艺流程如下:
已知碳酸锂的溶解度与温度的变化曲线如下:

回答下列问题:
(1)滤液1中的溶质除了NaOH外还有
(2)为确定“浸取”阶段应选择的氧化剂,用不同氧化剂分别进行浸取实验,使用相同原料,控制pH=1.5,浸取1.5h后,实验结果见下表:
| 序号 | 酸 | 氧化剂 | 浸出液 浓度/( 浓度/( ) ) | 滤渣中Li含量/% |
| 实验1 | HCl |  | 9.02 | 0.10 |
| 实验2 | HCl |  | 9.05 | 0.08 |
| 实验3 | HCl |  | 7.05 | 0.93 |
 的浸出率、安全环保因素,选择的氧化剂最好是
的浸出率、安全环保因素,选择的氧化剂最好是(3)“沉铁”时,浸出液中加入30%的
 溶液速度不能过快,并要及时搅拌,否则得到磷酸铁晶体中含有较多的红褐色物质,该红褐色物质是
溶液速度不能过快,并要及时搅拌,否则得到磷酸铁晶体中含有较多的红褐色物质,该红褐色物质是(4)“沉锂”后获得粗碳酸锂的一系列操作为
(5)粗碳酸锂中可能含有铁的化合物,请你设计检验杂质有铁的化合物的方案:
(6)工业上将回收的
 和
和 粉碎,再加入足量炭黑混合高温煅烧再生制备
粉碎,再加入足量炭黑混合高温煅烧再生制备 ,实现了物质的循环利用,请写出反应中生成
,实现了物质的循环利用,请写出反应中生成 的化学方程式
的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】下图是元素周期表的一部分,表中列出了①〜⑨种元素的位置,请根据要求回答问题。
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为________________ 。
(2)②与④形成的化合物的电子式可表示为_________________________________________ 。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是____________________ (填化学式)。
(4)写出⑤与氢氧化钠溶液反应的化学方程式:_____________________________________ 。
族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | VIA | ⅦA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ |
(2)②与④形成的化合物的电子式可表示为
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
(4)写出⑤与氢氧化钠溶液反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
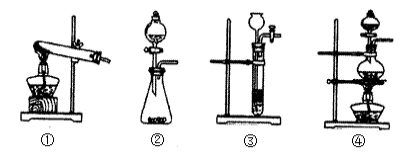
【推荐1】(1)已知草酸(H2C2O4)分解的化学方程式为:H2C2O4 CO↑+ CO2↑+ H2O,下列装置中,可用作草酸分解制取气体的是
CO↑+ CO2↑+ H2O,下列装置中,可用作草酸分解制取气体的是__________ (填序号)
(2)某实验小组为测定铁锈样品的组成(假定铁锈中只有Fe2O3·nH2O和Fe两种成分),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。

①、为得到干燥、纯净的CO气,洗气瓶A、B中盛放的试剂分别是_______ 、________ 。
②、在点燃C处酒精灯之前,应先持续通入一段时间的混合气体,其目的是______________________
③、准确称量样品的质量20.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为16.64g,D中浓硫酸增重1.44g,则n=______ 。
④、在本实验中,下列情况会使测定结果n偏大的是____ (填字母)
a.缺少装置A b.缺少装置B c.反应后固体是铁和少量Fe2O3·nH2O
 CO↑+ CO2↑+ H2O,下列装置中,可用作草酸分解制取气体的是
CO↑+ CO2↑+ H2O,下列装置中,可用作草酸分解制取气体的是
(2)某实验小组为测定铁锈样品的组成(假定铁锈中只有Fe2O3·nH2O和Fe两种成分),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。

①、为得到干燥、纯净的CO气,洗气瓶A、B中盛放的试剂分别是
②、在点燃C处酒精灯之前,应先持续通入一段时间的混合气体,其目的是
③、准确称量样品的质量20.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为16.64g,D中浓硫酸增重1.44g,则n=
④、在本实验中,下列情况会使测定结果n偏大的是
a.缺少装置A b.缺少装置B c.反应后固体是铁和少量Fe2O3·nH2O
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】已知甲、乙为常见的金属单质,A、B、C、D、E均为化合物,且A、B属于氧化物,它们之间有下图所示的转化关系,回答下列问题:

(1)反应①的化学方程式为____________ ,在实验室完成该反应时还需要的试剂有________ 、________ .
(2)C为________________ (填名称);上述反应属于氧化还原反应的是_____________ (填序号).
(3)反应⑤的离子方程式为_____________________ .
(4)D可以用来制造印刷电路板,也可以用来净水.为节约成本,工业上用NaClO3氧化E的酸性废液制得D,该反应的离子方程式为__________________________ .

(1)反应①的化学方程式为
(2)C为
(3)反应⑤的离子方程式为
(4)D可以用来制造印刷电路板,也可以用来净水.为节约成本,工业上用NaClO3氧化E的酸性废液制得D,该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】磁性材料A由两种元素组成,为探究其组成和性质,设计并完成如下实验:

(1) A的化学式为_____________________________________________________ 。
(2)用化学方程式表示气体C与氯水反应生成D的过程:___________________________________ 。
(3)B溶于盐酸后生成的物质F可用于净水,结合离子方程式说明其原因:__________________________ 。

(1) A的化学式为
(2)用化学方程式表示气体C与氯水反应生成D的过程:
(3)B溶于盐酸后生成的物质F可用于净水,结合离子方程式说明其原因:
您最近一年使用:0次



