A、B、C为为中学常见单质。通常状况下,A为固体,B为黄绿色气体,C为无色气体。D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种强酸,E为黑色固体,H在常温下为液体。它们之间转化关系如图所示(其中某些反应条件和部分反应物已略去)。请回答下列问题:
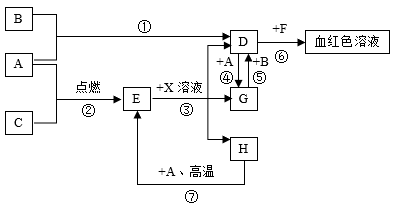
(1)写出下列物质的化学式:A___ 、X___ 。
(2)反应⑦的化学方程式是__ 。
(3)检验D的溶液中是否含有G中阳离子的方法是__ 。
(4)A的一种含氧酸根AO 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是__ 。
(5)在一定量A的氧化物中加入45mL4mol/L硫酸溶液恰好完全反应,所得溶液中A2+能恰好被标准状况下672mL氯气氧化。则该铁的氧化物的化学式为__ ,该氧化物与酸反应的离子方程式为__ 。

(1)写出下列物质的化学式:A
(2)反应⑦的化学方程式是
(3)检验D的溶液中是否含有G中阳离子的方法是
(4)A的一种含氧酸根AO
 具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是
具有强氧化性,在其钠盐溶液中加入稀硫酸,溶液变为黄色,并有无色气体产生。该反应的离子方程式是(5)在一定量A的氧化物中加入45mL4mol/L硫酸溶液恰好完全反应,所得溶液中A2+能恰好被标准状况下672mL氯气氧化。则该铁的氧化物的化学式为
更新时间:2020-12-23 13:15:41
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】某铜钴矿石主要含有CoOOH、CoCO3、Cu2(OH)2CO3和SiO2,其中还含有一定量的Fe2O3、MgO和CaO等。由该矿石制备Co2O3的部分工艺过程如下:
I.将粉碎的矿石用过量的稀H2SO4和Na2SO3溶液浸泡,过滤,分离除去沉淀a。
II.浸出液除去含铜的化合物后,向溶液中先加入NaClO3溶液,再加入一定浓度的Na2CO3溶液,过滤,分离除去沉淀b[主要成分是Na2Fe6(SO4)4(OH)12]。
III.向上述滤液中加入足量NaF溶液,过滤,分离除去沉淀c。
IV.III中滤液加入浓Na2CO3溶液,获得CoCO3沉淀。
V.将CoCO3溶解在盐酸中,再加入(NH4)2C2O4溶液,产生 CoC2O4·2H2O沉淀。分离出沉淀,将其在400℃~600℃ 煅烧,即得到Co2O3。
请回答:
(1)I 中,沉淀a的成分是_____ ,稀硫酸溶解CoCO3的化学方程式是_____ , 加入Na2SO3溶液的主要作用是_________ 。
(2)根据图1、图2分析:
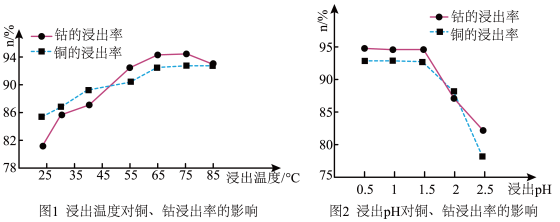
①矿石粉末浸泡的适宜条件应是:温度_____ 、pH_____ 。
②图2中铜、钴浸出率下降的可能原因是_____ 。
(3)II中,浸出液中的金属离子与NaClO3反应的离子方程式:ClO +
+_____ +_____ == Cl- +_____ + _____
(4)I中,检验铁元素完全除去的试剂是_____ ,实验现象是_____ 。
(5)I中,沉淀c的成分是CaF2、_____ (填化学式)。
(6)V中,加入Na2CO3的作用是_____ 。
(7)V中,分离出纯净的CoC2O4·2H2O的操作是_____ 。
I.将粉碎的矿石用过量的稀H2SO4和Na2SO3溶液浸泡,过滤,分离除去沉淀a。
II.浸出液除去含铜的化合物后,向溶液中先加入NaClO3溶液,再加入一定浓度的Na2CO3溶液,过滤,分离除去沉淀b[主要成分是Na2Fe6(SO4)4(OH)12]。
III.向上述滤液中加入足量NaF溶液,过滤,分离除去沉淀c。
IV.III中滤液加入浓Na2CO3溶液,获得CoCO3沉淀。
V.将CoCO3溶解在盐酸中,再加入(NH4)2C2O4溶液,产生 CoC2O4·2H2O沉淀。分离出沉淀,将其在400℃~600℃ 煅烧,即得到Co2O3。
请回答:
(1)I 中,沉淀a的成分是
(2)根据图1、图2分析:

①矿石粉末浸泡的适宜条件应是:温度
②图2中铜、钴浸出率下降的可能原因是
(3)II中,浸出液中的金属离子与NaClO3反应的离子方程式:ClO
 +
+(4)I中,检验铁元素完全除去的试剂是
(5)I中,沉淀c的成分是CaF2、
(6)V中,加入Na2CO3的作用是
(7)V中,分离出纯净的CoC2O4·2H2O的操作是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】已知A、B、C、D、E、F、G、H、I是中学化学中常见的九种化合物,其中B常温下为无色无味透明的液体,C焰色反应火焰呈黄色,E是红棕色的固体;X、Y是两种常见的单质,其中X常温常压下为气体。
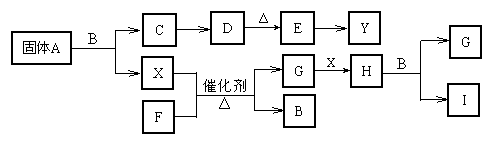
根据上面框图关系填空。
(1)A的化学式为________________ ,固体A的颜色为__________________ ;
(2)写出“X+F G+B”的化学反应方程式
G+B”的化学反应方程式________________________ ;
(3)写出“实验室中制取F气体”的化学反应方程式_____________________ ;
(4)写出“C→D”反应的离子方程式_________________________ ;
(5)写出“E+金属单质 Y+两性氧化物”的化学反应方程式
Y+两性氧化物”的化学反应方程式___________________ 。

根据上面框图关系填空。
(1)A的化学式为
(2)写出“X+F
 G+B”的化学反应方程式
G+B”的化学反应方程式(3)写出“实验室中制取F气体”的化学反应方程式
(4)写出“C→D”反应的离子方程式
(5)写出“E+金属单质
 Y+两性氧化物”的化学反应方程式
Y+两性氧化物”的化学反应方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】某课外学习小组对日常生活中不可缺少的调味品M进行探究。已知C可在D中燃烧发出苍白色火焰。M与其他物质的转化关系如下图所示(部分产物已略去):
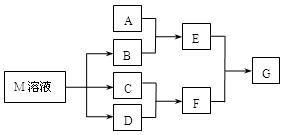
(1)写出用惰性电极电解M溶液的离子方程式__________ 。写出F的电子式___________ 。
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,E溶液与F溶液反应可以制备一种胶体,则E溶液的俗称是______________ 。
(3)若A是CO2气体,A与B溶液能够反应,反应后所得的溶液再与盐酸反应,如图所示,“则A与B溶液”反应后溶液中的溶质化学式为________ 。

(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是_______________ 。
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,向G溶液中加入苯酚溶液后显紫色,则由A转化成E的离子方程式是_____________
(6)若A是一种化肥。实验室可用A和B反应制取气体E,E与F、E与D相遇均冒白烟,且利用E与D的反应检验输送D的管道是否泄漏,写出E与D反应的化学方程式是________________ 。
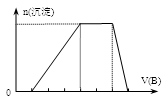
(7)若A是一种溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、CO32-、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图所示,由此可知,该溶液中肯定含有的离子及其浓度之比为_______________________ 。

(1)写出用惰性电极电解M溶液的离子方程式
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,E溶液与F溶液反应可以制备一种胶体,则E溶液的俗称是
(3)若A是CO2气体,A与B溶液能够反应,反应后所得的溶液再与盐酸反应,如图所示,“则A与B溶液”反应后溶液中的溶质化学式为

(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,向G溶液中加入苯酚溶液后显紫色,则由A转化成E的离子方程式是
(6)若A是一种化肥。实验室可用A和B反应制取气体E,E与F、E与D相遇均冒白烟,且利用E与D的反应检验输送D的管道是否泄漏,写出E与D反应的化学方程式是
(7)若A是一种溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、CO32-、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图所示,由此可知,该溶液中肯定含有的离子及其浓度之比为

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】A~H 是中学化学中常见的物质,转化关系如下图所示(部分反应物、反应条件和产物已略去)。A、H 是常见的金属单质,工业上常用电解法冶炼H;通常状况下B 为黄绿色气体;G 为红棕色固体;C、D、E、F、G 物种化合物含有同一种元素。

(1) B 的电子式为____________ 。
(2) 检验D中金属阳离子的实验方案是____________ 。
(3) 金属H 既能与强酸反应又能与强碱反应,其与NaOH 溶液反应的离子方程式为____________ 。
(4) E 在空气中转化成F 的化学方程式为____________ 。
(5) 理论上G 与H 反应生成1mol 固体A 放出428kJ 热量,G 与H 反应的热化学方程式为____________ 。
(6) 单质A 在氧气中的燃烧产物X 可用于去除地下水中的 具有放射性)。在酸性条件下,X 将TcO4-−转化为难溶于水的TcO2,同时得到F,该反应的离子方程式为
具有放射性)。在酸性条件下,X 将TcO4-−转化为难溶于水的TcO2,同时得到F,该反应的离子方程式为____________ 。

(1) B 的电子式为
(2) 检验D中金属阳离子的实验方案是
(3) 金属H 既能与强酸反应又能与强碱反应,其与NaOH 溶液反应的离子方程式为
(4) E 在空气中转化成F 的化学方程式为
(5) 理论上G 与H 反应生成1mol 固体A 放出428kJ 热量,G 与H 反应的热化学方程式为
(6) 单质A 在氧气中的燃烧产物X 可用于去除地下水中的
 具有放射性)。在酸性条件下,X 将TcO4-−转化为难溶于水的TcO2,同时得到F,该反应的离子方程式为
具有放射性)。在酸性条件下,X 将TcO4-−转化为难溶于水的TcO2,同时得到F,该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】高铁酸钾(K2FeO4)具有极强的氧化性和优良的絮凝功能,是一种绿色环保多功能型水处理剂。下图是生产高铁酸钾的一种工艺流程:
回答下列问题:
(1)写出①中发生反应的离子方程式:___________ 。
(2)②中加入NaOH固体的目的是___________(填字母序号)。
(3)完成④中反应的离子方程式:___________ ,氧化剂与氧化产物的物质的量之比为___________ ;若反应每生成lmol 转移电子的数目为:
转移电子的数目为:___________ 。
(4)从溶液II中得到K2FeO4晶体的操作是___________ 、洗涤、千燥。
(5)⑥中洗涤时,洗涤剂最好选用___________(填字母序号)。

| 溶解性 | 溶于水,微溶于浓KOH溶液,难溶于有机物 |
| 稳定性 | 温度为0~5℃或强碱性溶液中能稳定存在;酸性或中性溶液中放出O2 |
(1)写出①中发生反应的离子方程式:
(2)②中加入NaOH固体的目的是___________(填字母序号)。
| A.为后续反应提供碱性环境 |
| B.加入NaOH固体做氧化剂有利于除去NaCl |
| C.NaOH固体溶解时会放出较多的热量,有利于后续生成K2FeO4 |
| D.与溶液I中过量的Cl2继续反应,生成更多的NaClO |
(3)完成④中反应的离子方程式:
 转移电子的数目为:
转移电子的数目为:(4)从溶液II中得到K2FeO4晶体的操作是
(5)⑥中洗涤时,洗涤剂最好选用___________(填字母序号)。
| A.KOH溶液 | B.乙醇 | C.H2O | D.FeCl2溶液 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】硫酸亚铁铵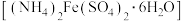 又名摩尔盐,是一种浅绿色晶体,易溶于水,不溶于乙醇,性质比一般亚铁盐稳定,接近100℃时易失去结晶水,是分析化学中的重要试剂。某研究性学习小组用下图所示的实验装置来制取摩尔盐。
又名摩尔盐,是一种浅绿色晶体,易溶于水,不溶于乙醇,性质比一般亚铁盐稳定,接近100℃时易失去结晶水,是分析化学中的重要试剂。某研究性学习小组用下图所示的实验装置来制取摩尔盐。

实验步骤如下:
①检查装置的气密性。
②往三颈烧瓶中依次加入过量的废铁屑(含杂质氧化铁和硫化亚铁)。
③关闭止水夹 、打开
、打开 ,打开分液漏斗的旋塞并控制好滴速。
,打开分液漏斗的旋塞并控制好滴速。
④把三颈烧瓶中的液体转移到装置乙中,当出现大量浅绿色晶体时,关闭分液漏斗的旋塞。
⑤将装置乙中所得晶体快速过滤、洗涤和干燥,得到产品。
回答下列问题:
(1)实验前需将废铁屑放入碳酸钠溶液中煮沸,倾倒出液体,用水洗净铁屑。以下仪器中完成该操作不需要的有___________ (填编号)。
①铁架台 ②玻璃棒 ③广口瓶 ④石棉网 ⑤烧杯 ⑥酒精灯 ⑦蒸发皿
(2)废铁屑中的杂质氧化铁和硫化亚铁无需在实验前除去,理由是___________ 、___________ 、___________ (用离子方程式表示)。
(3)步骤③向装置乙中通入氢气,通入氢气的目的是___________ ;装置丙中 溶液的作用是
溶液的作用是___________ 。
(4)通过调节 、
、 的开闭可实现步骤④中三颈烧瓶中液体自动转移至装置乙中,具体的实验操作为
的开闭可实现步骤④中三颈烧瓶中液体自动转移至装置乙中,具体的实验操作为___________ 。
(5)产品中 、
、 的检测。
的检测。
① 的定性检测:取少量产品于试管中,加水溶解,
的定性检测:取少量产品于试管中,加水溶解,___________ (填操作及现象),证明产品中含有 。
。
②测定产品中 的含量:称取10.0g产品,溶于水,加入足量NaOH溶液。过滤、洗涤、灼烧、冷却、称量。重复灼烧、冷却、称量,直到为止。称得最终固体质量为2.0g,则产品中
的含量:称取10.0g产品,溶于水,加入足量NaOH溶液。过滤、洗涤、灼烧、冷却、称量。重复灼烧、冷却、称量,直到为止。称得最终固体质量为2.0g,则产品中 的质量分数为
的质量分数为___________ 。(保留两位有效数字)
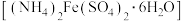 又名摩尔盐,是一种浅绿色晶体,易溶于水,不溶于乙醇,性质比一般亚铁盐稳定,接近100℃时易失去结晶水,是分析化学中的重要试剂。某研究性学习小组用下图所示的实验装置来制取摩尔盐。
又名摩尔盐,是一种浅绿色晶体,易溶于水,不溶于乙醇,性质比一般亚铁盐稳定,接近100℃时易失去结晶水,是分析化学中的重要试剂。某研究性学习小组用下图所示的实验装置来制取摩尔盐。
实验步骤如下:
①检查装置的气密性。
②往三颈烧瓶中依次加入过量的废铁屑(含杂质氧化铁和硫化亚铁)。
③关闭止水夹
 、打开
、打开 ,打开分液漏斗的旋塞并控制好滴速。
,打开分液漏斗的旋塞并控制好滴速。④把三颈烧瓶中的液体转移到装置乙中,当出现大量浅绿色晶体时,关闭分液漏斗的旋塞。
⑤将装置乙中所得晶体快速过滤、洗涤和干燥,得到产品。
回答下列问题:
(1)实验前需将废铁屑放入碳酸钠溶液中煮沸,倾倒出液体,用水洗净铁屑。以下仪器中完成该操作不需要的有
①铁架台 ②玻璃棒 ③广口瓶 ④石棉网 ⑤烧杯 ⑥酒精灯 ⑦蒸发皿
(2)废铁屑中的杂质氧化铁和硫化亚铁无需在实验前除去,理由是
(3)步骤③向装置乙中通入氢气,通入氢气的目的是
 溶液的作用是
溶液的作用是(4)通过调节
 、
、 的开闭可实现步骤④中三颈烧瓶中液体自动转移至装置乙中,具体的实验操作为
的开闭可实现步骤④中三颈烧瓶中液体自动转移至装置乙中,具体的实验操作为(5)产品中
 、
、 的检测。
的检测。①
 的定性检测:取少量产品于试管中,加水溶解,
的定性检测:取少量产品于试管中,加水溶解, 。
。②测定产品中
 的含量:称取10.0g产品,溶于水,加入足量NaOH溶液。过滤、洗涤、灼烧、冷却、称量。重复灼烧、冷却、称量,直到为止。称得最终固体质量为2.0g,则产品中
的含量:称取10.0g产品,溶于水,加入足量NaOH溶液。过滤、洗涤、灼烧、冷却、称量。重复灼烧、冷却、称量,直到为止。称得最终固体质量为2.0g,则产品中 的质量分数为
的质量分数为
您最近一年使用:0次



