借助现代科技手段研究化学反应原理能加深对知识本质的理解。
(1)下图是电解质导电性测试实验装置, 的电离方程式为
的电离方程式为___________ ,接通电源后,灯泡不亮,本质原因是___________ ,要使灯泡发光,可采取的操作是___________ ;将少量 溶液逐滴滴入A烧杯,除生成沉淀外,还可观察到的现象是
溶液逐滴滴入A烧杯,除生成沉淀外,还可观察到的现象是___________ 。

(2)下图是一套验证气体性质的实验装置,回答下列问题:
①实验室可用二氧化锰与浓盐酸制备氯气,反应的离子方程式为___________ ,如图所示,在A处通入干燥的氯气。一段时间后,观察到C处红布条褪色,则B处的开关应该处于___________ (填“关闭”或“打开”)状态。
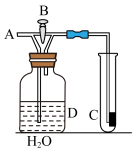
②实验后,利用数字传感器对D中的有色溶液进行光照实验分析,溶液光照实验前后比较,数目增加的离子有___________ (填化学式),对光照后溶液的叙述错误的是___________ (填标号)。
a.颜色变浅 b.漂白性增强 c.酸性增强 d.氧化性减弱
(1)下图是电解质导电性测试实验装置,
 的电离方程式为
的电离方程式为 溶液逐滴滴入A烧杯,除生成沉淀外,还可观察到的现象是
溶液逐滴滴入A烧杯,除生成沉淀外,还可观察到的现象是
(2)下图是一套验证气体性质的实验装置,回答下列问题:
①实验室可用二氧化锰与浓盐酸制备氯气,反应的离子方程式为

②实验后,利用数字传感器对D中的有色溶液进行光照实验分析,溶液光照实验前后比较,数目增加的离子有
a.颜色变浅 b.漂白性增强 c.酸性增强 d.氧化性减弱
更新时间:2023-11-07 11:19:08
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】现有10种物质:①铜线;②Cl2;③NH3;④HCl;⑤SO2;⑥稀盐酸;⑦乙醇(CH3CH2OH);⑧NaOH溶液;⑨BaSO4晶体;⑩熔融的NaCl。回答下列问题:
(1)上述物质属于如图所示化学概念交叉部分的有_______ (填序号)。
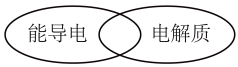
(2)向⑧中通入足量的⑤充分反应,产物为_______ (填化学式)。
(1)上述物质属于如图所示化学概念交叉部分的有

(2)向⑧中通入足量的⑤充分反应,产物为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求完成下列内容
(1)下列物质中:
①稀硫酸②液态氯化氢③熔融氯化钠④Fe⑤二氧化碳⑥乙醇⑦NH3·H2O⑧BaSO4
属于电解质的有(填序号,下同)_________ ;弱电解质有________ ;属于非电解质的有______ ;能直接导电的有_________ 。
(2)从上述物质中挑选合适物质,按照要求书写离子方程式(各写一个):
氧化还原反应:__________
酸碱中和反应:_______
(3)请写出下列物质的电离方程式。
①NaCl______________________
②NH3·H2O______________________
③Na2CO3______________________
④Ca(OH)2______________________
(4)请写出下列反应的离子方程式。
①盐酸去除铁锈(主要成分为氧化铁):_____________________
②澄清石灰水中通入CO2气体出现白色沉淀:_____________________
③胃舒平[主要成分为Al(OH)3]治疗胃酸过多:_____________________
④用适量澄清石灰水除去NaOH中的少量Na2CO3:_____________________
(1)下列物质中:
①稀硫酸②液态氯化氢③熔融氯化钠④Fe⑤二氧化碳⑥乙醇⑦NH3·H2O⑧BaSO4
属于电解质的有(填序号,下同)
(2)从上述物质中挑选合适物质,按照要求书写离子方程式(各写一个):
氧化还原反应:
酸碱中和反应:
(3)请写出下列物质的电离方程式。
①NaCl
②NH3·H2O
③Na2CO3
④Ca(OH)2
(4)请写出下列反应的离子方程式。
①盐酸去除铁锈(主要成分为氧化铁):
②澄清石灰水中通入CO2气体出现白色沉淀:
③胃舒平[主要成分为Al(OH)3]治疗胃酸过多:
④用适量澄清石灰水除去NaOH中的少量Na2CO3:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现有以下物质:① ②
② ③
③ ④
④ ⑤漂白粉 ⑥NaOH溶液 ⑦
⑤漂白粉 ⑥NaOH溶液 ⑦ 。回答下列问题:
。回答下列问题:
(1)上述物质中,属于酸性氧化物的有_______ (填标号,下同),属于电解质的有_______ ,⑤的有效成分为_______ (填化学式)。
(2)将②通入足量⑥中,发生反应的离子方程式为_______ 。
(3)向 ⑦的水溶液中逐滴滴加
⑦的水溶液中逐滴滴加 ④的水溶液至中性,此时溶液中的
④的水溶液至中性,此时溶液中的
_______  (假设混合后溶液体积的变化忽略不计)。
(假设混合后溶液体积的变化忽略不计)。
(4)向⑥中通入少量①,下图所示⑥溶液的电导率变化曲线合理的是_______(填标号)。
 ②
② ③
③ ④
④ ⑤漂白粉 ⑥NaOH溶液 ⑦
⑤漂白粉 ⑥NaOH溶液 ⑦ 。回答下列问题:
。回答下列问题:(1)上述物质中,属于酸性氧化物的有
(2)将②通入足量⑥中,发生反应的离子方程式为
(3)向
 ⑦的水溶液中逐滴滴加
⑦的水溶液中逐滴滴加 ④的水溶液至中性,此时溶液中的
④的水溶液至中性,此时溶液中的
 (假设混合后溶液体积的变化忽略不计)。
(假设混合后溶液体积的变化忽略不计)。(4)向⑥中通入少量①,下图所示⑥溶液的电导率变化曲线合理的是_______(填标号)。
A.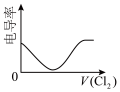 | B.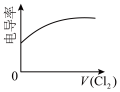 | C.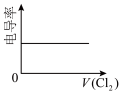 | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】实验室用如下装置制取干燥纯净的氯气,并用氯气进行实验。回答下列问题:
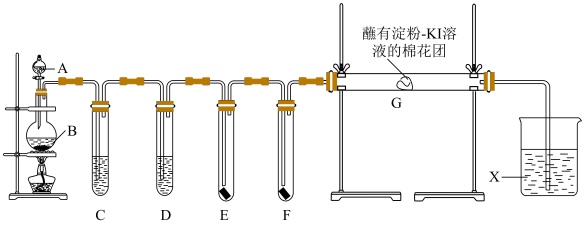
(1)装置连接完成后必须进行的操作是________ 。
(2)实验室制氯气的反应方程式为 ,其中参加反应的还原剂与氧化剂的数目之比为
,其中参加反应的还原剂与氧化剂的数目之比为_____ 。
(3)试管D中试剂为_______ 。
(4)E中为红色干布条,F中为红色湿布条,可观察到的现象是_______ 。对比E和F中现象的差异可得出的结论_______ 。
(5)装置G处棉花团变蓝,写出发生反应的化学方程式_______ (提示:淀粉遇I2变蓝)。

(1)装置连接完成后必须进行的操作是
(2)实验室制氯气的反应方程式为
 ,其中参加反应的还原剂与氧化剂的数目之比为
,其中参加反应的还原剂与氧化剂的数目之比为(3)试管D中试剂为
(4)E中为红色干布条,F中为红色湿布条,可观察到的现象是
(5)装置G处棉花团变蓝,写出发生反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】自来水的消毒关系到每个人的饮水安全问题。很早以前自来水厂常用氯气作自来水的消毒剂,后来发现用氯气有不妥之处,改用了ClO2或者Na2FeO4作消毒剂。
(1)请写出氯原子的结构示意图:_______ 。
(2)84消毒液(主要成分是NaClO和NaCl)和沽厕灵(主要成分是盐酸)混用会产生有毒气体,试写出反应的离子方程式:_______ 。
(3)高铁酸钠是用次氯酸钠和氢氧化铁在一定条件下制备的,请配平制备的反应方程式并用单线桥标出电子转移的方向和数目:___________
_______NaC1O+_______Fe(OH)3+_______=_______ Na2FeO4+NaCl+_______H2O。
氧化剂是_______ ,_______ 被氧化。
(4)①高铁酸钠被用作消毒剂是因为具有_______ 性,其产物是三价铁, 水解生成的Fe(OH)3分散系属于
水解生成的Fe(OH)3分散系属于_______ (填“浊液”、“胶体”或“溶液”),能够吸附水中带负电荷的固体颗粒物,达到净水的目的。
②ClO-在酸性环境下的氧化性更强,某同学准备用含次氯酸的溶液和硫酸铁去制备高铁酸或者高铁酸盐,结果失败了,下列判断可能正确的是_______ 。
A.碱性环境下三价铁的还原性更强
B.酸性环境下高铁酸根离子的氧化性太强
C.碱性环境下高铁酸钠的氧化性不强
(1)请写出氯原子的结构示意图:
(2)84消毒液(主要成分是NaClO和NaCl)和沽厕灵(主要成分是盐酸)混用会产生有毒气体,试写出反应的离子方程式:
(3)高铁酸钠是用次氯酸钠和氢氧化铁在一定条件下制备的,请配平制备的反应方程式并用单线桥标出电子转移的方向和数目:
_______NaC1O+_______Fe(OH)3+_______=_______ Na2FeO4+NaCl+_______H2O。
氧化剂是
(4)①高铁酸钠被用作消毒剂是因为具有
 水解生成的Fe(OH)3分散系属于
水解生成的Fe(OH)3分散系属于②ClO-在酸性环境下的氧化性更强,某同学准备用含次氯酸的溶液和硫酸铁去制备高铁酸或者高铁酸盐,结果失败了,下列判断可能正确的是
A.碱性环境下三价铁的还原性更强
B.酸性环境下高铁酸根离子的氧化性太强
C.碱性环境下高铁酸钠的氧化性不强
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】一场突如其来的新冠肺炎疫情,给人们的生活带来了巨大的冲击,在疫情期间外出需戴好口罩,返家后立即杀菌消毒。含氯消毒剂在日常生产生活中有着广泛的用途。
(1)实验室除了可以用 和浓盐酸制氯气外,还可以利用如下反应制取氯气:
和浓盐酸制氯气外,还可以利用如下反应制取氯气: 。若要制取标准状况下3.36L氯气,则发生反应的HCl的质量为
。若要制取标准状况下3.36L氯气,则发生反应的HCl的质量为_______ g,其中被氧化的HCl的物质的量为_______ mol,反应过程中转移的电子数为_______  。
。
(2)“84”消毒液(有效成分为NaClO)在抗击新冠肺炎疫情战役中发挥了重要的作用。常温下,可利用氯气与烧碱溶液反应制得“84”消毒液,在使用前将“84”消毒液的稀释液放置在空气中一段时间,其漂白效果更好,原因为_______ (用离子方程式表示,已知通常情况下,弱酸不能制强酸,酸性: )。
)。
(3)二氧化氯( )是一种黄绿色的气体。可用作饮用水的消毒杀菌处理剂,是国际上公认的安全、低毒的绿色消毒剂。实验室可用
)是一种黄绿色的气体。可用作饮用水的消毒杀菌处理剂,是国际上公认的安全、低毒的绿色消毒剂。实验室可用 和浓盐酸在一定温度下反应制得:
和浓盐酸在一定温度下反应制得: 。
。
①该反应的氧化产物为_______ (填化学式)。
②在该反应中浓盐酸表现出来的性质是_______ (填标号)。
A.还原性 B.氧化性 C.酸性
③ 、
、 、
、 (还原产物为
(还原产物为 )、
)、 等物质常被用作消毒剂。等物质的量的上述物质消毒的效率(以1mol物质的得电子数来衡量)最高的是
等物质常被用作消毒剂。等物质的量的上述物质消毒的效率(以1mol物质的得电子数来衡量)最高的是_______ (填标号)。
A. B.
B.  C.
C. D.
D.
(1)实验室除了可以用
 和浓盐酸制氯气外,还可以利用如下反应制取氯气:
和浓盐酸制氯气外,还可以利用如下反应制取氯气: 。若要制取标准状况下3.36L氯气,则发生反应的HCl的质量为
。若要制取标准状况下3.36L氯气,则发生反应的HCl的质量为 。
。(2)“84”消毒液(有效成分为NaClO)在抗击新冠肺炎疫情战役中发挥了重要的作用。常温下,可利用氯气与烧碱溶液反应制得“84”消毒液,在使用前将“84”消毒液的稀释液放置在空气中一段时间,其漂白效果更好,原因为
 )。
)。(3)二氧化氯(
 )是一种黄绿色的气体。可用作饮用水的消毒杀菌处理剂,是国际上公认的安全、低毒的绿色消毒剂。实验室可用
)是一种黄绿色的气体。可用作饮用水的消毒杀菌处理剂,是国际上公认的安全、低毒的绿色消毒剂。实验室可用 和浓盐酸在一定温度下反应制得:
和浓盐酸在一定温度下反应制得: 。
。①该反应的氧化产物为
②在该反应中浓盐酸表现出来的性质是
A.还原性 B.氧化性 C.酸性
③
 、
、 、
、 (还原产物为
(还原产物为 )、
)、 等物质常被用作消毒剂。等物质的量的上述物质消毒的效率(以1mol物质的得电子数来衡量)最高的是
等物质常被用作消毒剂。等物质的量的上述物质消毒的效率(以1mol物质的得电子数来衡量)最高的是A.
 B.
B.  C.
C. D.
D.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】完成下列小题。
(1)写出实验室制备氯气的化学方程式___________ 。
(2)在标准状况下,用干燥烧瓶收集一瓶氯化氢气体倒置于盛水的水槽中时,水充满烧瓶(假设烧瓶里溶液不扩散出水槽),烧瓶里盐酸的密度为 。该盐酸的物质的量浓度
。该盐酸的物质的量浓度___________ 、溶质的质量分数为___________ 。
(3)请用单线桥法 标出以下反应电子转移方向和数目:___________ 。
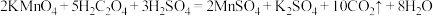
(4)高铁酸钠 是一种新型绿色消毒剂,工业上制备高铁酸钠有多种方法,其中一种是用
是一种新型绿色消毒剂,工业上制备高铁酸钠有多种方法,其中一种是用 在强碱性条件下氧化
在强碱性条件下氧化 ,写出该反应的
,写出该反应的离子方程式 ___________ 。
(1)写出实验室制备氯气的化学方程式
(2)在标准状况下,用干燥烧瓶收集一瓶氯化氢气体倒置于盛水的水槽中时,水充满烧瓶(假设烧瓶里溶液不扩散出水槽),烧瓶里盐酸的密度为
 。该盐酸的物质的量浓度
。该盐酸的物质的量浓度(3)请用
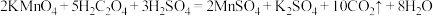
(4)高铁酸钠
 是一种新型绿色消毒剂,工业上制备高铁酸钠有多种方法,其中一种是用
是一种新型绿色消毒剂,工业上制备高铁酸钠有多种方法,其中一种是用 在强碱性条件下氧化
在强碱性条件下氧化 ,写出该反应的
,写出该反应的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】工厂里常用浓氨水检验氯气管道是否漏气,其反应方程式为: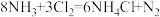 ,回答下列问题:
,回答下列问题:
(1)实验室用二氧化锰为原料制取Cl2,该反应的离子方程式为_____ ,干燥C12常用装有_____ 的洗气瓶。
(2)实验室用下列两种方法制氯气:①用含HCl146g的浓盐酸与足量的MnO2反应;②用87gMnO2与足量浓盐酸反应。所得的氯气_____。
(3)在 中
中
①还原剂是_____ ,还原产物是_____ (都填化学式)。
②氧化剂与还原剂的分子数之比为_____ ,当有4个NH3参加反应时,转移的电子个数为_____ 。
③当生成28gN2时,被氧化的物质为_____ g。
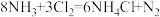 ,回答下列问题:
,回答下列问题:(1)实验室用二氧化锰为原料制取Cl2,该反应的离子方程式为
(2)实验室用下列两种方法制氯气:①用含HCl146g的浓盐酸与足量的MnO2反应;②用87gMnO2与足量浓盐酸反应。所得的氯气_____。
| A.①比②多 | B.②比①多 | C.一样多 | D.无法比较 |
 中
中①还原剂是
②氧化剂与还原剂的分子数之比为
③当生成28gN2时,被氧化的物质为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】分类是认识和研究物质及其变化的一种常用的科学方法。依据物质类别和元素价态可以对物质的性质进行解释和预测。以下为含氯物质的价类二维图,请回答下列问题:
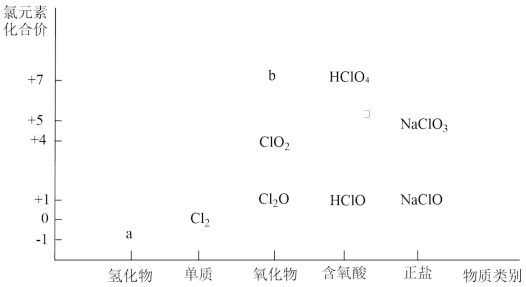
(1)a物质的化学式为_______ ,b属于_______ (填“酸性”或“碱性”)氧化物。
(2)用 消毒水时,
消毒水时, 还可将水中的
还可将水中的 转化为
转化为 ,
, 再水解生成
再水解生成 胶体,说明
胶体,说明 具有
具有_______ 性,在此水处理过程中生成的 胶体有
胶体有_______ 作用。
(3)工业上可以用反应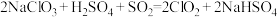 制备
制备 ,用单线桥法标出电子转移的数目和方向。
,用单线桥法标出电子转移的数目和方向。_______
(4)实验室制取氯气时,下列装置能达到相应实验目的是_______ 。
写出实验室用二氧化锰与浓盐酸反应制取氯气的离子方程式:_______ 。
(5)阅读资料,回答相关问题。
① 与
与 溶液反应的化学方程式是
溶液反应的化学方程式是_______ 。
②“84”消毒液不能与洁厕灵(含盐酸)混用,混用会产生氯气,写出反应的离子方程式:_______ 。

(1)a物质的化学式为
(2)用
 消毒水时,
消毒水时, 还可将水中的
还可将水中的 转化为
转化为 ,
, 再水解生成
再水解生成 胶体,说明
胶体,说明 具有
具有 胶体有
胶体有(3)工业上可以用反应
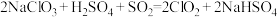 制备
制备 ,用单线桥法标出电子转移的数目和方向。
,用单线桥法标出电子转移的数目和方向。(4)实验室制取氯气时,下列装置能达到相应实验目的是
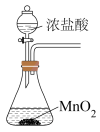 |  | 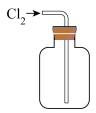 |  |
A.制备 | B.除去 中的 中的 | C.收集 | D.尾气处理 |
(5)阅读资料,回答相关问题。
资料:人们常用“84”消毒液进行消毒。“84”消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒液。“84”消毒液呈无色或淡黄色,可由 与 与 溶液反应制得,其主要成分为 溶液反应制得,其主要成分为 、 、 。 。 |
 与
与 溶液反应的化学方程式是
溶液反应的化学方程式是②“84”消毒液不能与洁厕灵(含盐酸)混用,混用会产生氯气,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)氢气在氯气中燃烧的化学方程式为___ 。
(2)容量瓶上需标有刻度线以下项中的___ 。(填序号)
①温度②浓度③容量④压强
(3)铁跟盐酸反应的离子方程式为___ ,反应后的溶液分装在2支试管里,往一支试管里滴加适量氯水后溶液变成___ 色,再滴入几滴KSCN溶液,溶液变成___ 色。往另一支试管里滴入过量的NaOH溶液,反应的现象是___ 。
(2)容量瓶上需标有刻度线以下项中的
①温度②浓度③容量④压强
(3)铁跟盐酸反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】小王同学在一次实验中发现:把新制氯水逐滴加到含有酚酞的氢氧化钠溶液中,当加到最后一滴时溶液的红色突然消失。
(1)将氯气通入水中发生反应的化学方程式为_______ 。
(2)氯水的颜色呈浅黄绿色,说明氯水中含有_______ ;向氯水中滴加AgNO3溶液,反应的离子方程式是_______ 。
(3)探究“溶液的红色突然消失”的原因:
①猜想
a:是氯水中的盐酸和次氯酸中和了 NaOH,使酚酞由红色变成无色;
b:是_______ 。
②设计实验:往已褪色的溶液中连续滴加 NaOH溶液至过量,若现象为_______ ,则证明“猜想 a”正确;若现象为_______ ,则证明“猜想 b”正确。
(1)将氯气通入水中发生反应的化学方程式为
(2)氯水的颜色呈浅黄绿色,说明氯水中含有
(3)探究“溶液的红色突然消失”的原因:
①猜想
a:是氯水中的盐酸和次氯酸中和了 NaOH,使酚酞由红色变成无色;
b:是
②设计实验:往已褪色的溶液中连续滴加 NaOH溶液至过量,若现象为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】从元素化合价和物质类别两个角度学习、研究物质的性质,是一种行之有效的方法。
(1)下图为氯及其化合物的“价类”二维图。图中A的类别为______ ;B的名称为______ 。

(2)已知高氯酸(HClO4)是一元强酸,写出高氯酸溶液与氢氧化钠溶液反应的离子方程式____ 。
(3)某同学研究HCl性质,进行如下预测:
①从物质类别上看,HCl属于酸,能与大理石反应,相应的离子方程式为__________ ;
②从化合价角度看,HCl具有__________ 性,能与__________ 发生反应(填标号)。
A.NaClO B.Fe C.KMnO4 D.NaOH
(4)某同学用强光照射氯水,同时使用数据采集器采集数据如图。

光照新制氯水,发生反应的化学方程式为_________ ;该同学采集的数据是__________ (填标号)。
A.氯水的pH B.氯离子的浓度 C.溶液的电导率 D.氧气的体积分数
(1)下图为氯及其化合物的“价类”二维图。图中A的类别为

(2)已知高氯酸(HClO4)是一元强酸,写出高氯酸溶液与氢氧化钠溶液反应的离子方程式
(3)某同学研究HCl性质,进行如下预测:
①从物质类别上看,HCl属于酸,能与大理石反应,相应的离子方程式为
②从化合价角度看,HCl具有
A.NaClO B.Fe C.KMnO4 D.NaOH
(4)某同学用强光照射氯水,同时使用数据采集器采集数据如图。

光照新制氯水,发生反应的化学方程式为
A.氯水的pH B.氯离子的浓度 C.溶液的电导率 D.氧气的体积分数
您最近一年使用:0次



