1 . 实验室用 与浓盐酸共热制备
与浓盐酸共热制备 ,反应如下:
,反应如下:
(1)该反应中被氧化的元素是___________ ,还原产物是___________ ;
(2)用单线桥标明电子转移的方向与数目___________ 。
(3)该反应中,氧化剂与还原剂的物质的量之比为___________ (前者比后者);盐酸在反应中表现出来的性质是___________ 。
(4)当生成标准状况下 时,转移的电子数目为
时,转移的电子数目为___________ ,被氧化的还原剂的物质的量为___________ 。
(5)也可以用 和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用
和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用 的原因:
的原因:___________ 。
(6)举例说明氯气的氧化性比硫单质强,___________ 。
 与浓盐酸共热制备
与浓盐酸共热制备 ,反应如下:
,反应如下:
(1)该反应中被氧化的元素是
(2)用单线桥标明电子转移的方向与数目
(3)该反应中,氧化剂与还原剂的物质的量之比为
(4)当生成标准状况下
 时,转移的电子数目为
时,转移的电子数目为(5)也可以用
 和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用
和浓盐酸反应,在常温下制氯气,请从化合价的角度分析,能够使用 的原因:
的原因:(6)举例说明氯气的氧化性比硫单质强,
您最近一年使用:0次
解题方法
2 . 自然界中的硫循环和氮循环。人类的文明历程与自然环境的变化密切相关。自然界中,陆地、海洋、大气中的硫元素和氮元素,通过各种循环建立起生态平衡。
(1)陆地和海洋中的硫通过有机物分解释放H2S或可溶硫酸盐、火山喷发(H2S、SO 、SO2)等过程使硫变成可移动的简单化合物进入大气。在火山气体中的硫蒸汽到达地面后会在喷口附近凝结,形成硫黄。火山喷发中形成的H2S和SO2也会发生反应,形成硫。请写出该反应的化学方程式
、SO2)等过程使硫变成可移动的简单化合物进入大气。在火山气体中的硫蒸汽到达地面后会在喷口附近凝结,形成硫黄。火山喷发中形成的H2S和SO2也会发生反应,形成硫。请写出该反应的化学方程式______ 。该反应的氧化剂是______ ,氧化产物和还原产物的比例为______ 。
(2)大气中的水能结合SO2,被氧化后形成硫酸,随降水落入土壤或水体中,以硫酸盐的形式被植物的根系吸收,转变成蛋白质等有机物。SO2与水反应的方程式为:______ 。
(3)工业革命以来,过度的资源开发和利用,打破了自然界的平衡。SO2的过渡排放会引起酸雨等一系列环境问题。下列措施中可用于减少SO2排放量,且经济可行的是______ 。
氮循环是指氮在自然界中的循环转化过程,是生物圈内基本的物质循环之一、大气中的氮经固氮作用进入土壤,最终又在微生物的参与下返回大气中,如此反复循环,以至无穷。
(4)使空气中的氮进入土壤的方法称为氮的固定。下列不属于氮的固定的是______ 。
人们对植物、水体施加氮肥的过程也是氮进入土壤、水体的途径之一、然而,铵态氮肥的施肥过度会造成水体的富营养化。研究发现,可以用化学方法和生物方法去除氨氮。
(5)化学方法一般用次氯酸钠氧化。次氯酸钠可以和水中溶解的氨气反应得到无毒无害物质,其离子方程式为:3ClO-+2NH3=3Cl-+N2↑+3H2O。氨氮脱除率受溶液pH和 的比例影响。表中是不同pH下的氨氮脱除率:
的比例影响。表中是不同pH下的氨氮脱除率:

由上述信息判断,反应的最佳pH范围是______ ,最佳投料比是______ 。
(6)生物方法是O2在硝化细菌作用下,将水体中的NH 转化为NO
转化为NO 。之后,在氧气较少的环境下,NO
。之后,在氧气较少的环境下,NO 又可以在反硝化细菌的作用下与NH
又可以在反硝化细菌的作用下与NH 反应,使氮以N2形式放出。生物方法相对于化学方法的优势是
反应,使氮以N2形式放出。生物方法相对于化学方法的优势是______ 。
(1)陆地和海洋中的硫通过有机物分解释放H2S或可溶硫酸盐、火山喷发(H2S、SO
 、SO2)等过程使硫变成可移动的简单化合物进入大气。在火山气体中的硫蒸汽到达地面后会在喷口附近凝结,形成硫黄。火山喷发中形成的H2S和SO2也会发生反应,形成硫。请写出该反应的化学方程式
、SO2)等过程使硫变成可移动的简单化合物进入大气。在火山气体中的硫蒸汽到达地面后会在喷口附近凝结,形成硫黄。火山喷发中形成的H2S和SO2也会发生反应,形成硫。请写出该反应的化学方程式(2)大气中的水能结合SO2,被氧化后形成硫酸,随降水落入土壤或水体中,以硫酸盐的形式被植物的根系吸收,转变成蛋白质等有机物。SO2与水反应的方程式为:
(3)工业革命以来,过度的资源开发和利用,打破了自然界的平衡。SO2的过渡排放会引起酸雨等一系列环境问题。下列措施中可用于减少SO2排放量,且经济可行的是
| A.用天然气代替煤炭做民用燃料 | B.将工厂的烟囱造高 |
| C.使用CS2萃取煤炭中的硫 | D.工业尾气经碱液处理后再排放 |
氮循环是指氮在自然界中的循环转化过程,是生物圈内基本的物质循环之一、大气中的氮经固氮作用进入土壤,最终又在微生物的参与下返回大气中,如此反复循环,以至无穷。
(4)使空气中的氮进入土壤的方法称为氮的固定。下列不属于氮的固定的是
A.N2+O2 2NO 2NO | B.2NO+O2=2NO2 |
C.N2+3H2 2NH3 2NH3 | D.3Mg+N2 Mg3N2 Mg3N2 |
人们对植物、水体施加氮肥的过程也是氮进入土壤、水体的途径之一、然而,铵态氮肥的施肥过度会造成水体的富营养化。研究发现,可以用化学方法和生物方法去除氨氮。
(5)化学方法一般用次氯酸钠氧化。次氯酸钠可以和水中溶解的氨气反应得到无毒无害物质,其离子方程式为:3ClO-+2NH3=3Cl-+N2↑+3H2O。氨氮脱除率受溶液pH和
 的比例影响。表中是不同pH下的氨氮脱除率:
的比例影响。表中是不同pH下的氨氮脱除率:
| pH | 氨氮脱除率 |
| 5.8 | 51.1% |
| 6.9 | 61.3% |
| 7.7 | 65.8% |
| 8.8 | 61.7% |
| 9.3 | 48.7% |
(6)生物方法是O2在硝化细菌作用下,将水体中的NH
 转化为NO
转化为NO 。之后,在氧气较少的环境下,NO
。之后,在氧气较少的环境下,NO 又可以在反硝化细菌的作用下与NH
又可以在反硝化细菌的作用下与NH 反应,使氮以N2形式放出。生物方法相对于化学方法的优势是
反应,使氮以N2形式放出。生物方法相对于化学方法的优势是
您最近一年使用:0次
名校
3 . 实验室制备 的原理是用亚氯酸钠固体与氯气反应:
的原理是用亚氯酸钠固体与氯气反应: 配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目_______ 。

 与
与 用作消毒剂时均被还原为
用作消毒剂时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的_______ 倍(保留小数点后2位,消毒能力可以用氧化剂转移电子数来衡量)。
 的原理是用亚氯酸钠固体与氯气反应:
的原理是用亚氯酸钠固体与氯气反应: 配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
 与
与 用作消毒剂时均被还原为
用作消毒剂时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的
您最近一年使用:0次
名校
4 . 氯气和一些含氯化合物常用作消毒剂。 制备流程可表述如下:
制备流程可表述如下:
① 与
与 作用生成
作用生成 ;
;
②在75℃左右, 进一步完全转化为
进一步完全转化为 ,
,
此步方程式为 (未配平)
(未配平)
(1)写出①生成 的化学方程式
的化学方程式_______ 。漂粉精久置空气中会变质,在变质过程中不会涉及的性质是_______
A. 的酸性 B.HClO的不稳定性 C.HClO的弱酸性 D.HClO的漂白性
的酸性 B.HClO的不稳定性 C.HClO的弱酸性 D.HClO的漂白性
(2)若某学生在上述流程中发现某含钙离子盐的化学式为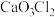 ,试根据盐的定义写出构成这种盐的酸根离子的符号
,试根据盐的定义写出构成这种盐的酸根离子的符号_______ 。
(3)若每一步反应均完全进行,且没有其他副产物,最终 与
与 的物质的量之比为
的物质的量之比为_______ 。
 制备流程可表述如下:
制备流程可表述如下:①
 与
与 作用生成
作用生成 ;
;②在75℃左右,
 进一步完全转化为
进一步完全转化为 ,
,此步方程式为
 (未配平)
(未配平)(1)写出①生成
 的化学方程式
的化学方程式A.
 的酸性 B.HClO的不稳定性 C.HClO的弱酸性 D.HClO的漂白性
的酸性 B.HClO的不稳定性 C.HClO的弱酸性 D.HClO的漂白性(2)若某学生在上述流程中发现某含钙离子盐的化学式为
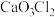 ,试根据盐的定义写出构成这种盐的酸根离子的符号
,试根据盐的定义写出构成这种盐的酸根离子的符号(3)若每一步反应均完全进行,且没有其他副产物,最终
 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
名校
解题方法
5 . 物质的类别和核心元素的化合价是研究物质性质的两个基本视角。请根据如图所示,回答下列问题:

(1)X的化学式为___________ ,W的浓溶液可以干燥氢气,体现其___________ 性。
(2)Y是形成酸雨的主要物质之一,含有Y的尾气可以用过量的NaOH溶液吸收,发生反应的化学方程式为___________ ;另一类硝酸型酸雨主要由人类活动(汽车尾气)产生的 造成的,写出
造成的,写出 与水反应的化学方程式为
与水反应的化学方程式为___________ 。
(3)硫酸钠和Z混和溶液,检验存在硫酸根离子的方法是:___________ 。
(4)火药是中国的“四大发明”之一,硫磺是黑火药的成分之一、黑火药在发生爆炸时,发生如下的反应: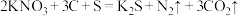 ,生成物中属于非电解质的是
,生成物中属于非电解质的是___________ 。每生成1mol氧化产物,消耗 的质量是
的质量是___________ 克。

(1)X的化学式为
(2)Y是形成酸雨的主要物质之一,含有Y的尾气可以用过量的NaOH溶液吸收,发生反应的化学方程式为
 造成的,写出
造成的,写出 与水反应的化学方程式为
与水反应的化学方程式为(3)硫酸钠和Z混和溶液,检验存在硫酸根离子的方法是:
(4)火药是中国的“四大发明”之一,硫磺是黑火药的成分之一、黑火药在发生爆炸时,发生如下的反应:
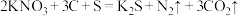 ,生成物中属于非电解质的是
,生成物中属于非电解质的是 的质量是
的质量是
您最近一年使用:0次
6 . 关于反应 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A. 中H元素被氧化 中H元素被氧化 | B. 在反应过程中失去电子 在反应过程中失去电子 |
| C.还原剂与氧化剂的质量之比为34∶69 | D.氧化产物与还原产物的质量之比为3∶4 |
您最近一年使用:0次
名校
7 . 100mL 稀硝酸,恰好使铜和氧化铜完全溶解,同时收集到标准状况下NO2.24L。
稀硝酸,恰好使铜和氧化铜完全溶解,同时收集到标准状况下NO2.24L。
请回答以下问题:
(1)铜和稀硝酸反应中氧化剂和还原剂的物质的量之比为___________ 。
(2)原混合物中铜的物质的量为___________ ,氧化铜的质量为___________ (写出计算过程)。
 稀硝酸,恰好使铜和氧化铜完全溶解,同时收集到标准状况下NO2.24L。
稀硝酸,恰好使铜和氧化铜完全溶解,同时收集到标准状况下NO2.24L。请回答以下问题:
(1)铜和稀硝酸反应中氧化剂和还原剂的物质的量之比为
(2)原混合物中铜的物质的量为
您最近一年使用:0次
名校
8 . 下列反应中,氧化剂与还原剂化学计量数为1:2的是
| A.Fe+2HCl=FeCl2+H2↑ |
| B.2HCl+Ca(ClO)2=2HClO+CaCl2 |
| C.I2+2NaClO3=2NaIO3+Cl2↑ |
D.4HCl(浓)+MnO2 MnCl2+Cl2↑+2H2O MnCl2+Cl2↑+2H2O |
您最近一年使用:0次
9 . Ⅰ.完成下列问题
(1)我国宋代《梦溪笔谈》中记叙了胆矾和铜的炼制过程:“信州铅山县有苦泉,煮之则得胆矾。熬胆矾铁釜,人之亦化为铜。”该炼制过程中没有涉及到的变化是_______
(2)为实现下列物质之间的转化,需要加入还原剂才能实现的是_______
(3)硫单质在反应3S+6KOH 2K2S+K2SO3+3H2O中的变化是_______
2K2S+K2SO3+3H2O中的变化是_______
(4)3Cl2+6KOH(浓) KClO3+5KCl+3H2O中,氧化剂与还原剂物质的量之比为_______
KClO3+5KCl+3H2O中,氧化剂与还原剂物质的量之比为_______
(5)神舟十三号载人飞船的燃料可为肼(N2H4),发射时发生的反应为:2N2H4+N2O4=3N2+4H2O,下列说法正确的是
(6)某溶液中可能含有H+、Fe2+、Na+、CO 、SO
、SO 、NO
、NO ,若H+和NO
,若H+和NO 的浓度分别为0.1mol·L-1、0.12mol·L-1,则溶液中一定大量存在_______
的浓度分别为0.1mol·L-1、0.12mol·L-1,则溶液中一定大量存在_______
Ⅱ.实验室用100mL浓盐酸跟足量的KClO3固体共热制取Cl2,反应的化学方程式为:KClO3+6HCl(浓) KCl+3Cl2↑+3H2O。
KCl+3Cl2↑+3H2O。
(7)用单线桥标出电子转移的方向和数目___________ 。
(8)此反应中,氧化剂为:___________ (填化学式),被氧化的元素为___________ 。
(9)此反应中,氧化产物与还原产物的质量之比为:___________ 。
(10)当有3.36L(STP)Cl2生成时,反应中转移的电子数为___________ 个。
(1)我国宋代《梦溪笔谈》中记叙了胆矾和铜的炼制过程:“信州铅山县有苦泉,煮之则得胆矾。熬胆矾铁釜,人之亦化为铜。”该炼制过程中没有涉及到的变化是_______
| A.复分解反应 | B.离子反应 | C.置换反应 | D.蒸发结晶 |
| A.KClO3→KCl | B.CuO→Cu | C.Cu→Cu(NO3)2 | D.HCO →CO2 →CO2 |
 2K2S+K2SO3+3H2O中的变化是_______
2K2S+K2SO3+3H2O中的变化是_______| A.被氧化 | B.被还原 |
| C.既被氧化又被还原 | D.既未被氧化又未被还原 |
 KClO3+5KCl+3H2O中,氧化剂与还原剂物质的量之比为_______
KClO3+5KCl+3H2O中,氧化剂与还原剂物质的量之比为_______| A.1:5 | B.4:1 | C.5:1 | D.1:4 |
| A.肼在反应中作氧化剂 |
| B.反应中每生成1个H2O转移4个电子 |
| C.N2O4在反应中被氧化 |
| D.氧化产物与还原产物的物质的量之比是2:1 |
 、SO
、SO 、NO
、NO ,若H+和NO
,若H+和NO 的浓度分别为0.1mol·L-1、0.12mol·L-1,则溶液中一定大量存在_______
的浓度分别为0.1mol·L-1、0.12mol·L-1,则溶液中一定大量存在_______| A.Fe2+ | B.Na+ | C.CO | D.SO |
Ⅱ.实验室用100mL浓盐酸跟足量的KClO3固体共热制取Cl2,反应的化学方程式为:KClO3+6HCl(浓)
 KCl+3Cl2↑+3H2O。
KCl+3Cl2↑+3H2O。(7)用单线桥标出电子转移的方向和数目
(8)此反应中,氧化剂为:
(9)此反应中,氧化产物与还原产物的质量之比为:
(10)当有3.36L(STP)Cl2生成时,反应中转移的电子数为
您最近一年使用:0次
名校
10 . 回答下列问题。
(1)电解氧化吸收法可将废气中的 NOx转变为NO 。电解NaCl溶液时,溶液中相关成分的浓度变化与电流强度的关系如下图所示。
。电解NaCl溶液时,溶液中相关成分的浓度变化与电流强度的关系如下图所示。

电解NaCl溶液作为吸收液,若电流强度为4A,吸收NO的反应离子方程式为___________ 。
(2)某氮肥厂处理氨氮废水的方案如图,回答下列问题:
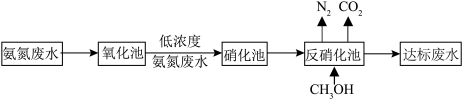
“反硝化池”中发生的变化为:HNO3→ →N2。1 mol HNO3完全转化理论上消耗甲醇的质量为
→N2。1 mol HNO3完全转化理论上消耗甲醇的质量为___________ 。
(3)纳米Fe 可还原去除水中的硝酸盐污染物。转化关系如下:





①检验还原后的溶液中存在 的实验方法是
的实验方法是___________ 。
②溶液初始 pH 较低有利于 的去除,其可能的原因是
的去除,其可能的原因是___________ 。
(1)电解氧化吸收法可将废气中的 NOx转变为NO
 。电解NaCl溶液时,溶液中相关成分的浓度变化与电流强度的关系如下图所示。
。电解NaCl溶液时,溶液中相关成分的浓度变化与电流强度的关系如下图所示。
电解NaCl溶液作为吸收液,若电流强度为4A,吸收NO的反应离子方程式为
(2)某氮肥厂处理氨氮废水的方案如图,回答下列问题:

“反硝化池”中发生的变化为:HNO3→
 →N2。1 mol HNO3完全转化理论上消耗甲醇的质量为
→N2。1 mol HNO3完全转化理论上消耗甲醇的质量为(3)纳米Fe 可还原去除水中的硝酸盐污染物。转化关系如下:





①检验还原后的溶液中存在
 的实验方法是
的实验方法是②溶液初始 pH 较低有利于
 的去除,其可能的原因是
的去除,其可能的原因是
您最近一年使用:0次



