实验室制备 的原理是用亚氯酸钠固体与氯气反应:
的原理是用亚氯酸钠固体与氯气反应: 配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目_______ 。

 与
与 用作消毒剂时均被还原为
用作消毒剂时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的_______ 倍(保留小数点后2位,消毒能力可以用氧化剂转移电子数来衡量)。
 的原理是用亚氯酸钠固体与氯气反应:
的原理是用亚氯酸钠固体与氯气反应: 配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
配平该氧化还原反应方程式,并用单线桥标出电子转移方向和数目
 与
与 用作消毒剂时均被还原为
用作消毒剂时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的
更新时间:2024-03-13 09:49:44
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列填空。
(1)0.5L1mol/L的CaCl2溶液,Cl-的物质的量浓度为___ mol/L。
(2)标况下,33.6L的NH3溶解于水配成1L溶液,则溶液的物质的量浓度为___ mol/L。
(3)在Fe2O3+2Al Al2O3+2Fe中,氧化剂是
Al2O3+2Fe中,氧化剂是___ ;还原产物是___ 。
(4)标出上述方程式电子转移的方向与数目(用双线桥法)___ 。
(5)实验室用MnO2和浓盐酸制氯气:MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑。
MnCl2+2H2O+Cl2↑。
(a)该反应中氧化剂和氧化产物的物质的量之比为___ 。
(b)该反应中,若有0.2molHCl被氧化,能生成标准状况下Cl2的体积为___ L。
(1)0.5L1mol/L的CaCl2溶液,Cl-的物质的量浓度为
(2)标况下,33.6L的NH3溶解于水配成1L溶液,则溶液的物质的量浓度为
(3)在Fe2O3+2Al
 Al2O3+2Fe中,氧化剂是
Al2O3+2Fe中,氧化剂是(4)标出上述方程式电子转移的方向与数目(用双线桥法)
(5)实验室用MnO2和浓盐酸制氯气:MnO2+4HCl(浓)
 MnCl2+2H2O+Cl2↑。
MnCl2+2H2O+Cl2↑。(a)该反应中氧化剂和氧化产物的物质的量之比为
(b)该反应中,若有0.2molHCl被氧化,能生成标准状况下Cl2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】钠和钠的化合物有许多重要的用途,碳酸钠可与氯气发生反应,涉及的反应如下: 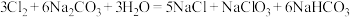
(1)用单线桥法标出电子转移的方向和数目_____________________ 。
(2)该反应中氧化剂与还原剂的个数之比是_____________ ,若  被氧化时,转移的电子是
被氧化时,转移的电子是_____________  。
。
(3)少量的钠应保存在_________ 中;钠着火时应采取的灭火措施是_____________ ,不能用水灭火,原因是_____________________ (涉及反应的离子方程式)。
(4)在实验室配制好的 溶液中通入过量的二氧化碳时发生的离子反应方程式是
溶液中通入过量的二氧化碳时发生的离子反应方程式是_________________________ 。
(5)实验室制备少量氯气的化学反应方程式是_____________________ 。
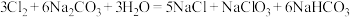
(1)用单线桥法标出电子转移的方向和数目
(2)该反应中氧化剂与还原剂的个数之比是
 被氧化时,转移的电子是
被氧化时,转移的电子是 。
。(3)少量的钠应保存在
(4)在实验室配制好的
 溶液中通入过量的二氧化碳时发生的离子反应方程式是
溶液中通入过量的二氧化碳时发生的离子反应方程式是(5)实验室制备少量氯气的化学反应方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求完成下列试题
(1)用单线桥标出下列反应电子转移的方向和数目
2Na+2H2O=2NaOH+H2↑____
(2)用双线桥标出下列反应化合价升降、电子得失、被氧化或被还原
C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O_____
(3)写出下列物质在水溶液中的电离方程式。
CH3COOH:_________ 。
KAl(SO4)2:_______________ 。
(4)写出硫酸铜溶液与氢氧化钡溶液反应的离子方程式:__________
(1)用单线桥标出下列反应电子转移的方向和数目
2Na+2H2O=2NaOH+H2↑
(2)用双线桥标出下列反应化合价升降、电子得失、被氧化或被还原
C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O(3)写出下列物质在水溶液中的电离方程式。
CH3COOH:
KAl(SO4)2:
(4)写出硫酸铜溶液与氢氧化钡溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】配平下列方程式:
(1)S +HNO3=SO2+NO+H2O______
(2)Zn+HNO3(稀) =Zn(NO3)2+N2O↑+H2O______
(3)Cu2S+HNO3(稀)=Cu(NO3)2+NO↑+H2SO4+H2O_______
(1)S +HNO3=SO2+NO+H2O
(2)Zn+HNO3(稀) =Zn(NO3)2+N2O↑+H2O
(3)Cu2S+HNO3(稀)=Cu(NO3)2+NO↑+H2SO4+H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】二氧化氯( )在工业上可用于淀粉及油脂的漂白及自来水的消毒。回答下列问题:
)在工业上可用于淀粉及油脂的漂白及自来水的消毒。回答下列问题:
(1)制备二氧化氯:
方法1:60℃时,用潮湿的 与草酸(
与草酸( )反应制取
)反应制取 。
。
方法2:亚氯酸钠( )和稀盐酸反应,反应原理为
)和稀盐酸反应,反应原理为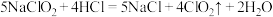 。
。
①方法1中制得的 中混有的气态杂质主要为
中混有的气态杂质主要为_____ (写分子式)。
②方法2中氧化产物和还原产物物质的量之比为______ 。
(2)利用 进行自来水消毒时,需要监测水中
进行自来水消毒时,需要监测水中 的含量,其步骤为:
的含量,其步骤为:
步骤1:量取自来水10.0mL,准确配制100mL检测液,量取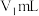 检测液于碘量瓶(
检测液于碘量瓶( )中。
)中。
步骤2:调节试样呈弱酸性,加入足量的KI,立即盖紧碘量瓶的塞子并在塞子周围加入少量水,将碘量瓶置于黑暗处静置片刻。
步骤3:加入几滴淀粉溶液于碘量瓶中,用 的
的 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液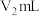 (发生的化学反应方程式:
(发生的化学反应方程式: )。
)。
①制100mL检测液,除了量筒外,还需要_____ (填字母)。
A.普通漏斗B.胶头滴管C.100mL容量瓶D.分液漏斗
②使用碘量瓶代替锥形瓶的目的是_______ (写出一点即可)。
③步骤2中发生反应的离子方程式为_______ 。
④该自来水样品中 的质量浓度为
的质量浓度为_____  (质量浓度
(质量浓度 )。
)。
 )在工业上可用于淀粉及油脂的漂白及自来水的消毒。回答下列问题:
)在工业上可用于淀粉及油脂的漂白及自来水的消毒。回答下列问题:(1)制备二氧化氯:
方法1:60℃时,用潮湿的
 与草酸(
与草酸( )反应制取
)反应制取 。
。方法2:亚氯酸钠(
 )和稀盐酸反应,反应原理为
)和稀盐酸反应,反应原理为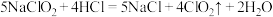 。
。①方法1中制得的
 中混有的气态杂质主要为
中混有的气态杂质主要为②方法2中氧化产物和还原产物物质的量之比为
(2)利用
 进行自来水消毒时,需要监测水中
进行自来水消毒时,需要监测水中 的含量,其步骤为:
的含量,其步骤为:步骤1:量取自来水10.0mL,准确配制100mL检测液,量取
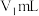 检测液于碘量瓶(
检测液于碘量瓶( )中。
)中。步骤2:调节试样呈弱酸性,加入足量的KI,立即盖紧碘量瓶的塞子并在塞子周围加入少量水,将碘量瓶置于黑暗处静置片刻。
步骤3:加入几滴淀粉溶液于碘量瓶中,用
 的
的 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液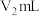 (发生的化学反应方程式:
(发生的化学反应方程式: )。
)。①制100mL检测液,除了量筒外,还需要
A.普通漏斗B.胶头滴管C.100mL容量瓶D.分液漏斗
②使用碘量瓶代替锥形瓶的目的是
③步骤2中发生反应的离子方程式为
④该自来水样品中
 的质量浓度为
的质量浓度为 (质量浓度
(质量浓度 )。
)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是我们常见的几种消毒剂:①“84”消毒液;② (二元弱酸);③
(二元弱酸);③ ;④
;④ ;⑤碘酒;⑥75%酒精;⑦高铁酸钠(Na2FeO4)。回答下列问题:
;⑤碘酒;⑥75%酒精;⑦高铁酸钠(Na2FeO4)。回答下列问题:
(1)上述杀菌消毒剂属于非电解质的是___________ (填序号)。
(2)请写出 的电离方程式:
的电离方程式:___________ 。
(3)各类杀菌消毒剂使用时,必须严格按照使用说明。
巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是 与
与 反应产生
反应产生 促进藻类快速生长。当有
促进藻类快速生长。当有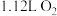 生成时(标准状况下),反应中转移电子为
生成时(标准状况下),反应中转移电子为___________ mol。
(4)工业上可在 溶液中,用
溶液中,用 氧化
氧化 的方法制备
的方法制备 。制备反应的离子方程式为
。制备反应的离子方程式为___________ 。
 (二元弱酸);③
(二元弱酸);③ ;④
;④ ;⑤碘酒;⑥75%酒精;⑦高铁酸钠(Na2FeO4)。回答下列问题:
;⑤碘酒;⑥75%酒精;⑦高铁酸钠(Na2FeO4)。回答下列问题:(1)上述杀菌消毒剂属于非电解质的是
(2)请写出
 的电离方程式:
的电离方程式:(3)各类杀菌消毒剂使用时,必须严格按照使用说明。
巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是
 与
与 反应产生
反应产生 促进藻类快速生长。当有
促进藻类快速生长。当有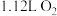 生成时(标准状况下),反应中转移电子为
生成时(标准状况下),反应中转移电子为(4)工业上可在
 溶液中,用
溶液中,用 氧化
氧化 的方法制备
的方法制备 。制备反应的离子方程式为
。制备反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下图是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学的知识,按要求填空:
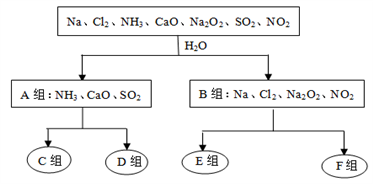
水溶液呈酸性 水溶液呈碱性 水作氧化剂 水既不作氧化剂也不作还原剂
(1)根据物质与水反应的情况,分成A、B组的分类依据是______________________________ ;
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属的物质类别为____ (填序号);
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
(3)D组中的气体水溶液呈弱碱性,用电离方程式表示其水溶液呈弱碱性的原因:________________________________________________________________________________ ;
(4)F组中与水反应氧化剂与还原剂的之比是1:1的物质是______________ (填化学式);
(5)SO2是形成酸雨的主要污染物,目前有一种较为有效的方法是在高空喷洒一种粉末状物质X,脱硫效果可达85%,其反应的化学方程式为:2X+2SO2+O2===2CaSO4+2CO2,由此可知X的化学式是_________ ;
(6)Cl2、Na2O2、SO2都能使品红褪色,其中漂白原理与其它两种物质不同的是_______________ ;将等物质的量的SO2、Cl2同时通入品红溶液中,实验现象是_________________________ ,产生该现象的原因是____________________________________ (用化学方程式表示)。

水溶液呈酸性 水溶液呈碱性 水作氧化剂 水既不作氧化剂也不作还原剂
(1)根据物质与水反应的情况,分成A、B组的分类依据是
(2)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属的物质类别为
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
(3)D组中的气体水溶液呈弱碱性,用电离方程式表示其水溶液呈弱碱性的原因:
(4)F组中与水反应氧化剂与还原剂的之比是1:1的物质是
(5)SO2是形成酸雨的主要污染物,目前有一种较为有效的方法是在高空喷洒一种粉末状物质X,脱硫效果可达85%,其反应的化学方程式为:2X+2SO2+O2===2CaSO4+2CO2,由此可知X的化学式是
(6)Cl2、Na2O2、SO2都能使品红褪色,其中漂白原理与其它两种物质不同的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应的化学方程式_____________ 漂白粉的有效成分是__________ (填化学式)。
(2)实验室制取氨气的化学方程式:__________________________________
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是______________ ;
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因___________________ 现象是:_________________________ 。反应的化学方程式:__________________________________
(5)碳酸钠水解反应的离子方程式(第一步):_________________________ 。
(6)铅蓄电池的负极反应式:_________________________ 。
(7)硫酸钡的沉淀溶解平衡:__________________________________ 。
(2)实验室制取氨气的化学方程式:
(3)1.2gRSO4中含0.01molR2+,则RSO4的摩尔质量是
(4)实验室制Fe(OH)2一般看不到白色的Fe(OH)2沉淀,原因
(5)碳酸钠水解反应的离子方程式(第一步):
(6)铅蓄电池的负极反应式:
(7)硫酸钡的沉淀溶解平衡:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,如图为氯元素的“价类二维图”的部分信息。请回答下列问题:
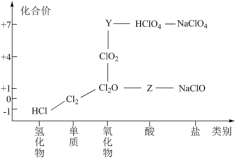
(1)根据图中信息写出Y、Z的化学式______ 、______ 。
(2)漂白液的有效成分是______ ,氯气既有氧化性又有还原性,结合图示说明理由______ 。
(3)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式______ ,该反应中盐酸表现______ (填字母)。
A.酸性 B.氧化性 C.还原性
(4)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为NaClO+2HCl═NaCl+Cl2↑+H2O,下列有关该反应说法不正确 的是______ 。
(5)ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去,下列试剂中可将ClO
),需将其转化为Cl-除去,下列试剂中可将ClO 转化为Cl-的是
转化为Cl-的是______ (填字母)。

(1)根据图中信息写出Y、Z的化学式
(2)漂白液的有效成分是
(3)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式
A.酸性 B.氧化性 C.还原性
(4)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为NaClO+2HCl═NaCl+Cl2↑+H2O,下列有关该反应说法
| A.n(氧化剂)∶n(还原剂)=1∶1 | B.n(氧化剂)∶n(还原剂)=1∶2 |
| C.氧化性:NaClO>Cl2 | D.Cl2既是氧化产物又是还原产物 |
 ),需将其转化为Cl-除去,下列试剂中可将ClO
),需将其转化为Cl-除去,下列试剂中可将ClO 转化为Cl-的是
转化为Cl-的是| A.O3 | B.FeSO4 | C.KI | D.KMnO4 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化还原反应在工农业生产、日常生活中具有广泛用途。
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中不易吸收的Fe3+转变为易吸收的Fe2+,故维生素C具有___________ 性(填“氧化”或“还原”,下同),在反应过程中维生素C发生___________ 反应。
(2)黑火药是我国古代的四大发明之一,爆炸时的反应为:
①配平上述反应。________
②该反应中还原剂是___________ ,还原产物是___________ ,生成1molN2转移电子的物质的量为___________ 。
(3)高温下铝粉和氧化铁的反应可以用来焊接钢轨。其原理是:该反应放出大量的热,置换出的铁呈熔融态。熔融的铁流入钢轨的裂缝里,冷却后将钢轨牢牢地焊接在一起。该反应的化学方程式为___________ ,其中被还原的物质是___________ (填化学式)。
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中不易吸收的Fe3+转变为易吸收的Fe2+,故维生素C具有
(2)黑火药是我国古代的四大发明之一,爆炸时的反应为:

①配平上述反应。
②该反应中还原剂是
(3)高温下铝粉和氧化铁的反应可以用来焊接钢轨。其原理是:该反应放出大量的热,置换出的铁呈熔融态。熔融的铁流入钢轨的裂缝里,冷却后将钢轨牢牢地焊接在一起。该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂。在NaOH溶液中ClO2与H2O2反应可以得到亚氯酸钠,化学反应方程式为:2ClO2+H2O2+2NaOH=2NaClO2+O2↑+2H2O。
(1)ClO2中氯元素的化合价是_______ ;在制备亚氯酸钠的反应中ClO2作_______ (填“氧化剂”或“还原剂”)。
(2)若反应中生成1molNaClO2,转移电子的物质的量为_______ 。
(3)在一定条件下,将Cl2通入填充有固体NaClO2的反应柱内,二者反应可制得ClO2.ClO2作_______ (填“氧化产物”或“还原产物”),当消耗标准状况下1.12LCl2时,制得ClO2_______ g。
(1)ClO2中氯元素的化合价是
(2)若反应中生成1molNaClO2,转移电子的物质的量为
(3)在一定条件下,将Cl2通入填充有固体NaClO2的反应柱内,二者反应可制得ClO2.ClO2作
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)根据反应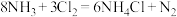 ,回答下列问题。
,回答下列问题。
①氧化剂___________ ,氧化产物___________ 。
②氧化剂与还原剂的分子个数之比:___________ 。
③用单线桥表示该反应的电子转移情况:___________ 。
(2)某反应体系有反应物和生成物共7种: 、
、 、
、 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生如下过程:
只发生如下过程: ,试回答下列问题:
,试回答下列问题:
①该反应中的还原剂是___________ 。
②该反应中,发生还原反应的过程是___________ →___________ 。
③若该反应转移了1mol电子,则产生的气体在标准状况下的体积为___________ L。
④ 可作为矿业废液消毒剂,有“绿色氧化剂”的美称,
可作为矿业废液消毒剂,有“绿色氧化剂”的美称, 被称为绿色氧化剂的理由是
被称为绿色氧化剂的理由是___________ 。
(1)根据反应
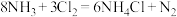 ,回答下列问题。
,回答下列问题。①氧化剂
②氧化剂与还原剂的分子个数之比:
③用单线桥表示该反应的电子转移情况:
(2)某反应体系有反应物和生成物共7种:
 、
、 、
、 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生如下过程:
只发生如下过程: ,试回答下列问题:
,试回答下列问题:①该反应中的还原剂是
②该反应中,发生还原反应的过程是
③若该反应转移了1mol电子,则产生的气体在标准状况下的体积为
④
 可作为矿业废液消毒剂,有“绿色氧化剂”的美称,
可作为矿业废液消毒剂,有“绿色氧化剂”的美称, 被称为绿色氧化剂的理由是
被称为绿色氧化剂的理由是
您最近一年使用:0次



