1 . 将一定量的锌与 浓硫酸充分反应后,锌完全溶解,同时生成气体
浓硫酸充分反应后,锌完全溶解,同时生成气体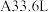 (标准状况)。将反应后的溶液稀释至
(标准状况)。将反应后的溶液稀释至 ,测得溶液的
,测得溶液的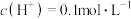 ,则下列叙述中正确的是
,则下列叙述中正确的是
 浓硫酸充分反应后,锌完全溶解,同时生成气体
浓硫酸充分反应后,锌完全溶解,同时生成气体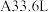 (标准状况)。将反应后的溶液稀释至
(标准状况)。将反应后的溶液稀释至 ,测得溶液的
,测得溶液的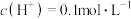 ,则下列叙述中正确的是
,则下列叙述中正确的是A.气体 为 为 |
B.稀释后所得溶液中硫酸根的浓度为 |
| C.该反应若不加热,锌会被钝化 |
D.反应中共转移 电子 电子 |
您最近半年使用:0次
2 . 从元素化合价和物质类别两个角度学习,研究物质的性质,是一种行之有效的方法。下图为氮元素的价类二维图。下列说法错误 的是

A. 的浓溶液与 的浓溶液与 的浓溶液靠近会产生白烟 的浓溶液靠近会产生白烟 |
B. 在一定条件下与氧气反应可直接生成 在一定条件下与氧气反应可直接生成 |
C. 与氧气按一定比例混合溶于水能得到 与氧气按一定比例混合溶于水能得到 |
D.若 为 为 ,碱性条件下由 ,碱性条件下由 、 、 制备 制备 的反应中氧化剂与还原剂的物质的量之比为 的反应中氧化剂与还原剂的物质的量之比为 |
您最近半年使用:0次
3 . 在无氧环境下,将 通入足量
通入足量 稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,并有气体产生。关于上述变化,下列说法
稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,并有气体产生。关于上述变化,下列说法错误 的是
 通入足量
通入足量 稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,并有气体产生。关于上述变化,下列说法
稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,并有气体产生。关于上述变化,下列说法A.最终被还原的是 |
B.氧化性: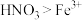 |
C.最终所得溶液中不存在 |
D.同温、同压下, 和逸出气体的体积比为 和逸出气体的体积比为 |
您最近半年使用:0次
4 . 草酸是一种二元弱酸,可用作还原剂、沉淀剂等。某校课外小组的同学设计利用C2H2气体制取H2C2O4·2H2O。回答下列问题:
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。___________ (写一种即可)。
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为___________ 。该过程中,可能产生新的杂质气体Cl2,其原因是:___________ (用离子方程式回答)。
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是___________ 。
②装置D中生成H2C2O4的化学方程式为___________ 。
③从装置D中得到产品,还需经过___________ (填操作名称)、过滤、洗涤及干燥。
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是___________ 。
②产品中H2C2O4·2H2O的质量分数为___________ (列出含 m、c、V 的表达式)。
(1)甲组的同学以电石(主要成分CaC2,少量CaS及Ca3P2杂质等)为原料,并用下图1装置制取C2H2。
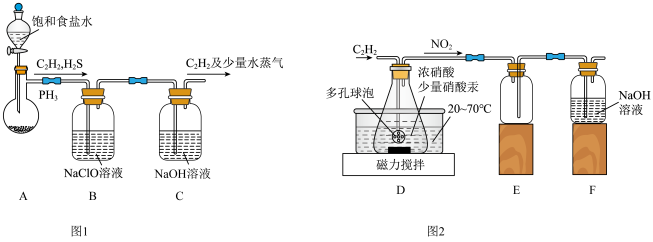
②装置B中,NaClO将H2S、PH3 氧化为硫酸及磷酸,本身被还原为NaCl,其中PH3被氧化的离子方程式为
(2)乙组的同学根据文献资料,用Hg(NO3)2作催化剂,浓硝酸氧化C2H2制取H2C2O4·2H2O。制备装置如上图2所示:
①装置D中多孔球泡的作用是
②装置D中生成H2C2O4的化学方程式为
③从装置D中得到产品,还需经过
(3)丙组设计了测定乙组产品中H2C2O4·2H2O的质量分数实验。他们的实验步骤如下:准确称取m g产品于锥形瓶中,加入适量的蒸馏水溶解,再加入少量稀硫酸,然后用c mol·L-1酸性KMnO4标准溶液进行滴定至终点,共消耗标准溶液V mL。
①滴定终点的现象是
②产品中H2C2O4·2H2O的质量分数为
您最近半年使用:0次
5 . 设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.78gNa2S和Na2O2的混合物中含有阴离子的数目为NA |
| B.标准状况下2.24LCl2完全溶于水时,转移电子数为0.1NA |
| C.46gC2H6O分子中含极性键数目一定是7NA |
| D.100g含甲酸46%的水溶液中含氧原子数为2NA |
您最近半年使用:0次
名校
解题方法
6 . NH3经一系列反应可以得到HNO3和NH4NO3,如图所示。
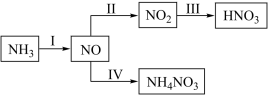
(1)氨气的结构式为_________ 。
(2)实验室里用NH4Cl和熟石灰共热制取氨气反应的化学方程式为_____________________ 。
(3)步骤Ⅰ中NH3和O2存催化剂作用下反应生成NO,其化学方程式是_____________________ 。
(4)写出步骤Ⅲ发生反应的化学方程式_______________________ ,该反应中氧化剂与还原剂的物质的量之比是____________ 。
(5)工业生产中为了盛装大量浓硝酸,最好选择_______作为罐体材料。
(6)通过实验检验试样中的 的方法:取少量试样于试管中,
的方法:取少量试样于试管中,_________________________ 。

(1)氨气的结构式为
(2)实验室里用NH4Cl和熟石灰共热制取氨气反应的化学方程式为
(3)步骤Ⅰ中NH3和O2存催化剂作用下反应生成NO,其化学方程式是
(4)写出步骤Ⅲ发生反应的化学方程式
(5)工业生产中为了盛装大量浓硝酸,最好选择_______作为罐体材料。
| A.铜 | B.铂 | C.铝 | D.镁 |
(6)通过实验检验试样中的
 的方法:取少量试样于试管中,
的方法:取少量试样于试管中,
您最近半年使用:0次
7 . 按要求回答下列问题:
(1)实验室制备氨气,下列方法中可以选用的是_______ 。
a.固态氯化铵加热分解 b.浓氨水中加入固体氢氧化钠
c.加热浓氨水 d.固态氯化铵与氢氧化钙混合加热
(2)氯化铵溶液显酸性,用离子方程式表示呈酸性的原因_______ 。
(3)NH3常用于检验氯气管道是否泄漏,写出反应的化学方程式_______ 。
(4)将57.6克的铜投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共1.4 mol。
①写出刚开始反应的化学方程式_______ ;
②求硝酸的浓度_______ mol·L-1;
③将生成的气体收集在大试管中,然后倒扣在水中,写出二氧化氮与水反应的化学方程式_______ ,若往试管中通入氧气让液体充满试管,则通入氧气的物质的量_______ mol。
(1)实验室制备氨气,下列方法中可以选用的是
a.固态氯化铵加热分解 b.浓氨水中加入固体氢氧化钠
c.加热浓氨水 d.固态氯化铵与氢氧化钙混合加热
(2)氯化铵溶液显酸性,用离子方程式表示呈酸性的原因
(3)NH3常用于检验氯气管道是否泄漏,写出反应的化学方程式
(4)将57.6克的铜投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共1.4 mol。
①写出刚开始反应的化学方程式
②求硝酸的浓度
③将生成的气体收集在大试管中,然后倒扣在水中,写出二氧化氮与水反应的化学方程式
您最近半年使用:0次
名校
解题方法
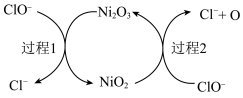
8 . 工业上常用碱性 废液吸收
废液吸收 ,反应原理为
,反应原理为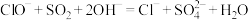 ,部分催化过程如图所示。下列说法正确的是
,部分催化过程如图所示。下列说法正确的是
 废液吸收
废液吸收 ,反应原理为
,反应原理为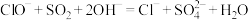 ,部分催化过程如图所示。下列说法正确的是
,部分催化过程如图所示。下列说法正确的是
A.“过程1”中氧化产物与还原产物的物质的量之比为 |
B.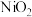 是该反应的催化剂 是该反应的催化剂 |
C.“过程2”可表示为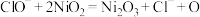 |
D.吸收过程中存在反应: |
您最近半年使用:0次
2024-03-02更新
|
444次组卷
|
3卷引用:湖南省宁乡市第一高级中学2021届高三第三次模拟考试化学试卷
9 . 近日,上海交通大学周保学教授等人提出了一种如下图所示的光电催化体系,该体系既能将SO2转化为 所释放的化学能用于驱动阴极H2O2的高效生成,也可以实现烟气脱SO2。则下列说法不正确的是
所释放的化学能用于驱动阴极H2O2的高效生成,也可以实现烟气脱SO2。则下列说法不正确的是
 所释放的化学能用于驱动阴极H2O2的高效生成,也可以实现烟气脱SO2。则下列说法不正确的是
所释放的化学能用于驱动阴极H2O2的高效生成,也可以实现烟气脱SO2。则下列说法不正确的是
A.阴极反应为: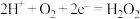 |
B.电路中转移 电子时,阴极消耗 电子时,阴极消耗 的氧气 的氧气 |
C.每生成 ,伴随着1mol H2O2的生成 ,伴随着1mol H2O2的生成 |
| D.电解液中有2个离子交换膜,靠近阳极的为阴离子交换膜,靠近阴极的为阳离子交换膜 |
您最近半年使用:0次
名校
10 . 已知反应:6HCl(浓)+KClO3=KCl+3Cl2 ↑+3H2O ,下列说法正确的是
| A.浓盐酸只做还原剂 | B.生成 3 分子 Cl2 有 6 个电子转移 |
| C.被氧化和被还原的的氯元素的质量比为 6:1 | D.氯气既是氧化产物又是还原产物 |
您最近半年使用:0次



