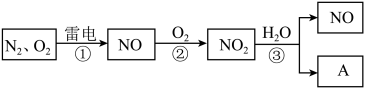
1 . 以下是氮循环的一部分:_____ ;
(2)反应 的化学方程式是
的化学方程式是_____ ;
(3) 易溶于水,并和水发生化学反应。该反应中,氧化剂是
易溶于水,并和水发生化学反应。该反应中,氧化剂是_____ ;
(4)化合物 的化学式是
的化学式是_____ ;
(5)治理汽车尾气的一种方法是用催化剂使 与
与 发生反应:
发生反应: 。当生成
。当生成 时,被还原的
时,被还原的 为
为_____  。
。
(2)反应
 的化学方程式是
的化学方程式是(3)
 易溶于水,并和水发生化学反应。该反应中,氧化剂是
易溶于水,并和水发生化学反应。该反应中,氧化剂是(4)化合物
 的化学式是
的化学式是(5)治理汽车尾气的一种方法是用催化剂使
 与
与 发生反应:
发生反应: 。当生成
。当生成 时,被还原的
时,被还原的 为
为 。
。
您最近半年使用:0次
2 . 有效去除大气中的 是环境保护的重要课题。
是环境保护的重要课题。
(1)用水吸收 的相关热化学方程式如下:
的相关热化学方程式如下:
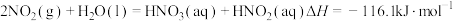
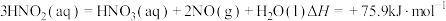
反应 的
的
___________  。
。
(2)用稀硝酸吸收 ,得到
,得到 和
和 的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式:
的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式:___________ 。( 是弱酸)
是弱酸)
(3)用酸性 水溶液吸收
水溶液吸收 ,吸收过程中存在
,吸收过程中存在 与
与 生成
生成 和
和 的反应,写出该反应的化学方程式:
的反应,写出该反应的化学方程式:___________ 。
(4)在有氧条件下,新型催化剂 能催化
能催化 与
与 反应生成
反应生成 。
。
① 与
与 生成
生成 的反应中,当生成
的反应中,当生成 时,转移的电子数为
时,转移的电子数为___________  。
。
②将一定比例的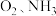 和
和 的混合气体,匀速通入装有催化剂
的混合气体,匀速通入装有催化剂 的反应器中反应(装置见图):
的反应器中反应(装置见图): 的去除率随反应温度的变化曲线如图所示,在
的去除率随反应温度的变化曲线如图所示,在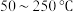 范围内随着温度的升高,
范围内随着温度的升高, 的去除率先迅速上升后缓慢上升的主要原因是
的去除率先迅速上升后缓慢上升的主要原因是___________ 。 (氯的化合价为
(氯的化合价为 价),其原理是
价),其原理是
 接电源的
接电源的___________ (填“正”或“负”)极。
②阳极反应式是___________ 。
 是环境保护的重要课题。
是环境保护的重要课题。(1)用水吸收
 的相关热化学方程式如下:
的相关热化学方程式如下: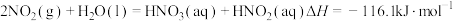
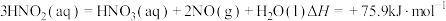
反应
 的
的
 。
。(2)用稀硝酸吸收
 ,得到
,得到 和
和 的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式:
的混合溶液,电解该混合溶液可获得较浓的硝酸,写出电解时阳极的电极反应式: 是弱酸)
是弱酸)(3)用酸性
 水溶液吸收
水溶液吸收 ,吸收过程中存在
,吸收过程中存在 与
与 生成
生成 和
和 的反应,写出该反应的化学方程式:
的反应,写出该反应的化学方程式:(4)在有氧条件下,新型催化剂
 能催化
能催化 与
与 反应生成
反应生成 。
。①
 与
与 生成
生成 的反应中,当生成
的反应中,当生成 时,转移的电子数为
时,转移的电子数为 。
。②将一定比例的
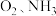 和
和 的混合气体,匀速通入装有催化剂
的混合气体,匀速通入装有催化剂 的反应器中反应(装置见图):
的反应器中反应(装置见图):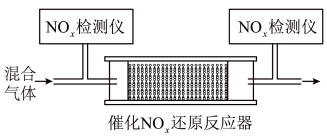
 的去除率随反应温度的变化曲线如图所示,在
的去除率随反应温度的变化曲线如图所示,在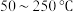 范围内随着温度的升高,
范围内随着温度的升高, 的去除率先迅速上升后缓慢上升的主要原因是
的去除率先迅速上升后缓慢上升的主要原因是
 (氯的化合价为
(氯的化合价为 价),其原理是
价),其原理是
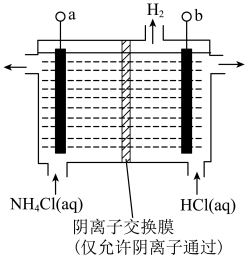
 接电源的
接电源的②阳极反应式是
您最近半年使用:0次
名校
3 . 设 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是
 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是A.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2 |
B.含2mol  的浓硫酸和足量的Cu反应可生成 的浓硫酸和足量的Cu反应可生成 个 个 分子 分子 |
C.标准状况下,22.4L  和 和 混合气中含 混合气中含 个原子 个原子 |
D.18g  和18g 和18g  中含有的质子数均为10 中含有的质子数均为10 |
您最近半年使用:0次
4 . 可用Al与NaOH溶液反应来疏通下水管道。下列说法错误的是
| A.Al是还原剂,发生氧化反应 |
B.每生成1mol  ,转移2mol电子 ,转移2mol电子 |
| C.可用NaOH溶液除去镁粉中混有的少量Al粉 |
D.等量的铝与足量NaOH溶液反应生成的 比与足量盐酸反应生成的多 比与足量盐酸反应生成的多 |
您最近半年使用:0次
名校
5 . 一种新型人工固氮的原理如图所示,下列叙述正确的是
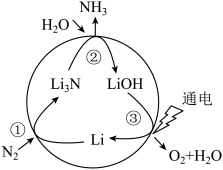
| A.转化过程中所涉及的元素均呈现了两种价态 |
| B.参与反应的物质均只含离子键 |
| C.反应①②③均为氧化还原反应 |
D.假设每一步均完全转化,每生成2mol ,同时生成1.5mol ,同时生成1.5mol |
您最近半年使用:0次
2024-04-20更新
|
200次组卷
|
2卷引用:2024届天津市宁河区芦台第一中学高三下学期第三次模拟化学试题
名校
解题方法
6 . I.将39g锌与50mL18.4mol/L的浓硫酸充分反应,锌完全溶解,同时收集到标准状况下气体VL,将反应后的溶液稀释到500mL,测得溶液中氢离子的浓度为0.08mol/L。
(1)反应过程中消耗 的物质的量是
的物质的量是_______ 。
(2)气体的成分是_______ ,V=_______ 。
Ⅱ.将1.52g铜镁合金完全溶解于50mL8mol/L的浓硝酸中,得到NO和 的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。
的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。
(3)此时加入的1.0mol/LNaOH溶液的体积为_______ mL。
(4)混合气体中,NO和 的物质的量之比为
的物质的量之比为_______ 。
(5)若将上述生成的混合气体全部与 一起通入水中,使其完全转化为
一起通入水中,使其完全转化为 ,需通入标准状况下的氧气至少
,需通入标准状况下的氧气至少_______ mL。
(1)反应过程中消耗
 的物质的量是
的物质的量是(2)气体的成分是
Ⅱ.将1.52g铜镁合金完全溶解于50mL8mol/L的浓硝酸中,得到NO和
 的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。
的混合气体896mL(标准状况),向反应后的溶液中加入1.0mol/LNaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。(3)此时加入的1.0mol/LNaOH溶液的体积为
(4)混合气体中,NO和
 的物质的量之比为
的物质的量之比为(5)若将上述生成的混合气体全部与
 一起通入水中,使其完全转化为
一起通入水中,使其完全转化为 ,需通入标准状况下的氧气至少
,需通入标准状况下的氧气至少
您最近半年使用:0次
7 . 实验室制取A并进一步制取无水FeCl3的实验装置如图所示。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。
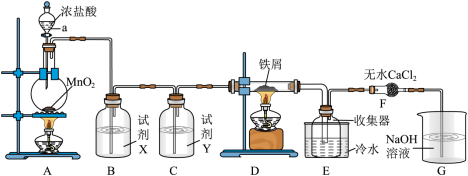
回答下列问题:
(1)仪器a的名称是_______ ,装置A所发生的氧化还原反应中,氧化剂与还原剂的物质的量之比为_______ 。
(2)试剂X是_______ 。
(3)装置F中无水CaCl2的作用是_______
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:_______ 。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。

回答下列问题:
(1)仪器a的名称是
(2)试剂X是
(3)装置F中无水CaCl2的作用是
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO
 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:
您最近半年使用:0次
8 . 纳米零价铁电化学法除去酸性废水中三氯乙烯、五价砷的原理如图所示。下列说法正确的是
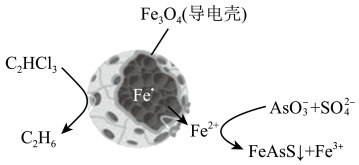
A. 是碱性氧化物 是碱性氧化物 |
B.该酸性废水中的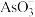 发生氧化反应 发生氧化反应 |
| C.该处理过程中纳米零价铁中的铁为正极 |
D.在电极反应中,每生成 乙烷气体(标准状况下),理论上会消耗 乙烷气体(标准状况下),理论上会消耗 纳米零价铁 纳米零价铁 |
您最近半年使用:0次
解题方法
9 . 如图为MnO2的有关转化关系图,下列有关说法中不正确的是


| A.反应①~⑥均属于氧化还原反应. |
| B.反应①中氧化剂与还原剂的物质的量之比为1:4 |
| C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1:2 |
| D.反应①生成的Cl2经干燥后,可用钢瓶贮运 |
您最近半年使用:0次
解题方法
10 . 我国科学家利用电力驱动电催化二氧化碳还原反应(CRR),将二氧化碳转换成高附加值的化学品或燃料,是一种有效的缓解能源危机和全球变暖的理想途径。该反应涉及到CO2、NaClO、CO、NaCl几种微粒,其中NaCl、CO的物质的量随时间变化的曲线如图所示。下列说法正确的是
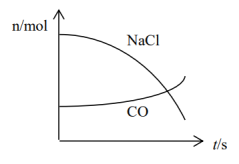

| A.该反应氧化剂与还原剂物质的量之比为1∶1 |
| B.NaClO作氧化剂 |
| C.NaClO是漂白粉的有效成分 |
| D.lmolNaCl完全反应,转移1mol电子 |
您最近半年使用:0次



