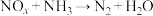 来消除污染。有关此反应,下列说法中错误的是
来消除污染。有关此反应,下列说法中错误的是| A.N2既是氧化产物又是还原产物 |
| B.当x=1时,每生成5个N2分子,被氧化的气体分子有6个 |
| C.当x=2时,有1个气体分子被还原,将转移4个电子 |
D.反应通式配平表示为: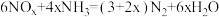 |
 。据此判断下列说法错误的是
。据此判断下列说法错误的是| A.X原子最外层电子数为5 |
| B.当有3个X2生成时,转移5个电子 |
C.“□”中所填的微粒为 |
| D.氧化产物和还原产物的质量之比为5∶1 |
| A.Na2O2与木炭的反应是放热反应 |
| B.Na2O2的阴、阳离子个数比是1∶1 |
| C.Na2O2与Al反应时Na2O2表现出强氧化性 |
| D.已知Na2O2与SO2反应可生成Na2SO4,SO2是还原剂 |
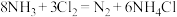 ,下列说法正确的是( )
,下列说法正确的是( )A. 发生氧化反应 发生氧化反应 |
B. 既是氧化剂又是还原剂 既是氧化剂又是还原剂 |
C.被氧化的 与被还原的 与被还原的 的化学计量数之比为2∶3 的化学计量数之比为2∶3 |
D.参加反应 的化学计量数与转移电子数之间的关系为: 的化学计量数与转移电子数之间的关系为: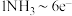 |
5 . 2023年10月4日,瑞典皇家科学院宣布将2023年诺贝尔化学奖授予美国麻省理工学院教授蒙吉·巴文迪(MoungiG.Bawendi)、美国群伦比亚大学教授路易斯・布鲁斯(LouisE.Brus)和美国纳米晶体科技公司科学家阿列克谢.叶基莫夫(AlexeyI.Ekimov),以表彰他们对量子点的发现与合成所作的贡献。中国科学技术大学熊宇杰、高超教授利用光催化和Ru可以有效地从CdS量子点中提取光生带正电空穴(用h+表示,可捕获电子)和电子,进一步氧化HMF( )来生产HMFCA(
)来生产HMFCA( )和DFF(
)和DFF( ),该成果于2022年发表于世界化学顶级期刊《Angew.Chem.Int.Ed.》,反应原理如图所示:下列说法错误的是
),该成果于2022年发表于世界化学顶级期刊《Angew.Chem.Int.Ed.》,反应原理如图所示:下列说法错误的是

| A.在相同条件下,适当增加光的强度或酸度有利于加快反应速率 |
| B.生成DFF整个过程中,氧化产物与还原产物的物质的量比为1:1 |
| C.生成HMFCA过程中,Ru-CdS表面反应的机理,一定有e-或h+参与 |
| D.当生成HMFCA与DFF物质的量比为1:1时,CdS量子点至少产生3molh+ |

下列说法正确的是
| A.反应物微粒为SO2、 Mn2+、 H+ |
| B.该反应发生后溶液酸性增强 |
| C.氧化剂和还原剂的化学计量数之比为5∶2 |
| D.配平后H⁺的化学计量数为8 |
 完全转化为
完全转化为 ,该反应可表示为
,该反应可表示为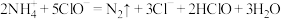 。下列说法中错误的是
。下列说法中错误的是A.还原性: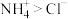 |
| B.反应中氮元素被还原,氯元素被氧化 |
C.反应中每生成1个 分子,转移6个电子 分子,转移6个电子 |
| D.经此法处理过的废水需要调至中性后再排放 |
(1)下列所含铁元素只有还原性的物质是
A.Fe B.FeCl3 C.FeSO4
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔(转化为Cu2+)来制造印刷电路板。写出FeCl3溶液与铜发生反应的化学方程式
A.固体中一定有铜 B.固体中一定有铁
C.溶液中一定有Fe2+ D.溶液中一定有Cu2+
(4)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式(5)某“铁基脱氧剂”的主要成分是还原Fe粉,使用一段时间后会部分变质为Fe2O3。将一包使用过一段时间后的脱氧剂用稀盐酸浸泡,浸泡过程中粉末表面有大量细小无色气泡产生。溶液中的反应有:
 、
、 、
、 (主要指NO和
(主要指NO和 )是大气主要污染物,有效去除大气中的
)是大气主要污染物,有效去除大气中的 是环境保护的重要课题,在催化剂的作用下,
是环境保护的重要课题,在催化剂的作用下, 与
与 可发生反应:
可发生反应: ,下列说法错误的是
,下列说法错误的是A.该反应中, 表现了还原性 表现了还原性 |
B.每生成7个 ,反应中转移了24个电子 ,反应中转移了24个电子 |
C.同温同压下,NO和 的密度之比为15∶23 的密度之比为15∶23 |
D.根据氧化还原反应的规律, 也可将 也可将 转化为 转化为 以消除污染 以消除污染 |
10 . 工业上用 (分子结构:
(分子结构: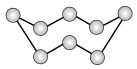 )与
)与 为原料制备
为原料制备 ,发生反应:
,发生反应: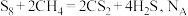 为阿伏加德罗常数的值,下列说法不正确的是
为阿伏加德罗常数的值,下列说法不正确的是
A. 既是氧化剂,又是还原剂 既是氧化剂,又是还原剂 |
B.生成 ,转移电子 ,转移电子 |
C.消耗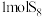 ,断裂的S-S键数目为 ,断裂的S-S键数目为 |
D. 既是氧化产物,又是还原产物 既是氧化产物,又是还原产物 |



