1 . 铁是地壳中占比较高的元素,其化合物在自然界十分常见。
(1)某铁原子可表示为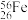 ,其核内中子数是
,其核内中子数是___________ 。
(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为___________ ;设阿伏加德罗常数的值为 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为___________ 。
(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入___________ 溶液并振荡,若滤液变为红色,则药品已变质。
(4)现有甲、乙、丙三名同学分别进行制备 胶体的实验。甲同学向
胶体的实验。甲同学向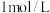 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
①操作正确的同学是___________ 。
②写出制备胶体过程中的离子方程式___________ 。欲除去胶体中混有的 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是___________ 。
③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为___________ 。
(1)某铁原子可表示为
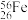 ,其核内中子数是
,其核内中子数是(2)将一个铁球打磨、烧红后放入充满水蒸气的容器中,则发生反应的化学方程式为
 ,当参与反应的
,当参与反应的 的物质的量为
的物质的量为 时,转移的电子数为
时,转移的电子数为(3)服用乳酸亚铁咀嚼片可以缓解缺铁性贫血的症状,其在长期贮存过程中可能因氧化而发生变质,现取少量药片碾碎、溶解、过滤,取滤液加入
(4)现有甲、乙、丙三名同学分别进行制备
 胶体的实验。甲同学向
胶体的实验。甲同学向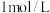 氯化铁溶液中滴入少量的
氯化铁溶液中滴入少量的 溶液;乙同学向
溶液;乙同学向 沸水中逐滴加入
沸水中逐滴加入 饱和溶液;丙同学直接加热
饱和溶液;丙同学直接加热 饱和
饱和 溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。
溶液;三人均准备在煮沸至液体呈红褐色后,停止加热。①操作正确的同学是
②写出制备胶体过程中的离子方程式
 杂质,可以采取的操作方法是
杂质,可以采取的操作方法是③丁同学向所得胶体中逐滴滴加稀硫酸,实验现象为
您最近半年使用:0次
2 . 在浓盐酸存在的情况下,黄金可以与硝酸反应生成氯金酸( )与
)与 ,则参与反应的氧化剂与还原剂的物质的量之比为
,则参与反应的氧化剂与还原剂的物质的量之比为
 )与
)与 ,则参与反应的氧化剂与还原剂的物质的量之比为
,则参与反应的氧化剂与还原剂的物质的量之比为A.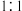 | B.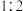 | C.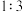 | D.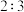 |
您最近半年使用:0次
3 . 联氨( )可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,其中一种反应机理如图所示。下列叙述不正确的是
)可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,其中一种反应机理如图所示。下列叙述不正确的是
 )可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,其中一种反应机理如图所示。下列叙述不正确的是
)可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,其中一种反应机理如图所示。下列叙述不正确的是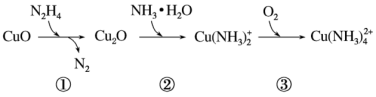
A.①转化中 是还原剂 是还原剂 | B.③转化中 是氧化产物 是氧化产物 |
C.1分子 可处理1分子 可处理1分子 | D.上述三个转化过程①②③均为氧化还原反应 |
您最近半年使用:0次
名校
解题方法
4 . 水合硼酸锌(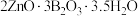 ,不溶于冷水)在阻燃方面具有诸多优点。以铁硼矿(主要成分为
,不溶于冷水)在阻燃方面具有诸多优点。以铁硼矿(主要成分为 ,以及少量
,以及少量 和
和 等)和菱锌矿(主要成分为
等)和菱锌矿(主要成分为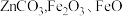 和
和 等)为原料制备水合硼酸锌的工艺流程如下:
等)为原料制备水合硼酸锌的工艺流程如下: 如下表所示:
如下表所示:
回答下列问题:
(1)“酸浸”时, 与硫酸反应的离子方程式为
与硫酸反应的离子方程式为__________ 。为加快“酸浸”时的浸取速率,下列措施中无法达到目的是__________ (填字母)。
a.将样品粉碎 b.延长浸取时间 c.充分搅拌 d.适当增加硫酸浓度 e.适当升高温度
(2)滤渣1的主要成分为__________ (填化学式)。
(3)“氧化”的目的是__________ (语言叙述), 也可以用
也可以用 代替,若“氧化”过程中转移电子数相等,则消耗
代替,若“氧化”过程中转移电子数相等,则消耗 和
和 的物质的量之比为
的物质的量之比为__________ 。
(4)“一次调 ”时,调节溶液的
”时,调节溶液的 ,目的是
,目的是__________ 。“二次调 ”时的
”时的 范围为
范围为__________ 。
(5)“制备”水合硼酸锌的化学方程式为__________ 。
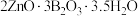 ,不溶于冷水)在阻燃方面具有诸多优点。以铁硼矿(主要成分为
,不溶于冷水)在阻燃方面具有诸多优点。以铁硼矿(主要成分为 ,以及少量
,以及少量 和
和 等)和菱锌矿(主要成分为
等)和菱锌矿(主要成分为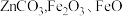 和
和 等)为原料制备水合硼酸锌的工艺流程如下:
等)为原料制备水合硼酸锌的工艺流程如下:
 如下表所示:
如下表所示:金属离子 |
|
|
|
|
|
开始沉淀 | 1.9 | 7.0 | 3.0 | 6.2 | 8.9 |
完全沉淀 | 3.2 | 9.0 | 4.7 | 8.0 | 10.9 |
(1)“酸浸”时,
 与硫酸反应的离子方程式为
与硫酸反应的离子方程式为a.将样品粉碎 b.延长浸取时间 c.充分搅拌 d.适当增加硫酸浓度 e.适当升高温度
(2)滤渣1的主要成分为
(3)“氧化”的目的是
 也可以用
也可以用 代替,若“氧化”过程中转移电子数相等,则消耗
代替,若“氧化”过程中转移电子数相等,则消耗 和
和 的物质的量之比为
的物质的量之比为(4)“一次调
 ”时,调节溶液的
”时,调节溶液的 ,目的是
,目的是 ”时的
”时的 范围为
范围为(5)“制备”水合硼酸锌的化学方程式为
您最近半年使用:0次
2024-04-21更新
|
161次组卷
|
2卷引用:2024届内蒙古自治区乌海市第六中学高三下学期第三次模拟考试理综试题-高中化学
名校
5 . 一种新型人工固氮的原理如图所示,下列叙述正确的是
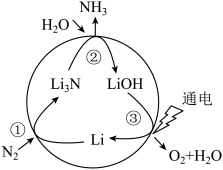
| A.转化过程中所涉及的元素均呈现了两种价态 |
| B.参与反应的物质均只含离子键 |
| C.反应①②③均为氧化还原反应 |
D.假设每一步均完全转化,每生成2mol ,同时生成1.5mol ,同时生成1.5mol |
您最近半年使用:0次
2024-04-20更新
|
200次组卷
|
2卷引用:2024届内蒙古自治区赤峰市高三一模化学试题
名校
6 . 电视剧中美轮美奂的“仙境”,其中所需的烟雾是在置于温热石棉网上的NH4NO3和Zn粉混合物中滴几滴水后能持续产生白烟,涉及反应: 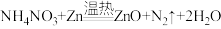 。下列有关说法中错误的是
。下列有关说法中错误的是
| A.上述反应属于氧化还原反应 |
| B.氮气既是氧化产物也是还原反应 |
| C.在标准状况下,11.2LN2中所含电子的物质的量为6mol |
| D.每生成1molZnO共转移5mol电子 |
您最近半年使用:0次
7 . 强氧化剂一般用来进行消毒、漂白等工序。回答下列问题:
(1)臭氧可以通过氧气在放电条件下生成,上述两种单质都是氧元素的_______ 。
(2)1984年,北京第一传染病医院研制成功能迅速杀灭各类肝炎病毒的消毒液,后更名为“84消毒液”。该消毒液可用氯气与氢氧化钠溶液在常温下反应制得,发生反应的离子方程式为_______ 。如果在某次反应中,有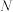 个氯气分子参与此反应,则过程中转移的电子数为
个氯气分子参与此反应,则过程中转移的电子数为_______ 。
(3)漂粉精中的有效成分为_______ ,其进行焰色试验的特征颜色为_______ (填标号)。
a.黄色 b.砖红色 c.绿色 d.紫红色
(4)新型的消毒剂 在中性溶液中可将剧毒的
在中性溶液中可将剧毒的 氧化为两种无毒的气体,自身被还原为
氧化为两种无毒的气体,自身被还原为 ,则发生反应的离子方程式为
,则发生反应的离子方程式为_______ ;“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是“分别在氧化还原反应中得到等量的电子时, 与该种含氯消毒剂的质量比”,则
与该种含氯消毒剂的质量比”,则 的有效氯含量为
的有效氯含量为_______ (结果保留两位小数)。
(1)臭氧可以通过氧气在放电条件下生成,上述两种单质都是氧元素的
(2)1984年,北京第一传染病医院研制成功能迅速杀灭各类肝炎病毒的消毒液,后更名为“84消毒液”。该消毒液可用氯气与氢氧化钠溶液在常温下反应制得,发生反应的离子方程式为
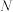 个氯气分子参与此反应,则过程中转移的电子数为
个氯气分子参与此反应,则过程中转移的电子数为(3)漂粉精中的有效成分为
a.黄色 b.砖红色 c.绿色 d.紫红色
(4)新型的消毒剂
 在中性溶液中可将剧毒的
在中性溶液中可将剧毒的 氧化为两种无毒的气体,自身被还原为
氧化为两种无毒的气体,自身被还原为 ,则发生反应的离子方程式为
,则发生反应的离子方程式为 与该种含氯消毒剂的质量比”,则
与该种含氯消毒剂的质量比”,则 的有效氯含量为
的有效氯含量为
您最近半年使用:0次
8 . 在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验所用的仪器如下:
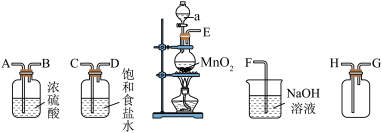
回答下列问题:
(1)仪器a的名称为_______ 。
(2)连接上述装置的正确顺序是:
_______  。
。
(3)气体发生装置中进行的反应化学方程式是_______ ;若收集到的氯气的质量为7.1g,则被氧化的 的质量是
的质量是_______ 。
(4)饱和食盐水的作用为_______ 。
(5)将足量氯气缓慢通入紫色石蕊溶液中,现象为_______ 。
(6)常温下使用高锰酸钾与浓盐酸也可以制氯气,且锰元素在反应中全部转化为 ,反应的化学方程式为
,反应的化学方程式为_______ 。

回答下列问题:
(1)仪器a的名称为
(2)连接上述装置的正确顺序是:
 。
。(3)气体发生装置中进行的反应化学方程式是
 的质量是
的质量是(4)饱和食盐水的作用为
(5)将足量氯气缓慢通入紫色石蕊溶液中,现象为
(6)常温下使用高锰酸钾与浓盐酸也可以制氯气,且锰元素在反应中全部转化为
 ,反应的化学方程式为
,反应的化学方程式为
您最近半年使用:0次
名校
解题方法
9 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。黑木耳中含有比较丰富的铁元素,某研究型学习小组同学测定某地黑木耳中铁的含量。
(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用下图流程处理,对滤液中的溶质进行研究。
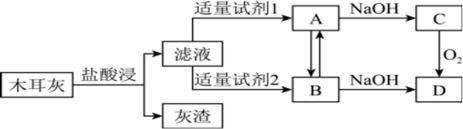
①浸泡液检测不出铁元素的原因是_______ 。
②试剂l应该是_______ 。
(2)A转化为B可加入的试剂有_______ 。
a.酸性高锰酸钾 b.Cl2 c.H2O2溶液
(3)C生成D时的反应现象为_______ 。
(4)已知在酸性条件下Fe2+可被氧气氧化为Fe3+,该反应每转移8mol电子,标准状况下消耗氧气的体积为_______ L。
(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用下图流程处理,对滤液中的溶质进行研究。

①浸泡液检测不出铁元素的原因是
②试剂l应该是
(2)A转化为B可加入的试剂有
a.酸性高锰酸钾 b.Cl2 c.H2O2溶液
(3)C生成D时的反应现象为
(4)已知在酸性条件下Fe2+可被氧气氧化为Fe3+,该反应每转移8mol电子,标准状况下消耗氧气的体积为
您最近半年使用:0次
名校
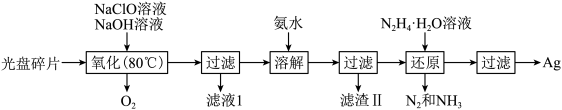
10 . 利用如下流程可从废光盘中回收金属层中的银(金属层中其他金属含量过低,对实验影响可忽略):
已知: 溶液在加热时易分解生成
溶液在加热时易分解生成 和
和 。下列说法不正确的是
。下列说法不正确的是
已知:
 溶液在加热时易分解生成
溶液在加热时易分解生成 和
和 。下列说法不正确的是
。下列说法不正确的是
| A.若省略第一次过滤,会使氨水的用量增加 |
B.若“还原”工序利用原电池来实现,则 是正极产物 是正极产物 |
C.“还原”时,每生成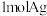 ,理论上消耗 ,理论上消耗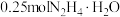 |
D.“溶解”工序发生的反应: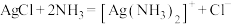 |
您最近半年使用:0次








