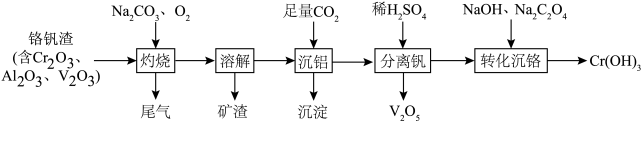
1 . 某科研团队从铬钒渣中分离钒并制备Cr(OH)3的流程如下:
②Cr的最高价含氧酸根离子在酸性介质中主要以 存在,在碱性介质中主要以
存在,在碱性介质中主要以 存在。
存在。
下列说法错误的是
②Cr的最高价含氧酸根离子在酸性介质中主要以
 存在,在碱性介质中主要以
存在,在碱性介质中主要以 存在。
存在。下列说法错误的是
| A.“灼烧”步骤的尾气中含CO2 |
B.“沉铝”步骤的离子方程式为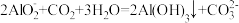 |
C.“分离钒”之后Cr元素的存在形式主要为 |
| D.“转化沉铬”步骤中氧化剂与还原剂的物质的量之比为1∶3 |
您最近半年使用:0次
7日内更新
|
229次组卷
|
2卷引用:福建省漳州市2024届高三下学期毕业班第三次质量检测三模化学试题
名校
解题方法
2 . 2.48g铁铜合金完全溶解于80mL 4.0 稀硝酸中,得到标准状况下672mL NO气体(假设此时无其他气体产生),下列说法正确的是
稀硝酸中,得到标准状况下672mL NO气体(假设此时无其他气体产生),下列说法正确的是
 稀硝酸中,得到标准状况下672mL NO气体(假设此时无其他气体产生),下列说法正确的是
稀硝酸中,得到标准状况下672mL NO气体(假设此时无其他气体产生),下列说法正确的是A.反应后溶液中不存在 |
| B.该合金中铁与铜的物质的量之比是1∶2 |
C.反应后溶液(忽略溶液体积变化)中 |
D.向反应后的溶液中加入2.0 NaOH溶液至金属离子恰好全部沉淀时,需加入NaOH溶液的体积是120mL NaOH溶液至金属离子恰好全部沉淀时,需加入NaOH溶液的体积是120mL |
您最近半年使用:0次
名校
解题方法
3 . 离子化合物 和
和 与水的反应分别为①
与水的反应分别为①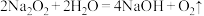 ;②
;②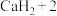
 。下列说法正确的是
。下列说法正确的是
 和
和 与水的反应分别为①
与水的反应分别为①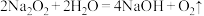 ;②
;②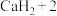
 。下列说法正确的是
。下列说法正确的是A. 、 、 中均有离子键和共价键 中均有离子键和共价键 |
| B.①中水发生氧化反应,②中水发生还原反应 |
C. 中阴、阳离子个数比为1∶2, 中阴、阳离子个数比为1∶2, 中阴、阳离子个数比为2∶1 中阴、阳离子个数比为2∶1 |
D.当反应①和②中转移的电子数相同时,产生的 和 和 的物质的量相同 的物质的量相同 |
您最近半年使用:0次
4 . 化学与人类生产、生活密切相关,利用所学知识进行填空(用 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)下列物质能导电且属于电解质的是___________(填字母)。
(2)NaH可在野外作生氢剂,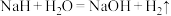 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为___________ 。
(3)标准状况下,44.8L 对应的物质的量是
对应的物质的量是___________ ,含有的化学键类型为___________ 键(填共价键或离子键)。 电子式为:
电子式为:___________ ,CaF2的电子式为:___________ 。
(4)氮的氧化物是大气污染的主要污染物之一,对人类危害很大,每天行驶的汽车排放的尾气中就含有大量的氮氧化物。标准状况下,将盛满二氧化氮的大试管倒扣在盛水的水槽中,充分吸收后,其反应的的化学方程式是___________ ,试管内溶液的物质的量浓度是___________ 。
 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(1)下列物质能导电且属于电解质的是___________(填字母)。
| A.氯化钠固体 | B.熔融的氯化钠 | C.氯化钠溶液 | D.钠 |
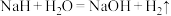 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为(3)标准状况下,44.8L
 对应的物质的量是
对应的物质的量是 电子式为:
电子式为:(4)氮的氧化物是大气污染的主要污染物之一,对人类危害很大,每天行驶的汽车排放的尾气中就含有大量的氮氧化物。标准状况下,将盛满二氧化氮的大试管倒扣在盛水的水槽中,充分吸收后,其反应的的化学方程式是
您最近半年使用:0次
名校
5 . 一种处理温室气体二氧化碳的方法: ,
, 代表阿伏加德罗常数的值。下列说法
代表阿伏加德罗常数的值。下列说法不正确 的是
 ,
, 代表阿伏加德罗常数的值。下列说法
代表阿伏加德罗常数的值。下列说法A.标准状况下,2.24 L  中共用的电子对数为 中共用的电子对数为 |
B.0.1 mol 中含有的电子数为 中含有的电子数为 |
C.生成18 g 转移电子数为 转移电子数为 |
D.1 mol  和2 mol 和2 mol  充分反应生成 充分反应生成 的分子数为 的分子数为 |
您最近半年使用:0次
名校
6 . 铜及其化合物在生产生活有广泛应用,铜在化合物中的常见化合价有+1、+2.已知 与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
(1)工业上可用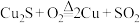 反应制取粗铜,该反应中
反应制取粗铜,该反应中___________ 元素被还原。不考虑杂质的反应,理论上生成1mol的 电子转移的数目为
电子转移的数目为___________
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为___________ 。温度控制在50~60℃的原因除了加快反应速率外,还有___________ 。在 溶液中加入一定量的
溶液中加入一定量的 和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:
和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:___________ 。
(3)现向Cu、 和CuO组成的混合物中,加入2L 0.6
和CuO组成的混合物中,加入2L 0.6
 溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。
溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。 跟稀硝酸反应的离子方程式为
跟稀硝酸反应的离子方程式为___________ 。若将上述混合物用足量的 加热还原,所得到固体的质量为
加热还原,所得到固体的质量为___________ g。若上述混合物中含0.2mol Cu,将该混合物与稀硫酸充分反应,消耗 的物质的量为
的物质的量为___________ mol。
 与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。(1)工业上可用
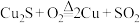 反应制取粗铜,该反应中
反应制取粗铜,该反应中 电子转移的数目为
电子转移的数目为(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入
 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为 溶液中加入一定量的
溶液中加入一定量的 和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:
和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:(3)现向Cu、
 和CuO组成的混合物中,加入2L 0.6
和CuO组成的混合物中,加入2L 0.6
 溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。
溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。 跟稀硝酸反应的离子方程式为
跟稀硝酸反应的离子方程式为 加热还原,所得到固体的质量为
加热还原,所得到固体的质量为 的物质的量为
的物质的量为
您最近半年使用:0次
解题方法
7 . 根据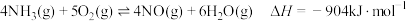 ,下列说法
,下列说法不正确 的是
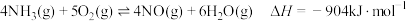 ,下列说法
,下列说法A.反应的 |
B.有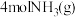 和 和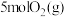 在反应器中充分反应,能放出 在反应器中充分反应,能放出 热量 热量 |
C.断裂1mol 键的同时,断裂 键的同时,断裂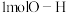 键,说明该反应达到平衡状态 键,说明该反应达到平衡状态 |
D.每消耗 转移电子的数目约为 转移电子的数目约为 |
您最近半年使用:0次
8 . 铁及其化合物与生产、生活关系密切:
(1)下列铁化合物中,可以通过化合反应得到是_______(填字母序号)。
(2) 可作为铜电路板的腐蚀液,该反应的化学方程式
可作为铜电路板的腐蚀液,该反应的化学方程式_______ 。向反应后的溶液加入_______ (填名称),可回收Cu,并得到 溶液。
溶液。
(3)用废铁皮制取( )的部分流程示意图如下:
)的部分流程示意图如下:_______ 。
(4) 可制取新型、高效水处理剂高铁酸钾,反应原理为
可制取新型、高效水处理剂高铁酸钾,反应原理为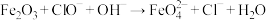 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为_______ 。
(5) 可将氨氮废水中
可将氨氮废水中 的转化为
的转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是_______ 。当该反应转移1.2mol电子时,能产生_______ mol 。
。
(1)下列铁化合物中,可以通过化合反应得到是_______(填字母序号)。
A. | B. | C. | D. |
(2)
 可作为铜电路板的腐蚀液,该反应的化学方程式
可作为铜电路板的腐蚀液,该反应的化学方程式 溶液。
溶液。(3)用废铁皮制取(
 )的部分流程示意图如下:
)的部分流程示意图如下: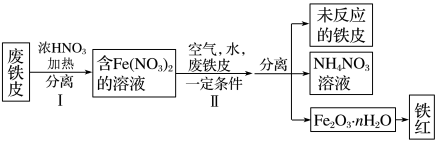
(4)
 可制取新型、高效水处理剂高铁酸钾,反应原理为
可制取新型、高效水处理剂高铁酸钾,反应原理为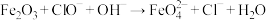 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为(5)
 可将氨氮废水中
可将氨氮废水中 的转化为
的转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是 。
。
您最近半年使用:0次
2024-05-03更新
|
99次组卷
|
2卷引用:福建省晋江市养正中学2023-2024学年高一下学期3月第一次月考化学试题
2024·湖南常德·一模
9 . 基态饿原子( )的价电子排布式为
)的价电子排布式为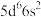 。氧化物
。氧化物 常作烯烃醇化的氧化剂,其重要的氮基饿酸盐有
常作烯烃醇化的氧化剂,其重要的氮基饿酸盐有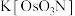 。有关反应如下:
。有关反应如下:
反应I:
反应Ⅱ:
 )的价电子排布式为
)的价电子排布式为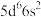 。氧化物
。氧化物 常作烯烃醇化的氧化剂,其重要的氮基饿酸盐有
常作烯烃醇化的氧化剂,其重要的氮基饿酸盐有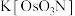 。有关反应如下:
。有关反应如下:反应I:

反应Ⅱ:

反应IⅢ:
A. 的立体异构分子中不存在手性分子 的立体异构分子中不存在手性分子 |
B.反应I中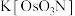 的 的 的化合价为+8 的化合价为+8 |
| C.反应Ⅱ中氧化产物与还原产物的物质的量之比为1∶1 |
D.由反应Ⅲ可推测氧化性: 强于酸性 强于酸性 溶液 溶液 |
您最近半年使用:0次
2024·北京门头沟·一模
解题方法
10 . 为吸收工业尾气中的 和
和 ,设计如图流程,同时还能获得连二亚硫酸钠(
,设计如图流程,同时还能获得连二亚硫酸钠( ,其结晶水合物又称保险粉)和
,其结晶水合物又称保险粉)和 产品。(
产品。( 为铈元素)
为铈元素)不正确 的是
 和
和 ,设计如图流程,同时还能获得连二亚硫酸钠(
,设计如图流程,同时还能获得连二亚硫酸钠( ,其结晶水合物又称保险粉)和
,其结晶水合物又称保险粉)和 产品。(
产品。( 为铈元素)
为铈元素)
A.工业尾气中的 和 和 排放到大气中会形成酸雨 排放到大气中会形成酸雨 |
B.装置Ⅱ的作用是吸收 |
C. 从阴极口流出回到装置Ⅱ循环使用 从阴极口流出回到装置Ⅱ循环使用 |
D.装置Ⅳ中氧化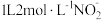 ,至少需要标准状况下 ,至少需要标准状况下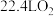 |
您最近半年使用:0次



