1 . 油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄( )褪色的主要原因是发生了以下两种化学反应:
)褪色的主要原因是发生了以下两种化学反应:
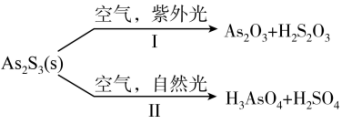
下列说法正确的是
 )褪色的主要原因是发生了以下两种化学反应:
)褪色的主要原因是发生了以下两种化学反应:
下列说法正确的是
A.反应Ⅰ和Ⅱ中,氧化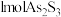 转移的电子数之比为 转移的电子数之比为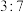 |
B. 和 和 的空间结构都是正四面体形 的空间结构都是正四面体形 |
C.元素 和 和 形成的气态氢化物,键角 形成的气态氢化物,键角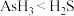 |
D.酸性: |
您最近一年使用:0次
名校
2 . 建筑工地常用的 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O
能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O
(1)配平上述化学方程式,并用双线桥表示电子转移情况____ 。
(2)上述反应的氧化剂是____ ;若有1mol的还原剂被氧化,则反应中转移电子的数目是_______ 。
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别 和
和 ,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。
,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。
(4)某厂废液中,含有2%~5%的 ,直接排放会造成污染,使用
,直接排放会造成污染,使用 处理,能使
处理,能使 转化为不引起二次污染的
转化为不引起二次污染的 ,反应的化学方程式为
,反应的化学方程式为______ 。
(5)以过氧化氢作还原剂,在硫酸介质中还原NaClO3制备ClO2,并将制得的ClO2处理含CN-废水。ClO2处理含CN-废水的离子方程式为______ 。
 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O
能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O(1)配平上述化学方程式,并用双线桥表示电子转移情况
(2)上述反应的氧化剂是
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别
 和
和 ,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。
,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。| A.③⑤ | B.②④ | C.②⑤ | D.①②③⑤ |
 ,直接排放会造成污染,使用
,直接排放会造成污染,使用 处理,能使
处理,能使 转化为不引起二次污染的
转化为不引起二次污染的 ,反应的化学方程式为
,反应的化学方程式为(5)以过氧化氢作还原剂,在硫酸介质中还原NaClO3制备ClO2,并将制得的ClO2处理含CN-废水。ClO2处理含CN-废水的离子方程式为
您最近一年使用:0次
3 . 过二硫酸钾( )是工业上一种重要的消毒剂和织物漂白剂,可通过电解
)是工业上一种重要的消毒剂和织物漂白剂,可通过电解 溶液制备。它在
溶液制备。它在 下能发生分解反应:
下能发生分解反应: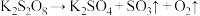 (未配平),设
(未配平),设 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是
 )是工业上一种重要的消毒剂和织物漂白剂,可通过电解
)是工业上一种重要的消毒剂和织物漂白剂,可通过电解 溶液制备。它在
溶液制备。它在 下能发生分解反应:
下能发生分解反应: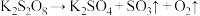 (未配平),设
(未配平),设 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是A.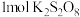 中存在 中存在 个非极性共价键 个非极性共价键 |
B.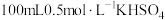 溶液的离子总数为 溶液的离子总数为 |
C.标准状况下,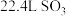 含有的原子数大于 含有的原子数大于 |
D.上述反应,每生成 ,转移 ,转移 个电子 个电子 |
您最近一年使用:0次
2024-02-27更新
|
499次组卷
|
2卷引用:福建省福州市福建师范大学附属中学2024届高三一模化学试题
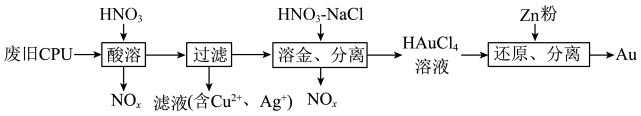
4 . 从废旧CPU中回收Au(金)、Ag、Cu的部分流程如下: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.酸溶时,溶解相同的原料,使用浓硝酸产生的氮氧化物比使用稀硝酸的少 |
| B.向过滤所得滤液中加入过量浓氨水,可以分离Cu2+、Ag+ |
| C.用浓盐酸和浓NaNO3溶液的混合液也可以溶解金 |
| D.向1 mol HAuCl4中加入过量Zn使其完全还原为Au,只需消耗1.5 mol Zn |
您最近一年使用:0次
2024-02-24更新
|
456次组卷
|
3卷引用:福建省泉州市泉港区第二中学2024届高三下学期第一次模拟预测化学试题
名校
5 . 回答下列问题。
(1)神舟十三飞船以 和
和 为动力源,发生反应:
为动力源,发生反应: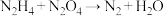 (未配平),反应温度可高达
(未配平),反应温度可高达 ,回答下列问题。
,回答下列问题。
①配平方程式并用双线桥标出电子转移的方向和数目:___________ 。
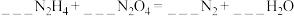 。
。
②氧化产物与还原产物的质量之比为___________ 。
(2)家庭中常用84消毒液(主要成分为 )与洁则灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
)与洁则灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
①“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:___________ 。
②某届奥运会期间,由于工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(1)神舟十三飞船以
 和
和 为动力源,发生反应:
为动力源,发生反应: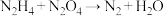 (未配平),反应温度可高达
(未配平),反应温度可高达 ,回答下列问题。
,回答下列问题。①配平方程式并用双线桥标出电子转移的方向和数目:
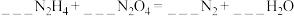 。
。②氧化产物与还原产物的质量之比为
(2)家庭中常用84消毒液(主要成分为
 )与洁则灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
)与洁则灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。| 注意事项: 1.本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用 2.密封保存,请勿与洁厕灵同时使用 3.保质期为一年 |
②某届奥运会期间,由于工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是
 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
名校
6 . 细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。

(1)上图所示氮循环中,属于氮的固定的有___________ (填字母序号)。
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为___________ 。
(3)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为___________ mol。
(4)土壤中的铁循环可用于水体脱氮:脱氮是指将氮元素从水体中除去 ,
①用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:___________ ,
②用离子方程式说明利用土壤中的铁循环脱除水体中硝态氮的原理:___________ 。
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:
将vL气样通入适量酸化的H2O2溶液中,使NO完全被氧化为 。向上述反应后溶液中加入v1mLc1mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为
。向上述反应后溶液中加入v1mLc1mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为 的离子方程式是
的离子方程式是_______ 。上述过程中发生下列反应:3Fe2++ +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O; +6Fe2++14H+=2Cr3++6Fe3++7H2O,则气样中NO的含量为
+6Fe2++14H+=2Cr3++6Fe3++7H2O,则气样中NO的含量为_________ g/L。

(1)上图所示氮循环中,属于氮的固定的有
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
(3)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为
(4)土壤中的铁循环可用于水体脱氮:
①用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:
②用离子方程式说明利用土壤中的铁循环脱除水体中硝态氮的原理:
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:
将vL气样通入适量酸化的H2O2溶液中,使NO完全被氧化为
 。向上述反应后溶液中加入v1mLc1mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为
。向上述反应后溶液中加入v1mLc1mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为 的离子方程式是
的离子方程式是 +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O; +6Fe2++14H+=2Cr3++6Fe3++7H2O,则气样中NO的含量为
+6Fe2++14H+=2Cr3++6Fe3++7H2O,则气样中NO的含量为
您最近一年使用:0次
解题方法
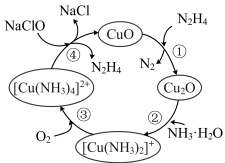
7 . 肼( )可用作锅炉和反应釜的脱氧清洗处理剂,其中一种反应机理如图所示。下列叙述
)可用作锅炉和反应釜的脱氧清洗处理剂,其中一种反应机理如图所示。下列叙述错误 的是
 )可用作锅炉和反应釜的脱氧清洗处理剂,其中一种反应机理如图所示。下列叙述
)可用作锅炉和反应釜的脱氧清洗处理剂,其中一种反应机理如图所示。下列叙述
A.转化①中 是氧化产物 是氧化产物 |
| B.转化②发生了氧化还原反应 |
C.转化③中 是氧化剂 是氧化剂 |
D.转化④中理论上生成 要消耗 要消耗 |
您最近一年使用:0次
解题方法
8 .  与强碱溶液反应时,它的产物取决于强碱溶液的温度。一定条件下足量
与强碱溶液反应时,它的产物取决于强碱溶液的温度。一定条件下足量 与
与 溶液完全反应,测得溶液中
溶液完全反应,测得溶液中 、
、 物质的量之比为
物质的量之比为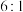 ,则溶液中
,则溶液中 和
和 物质的量之比为
物质的量之比为
 与强碱溶液反应时,它的产物取决于强碱溶液的温度。一定条件下足量
与强碱溶液反应时,它的产物取决于强碱溶液的温度。一定条件下足量 与
与 溶液完全反应,测得溶液中
溶液完全反应,测得溶液中 、
、 物质的量之比为
物质的量之比为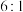 ,则溶液中
,则溶液中 和
和 物质的量之比为
物质的量之比为A. | B. | C.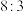 | D. |
您最近一年使用:0次
9 . 微生物反应器去除废水中铵盐和甲烷的过程如图。
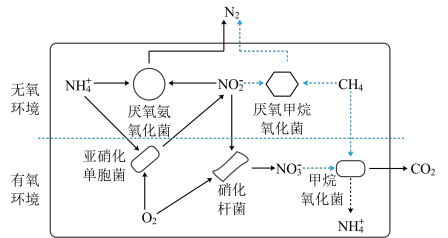
回答下列问题:
(1) 的电离方程式为
的电离方程式为_______ 。
(2)Cu和稀硝酸反应的化学方程式为_______ ,反应过程体现了硝酸性质中的________ 。
(3)在厌氧氨氧化菌作用下,转移 电子时产生
电子时产生 的物质的量为
的物质的量为_______ 。
(4)甲烷属于________ (填“电解质”或“非电解质”)。在酸性废水中,甲烷氧化菌催化甲烷转化的离子方程式为_______ 。

回答下列问题:
(1)
 的电离方程式为
的电离方程式为(2)Cu和稀硝酸反应的化学方程式为
(3)在厌氧氨氧化菌作用下,转移
 电子时产生
电子时产生 的物质的量为
的物质的量为(4)甲烷属于
您最近一年使用:0次
10 . 制备高铁酸钠的反应为 。下列说法不正确的是
。下列说法不正确的是
 。下列说法不正确的是
。下列说法不正确的是A.该反应的还原产物为 | B.氧化剂与还原剂的物质的量之比为 |
C.碱性条件下氧化性: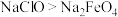 | D.每生成 转移 转移 电子 电子 |
您最近一年使用:0次



