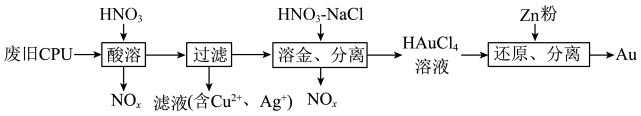
从废旧CPU中回收Au(金)、Ag、Cu的部分流程如下: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.酸溶时,溶解相同的原料,使用浓硝酸产生的氮氧化物比使用稀硝酸的少 |
| B.向过滤所得滤液中加入过量浓氨水,可以分离Cu2+、Ag+ |
| C.用浓盐酸和浓NaNO3溶液的混合液也可以溶解金 |
| D.向1 mol HAuCl4中加入过量Zn使其完全还原为Au,只需消耗1.5 mol Zn |
更新时间:2024-02-24 11:17:02
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】不溶于水的氧化亚铜可溶于含硫酸铁的硫酸溶液中,这时生成的硫酸亚铁可用酸性高锰酸钾溶液滴定,从而测定氧化亚铜的量:Cu2O+Fe2(SO4)3+H2SO4——FeSO4+CuSO4+H2O FeSO4+KMnO4+H2SO4——Fe2(SO4)3+MnSO4+K2SO4+H2O 由上述反应知;0.1mol/L的KMnO4溶液1mL相当于氧化亚铜的量是
| A.360mg | B.3.6g | C.0.36g | D.2.5×10-4mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】某温度下,将氯气通入到氢氧化钠溶液中,反应得到NaCl,NaClO,NaClO3的混合溶液,经测定溶液中c(ClO)∶c(ClO)=1∶3.则氯气与氢氧化钠溶液反应时被还原的氯原子与被氧化的氯原于的数目之比为
| A.21:5 | B.4:1 | C.3:1 | D.11:3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】向2L的 和
和 的混合稀溶液中逐渐加入铁粉,产生无色气体,该气体遇到空气变为红棕色,溶液中
的混合稀溶液中逐渐加入铁粉,产生无色气体,该气体遇到空气变为红棕色,溶液中 的物质的量和加入Fe粉的物质的量之间的关系如图所示,下列叙述错误的是
的物质的量和加入Fe粉的物质的量之间的关系如图所示,下列叙述错误的是

 和
和 的混合稀溶液中逐渐加入铁粉,产生无色气体,该气体遇到空气变为红棕色,溶液中
的混合稀溶液中逐渐加入铁粉,产生无色气体,该气体遇到空气变为红棕色,溶液中 的物质的量和加入Fe粉的物质的量之间的关系如图所示,下列叙述错误的是
的物质的量和加入Fe粉的物质的量之间的关系如图所示,下列叙述错误的是
A.开始时加入铁粉反应的离子方程式为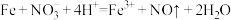 |
B.加入4mol铁粉时,溶液中有2mol  ,3mol ,3mol  |
| C.加入5mol铁粉后的溶液中加入盐酸,会有NO气体产生 |
D.原溶液中 和 和 的物质的量分别为6mol和1mol 的物质的量分别为6mol和1mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】将一定质量的镁铝合金投入100mL稀硝酸中完全溶解,反应过程中无气体放出。向反应后的溶液中,逐滴加入1.00 mol/L NaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量关系如图所示,则下列说法错误的是


| A.合金中镁铝的物质的量之比为1:2 |
| B.合金完全溶解转移电子的物质的量为0.032mol |
| C.原稀硝酸的物质的量浓度为0.45 mol/L |
| D.F点溶液中,溶质仅为Na[Al(OH)4] |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】根据下列框图分析,下列说法正确的是

| A.E2+的氧化性比M2+的氧化性强 |
| B.在③反应中若不加稀硫酸可能看到红褐色沉淀 |
C.反应④的离子方程式可表示为: E3+ +3SCN- E(SCN)3↓ E(SCN)3↓ |
| D.在反应①中只能用浓硫酸,既表现了酸性、又表现了氧化性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列有关含硫物质转化判断正确的是

| A.0.1molCu与足量的硫充分反应,生成物的质量比该单质的质量增加了1.6g |
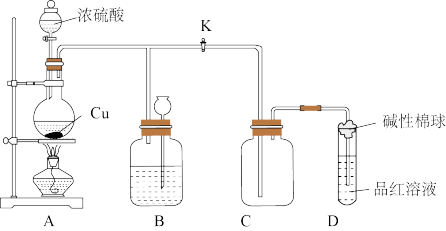
| B.如图是铜与浓硫酸反应的实验装置。B中盛装的是浓硫酸,作用是干燥SO2 |
| C.Cu投入稀硫酸中加热,没有明显变化,加入一定量的H2O2溶液,金属Cu逐渐溶解,反应中H2O2起催化作用 |
D.25.0mL0.100mol•L-1的Na2S2O3溶液恰好把224mL(标况)Cl2转化为Cl-,则S2O 将转化为S 将转化为S |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】结构与组成的变化可以引起性能的变化,下列推测不合理 的是
| 材料 | 结构和组成变化 | 性能变化 | |
| A | 生铁 | 减少含碳量 | 增强延展性 |
| B | 玻璃 | 加入硼酸盐 | 耐温度急剧变化 |
| C | 纤维素 | 接入带有强亲水基团的支链 | 提高吸水能力 |
| D | 冠醚 |
| 增大识别的阳离子半径 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某企业以辉铜矿为原料生产碱式碳酸铜,工艺流程如下所示:
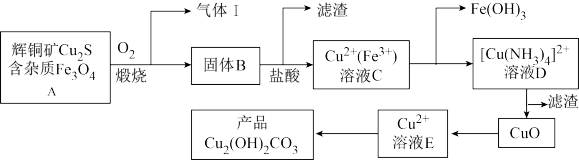
已知: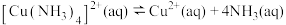
根据以上工艺流程,下列说法不正确的是

已知:
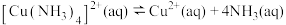
根据以上工艺流程,下列说法不正确的是
A.为实现溶液C到溶液D的转化,加入过量 后过滤即可 后过滤即可 |
| B.溶液E和碳酸钠混合方式不同对产品的成分没有影响 |
C.在制备产品时,溶液D中不直接加入 溶液的原因是游离的 溶液的原因是游离的 浓度太低 浓度太低 |
D.蒸氨过程发生总反应的化学方程式为: |
您最近一年使用:0次

 和1mol
和1mol 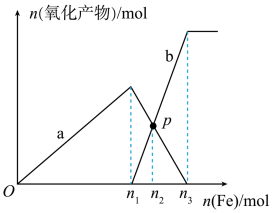
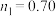
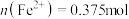
 改成
改成
 ,含
,含 杂质]合成
杂质]合成 目标产物的流程如下。下列说法正确的是
目标产物的流程如下。下列说法正确的是
 中煅烧产生气体的主要成分:
中煅烧产生气体的主要成分:
 中溶质的主要成分:
中溶质的主要成分: 和
和



