细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。

(1)上图所示氮循环中,属于氮的固定的有___________ (填字母序号)。
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为___________ 。
(3)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为___________ mol。
(4)土壤中的铁循环可用于水体脱氮:脱氮是指将氮元素从水体中除去 ,
①用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:___________ ,
②用离子方程式说明利用土壤中的铁循环脱除水体中硝态氮的原理:___________ 。
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:
将vL气样通入适量酸化的H2O2溶液中,使NO完全被氧化为 。向上述反应后溶液中加入v1mLc1mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为
。向上述反应后溶液中加入v1mLc1mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为 的离子方程式是
的离子方程式是_______ 。上述过程中发生下列反应:3Fe2++ +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O; +6Fe2++14H+=2Cr3++6Fe3++7H2O,则气样中NO的含量为
+6Fe2++14H+=2Cr3++6Fe3++7H2O,则气样中NO的含量为_________ g/L。

(1)上图所示氮循环中,属于氮的固定的有
a.N2转化为氨态氮 b.硝化过程 c.反硝化过程
(2)氮肥是水体中氨态氮的主要来源之一,氨气是生产氮肥的主要原料,工业合成氨的化学方程式为
(3)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为
(4)土壤中的铁循环可用于水体脱氮:
①用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理:
②用离子方程式说明利用土壤中的铁循环脱除水体中硝态氮的原理:
(5)NO是大气污染气体,测定某气体样品中NO含量操作如下:
将vL气样通入适量酸化的H2O2溶液中,使NO完全被氧化为
 。向上述反应后溶液中加入v1mLc1mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为
。向上述反应后溶液中加入v1mLc1mol·L−1FeSO4溶液(过量),充分反应后,多余Fe2+与v2mL、c2mol·L−1K2Cr2O7恰好反应。NO被H2O2氧化为 的离子方程式是
的离子方程式是 +4H+=NO↑+3Fe3++2H2O;
+4H+=NO↑+3Fe3++2H2O; +6Fe2++14H+=2Cr3++6Fe3++7H2O,则气样中NO的含量为
+6Fe2++14H+=2Cr3++6Fe3++7H2O,则气样中NO的含量为
更新时间:2024-02-20 15:18:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)按要求填空。
①碳酸钙和盐酸(写出离子方程式)
___________________________________________________________________ 。
②氢氧化钡溶液和硫酸铜溶液(写出离子方程式)
___________________________________________________________________ 。
③Fe2(SO4)3(写出电离方程式)
___________________________________________________________________ 。
④H++OH- H2O(写出对应的化学方程式)
H2O(写出对应的化学方程式)
___________________________________________________________________ 。
⑤CO32-+2H+ CO2↑+H2O(写出对应的化学方程式)
CO2↑+H2O(写出对应的化学方程式) ________________________ 。
(2)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2H++Zn Zn2++H2↑的拆写结果是:氧化反应为Zn-2e-
Zn2++H2↑的拆写结果是:氧化反应为Zn-2e- Zn2+;还原反应为2H++2e-
Zn2+;还原反应为2H++2e- H2↑。
H2↑。
①请据此将反应:2Fe3++Cu 2Fe2++Cu2+拆写成两个“半反应式”。
2Fe2++Cu2+拆写成两个“半反应式”。
氧化反应为_________________________________________________________ ;
还原反应为_________________________________________________________ 。
②已知某一氧化还原反应,其中氧化反应的半反应可写为Fe-2e- Fe2+;还原反应的半反应可写为2Fe3++2e-
Fe2+;还原反应的半反应可写为2Fe3++2e- 2Fe2+;则此氧化还原反应为
2Fe2+;则此氧化还原反应为________________ 。
①碳酸钙和盐酸(写出离子方程式)
②氢氧化钡溶液和硫酸铜溶液(写出离子方程式)
③Fe2(SO4)3(写出电离方程式)
④H++OH-
 H2O(写出对应的化学方程式)
H2O(写出对应的化学方程式)⑤CO32-+2H+
 CO2↑+H2O(写出对应的化学方程式)
CO2↑+H2O(写出对应的化学方程式) (2)一个完整的氧化还原反应方程式可以拆开写成两个“半反应式”,一个是“氧化反应”式,一个是“还原反应”式。如2H++Zn
 Zn2++H2↑的拆写结果是:氧化反应为Zn-2e-
Zn2++H2↑的拆写结果是:氧化反应为Zn-2e- Zn2+;还原反应为2H++2e-
Zn2+;还原反应为2H++2e- H2↑。
H2↑。①请据此将反应:2Fe3++Cu
 2Fe2++Cu2+拆写成两个“半反应式”。
2Fe2++Cu2+拆写成两个“半反应式”。氧化反应为
还原反应为
②已知某一氧化还原反应,其中氧化反应的半反应可写为Fe-2e-
 Fe2+;还原反应的半反应可写为2Fe3++2e-
Fe2+;还原反应的半反应可写为2Fe3++2e- 2Fe2+;则此氧化还原反应为
2Fe2+;则此氧化还原反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】图中两圆相交部分(A、B、C、D)表示铁、稀盐酸、澄清石灰水、氯化铜溶液彼此之间的反应关系,写出对应的离子反应方程式。

(1)A_______ 、B_______ 、C_______ 、D_______
(2)用双线桥标出上述氧化还原反应中电子转移的方向和数目。_______
(3)自来水中的 对人类健康会产生危害,碱性条件下用Al粉还原
对人类健康会产生危害,碱性条件下用Al粉还原 ,产物是N2,发生的反应可表示如下,完成方程式并配平。
,产物是N2,发生的反应可表示如下,完成方程式并配平。_____ Al+ _____  +
+ ________ = _____  +
+_____ N2↑ +_____

(1)A
(2)用双线桥标出上述氧化还原反应中电子转移的方向和数目。
(3)自来水中的
 对人类健康会产生危害,碱性条件下用Al粉还原
对人类健康会产生危害,碱性条件下用Al粉还原 ,产物是N2,发生的反应可表示如下,完成方程式并配平。
,产物是N2,发生的反应可表示如下,完成方程式并配平。 +
+  +
+
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。根据所学知识回答下列问题:
(1) 是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验
是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验 是否泄漏,有关反应的化学方程式为
是否泄漏,有关反应的化学方程式为 ,该反应中氧化剂为
,该反应中氧化剂为___________ (填化学式),标准状况下,每生成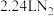 ,反应中转移的电子的物质的量为
,反应中转移的电子的物质的量为___________  。
。
(2)在一定条件下, 可与
可与 发生反应:
发生反应: ,在此过程中
,在此过程中 被
被___________ (填“氧化”或“还原”), 中
中 的化合价是
的化合价是___________ 价。
(3)某一反应体系有反应物和生成物共七种物质: 、
、 、
、 、
、 、
、 、
、 、
、 ,已知该反应中有气体生成。
,已知该反应中有气体生成。
①该反应中的还原剂是___________ (填化学式,下同),被还原的物质为___________ 。
②写出该反应的化学方程式:___________ 。
(1)
 是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验
是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验 是否泄漏,有关反应的化学方程式为
是否泄漏,有关反应的化学方程式为 ,该反应中氧化剂为
,该反应中氧化剂为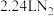 ,反应中转移的电子的物质的量为
,反应中转移的电子的物质的量为 。
。(2)在一定条件下,
 可与
可与 发生反应:
发生反应: ,在此过程中
,在此过程中 被
被 中
中 的化合价是
的化合价是(3)某一反应体系有反应物和生成物共七种物质:
 、
、 、
、 、
、 、
、 、
、 、
、 ,已知该反应中有气体生成。
,已知该反应中有气体生成。①该反应中的还原剂是
②写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】将过量的铜置入一定量的浓硝酸中,充分反应后放出11.2 L气体(标准状况下),试回答下列问题:
(1)反应放出的气体中,含有_____________ (写化学式);
(2)写出反应过程中的的化学方程式:___________________________ ;
(3)若有19.2g铜溶解,则参加反应的HNO3的物质的量__________ 被还原HNO3的质量为______________
(1)反应放出的气体中,含有
(2)写出反应过程中的的化学方程式:
(3)若有19.2g铜溶解,则参加反应的HNO3的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)下列反应中都有水参加:
A.Cl2+ H2O +Na2SO3=2HCl + Na2SO4
B.3NO2 + H2O = 2HNO3 + NO↑
C.NaH +H2O = NaOH + H2↑
D.2H2O电解2H2↑+ O2↑
其中,水只是氧化剂的是_________ ,水既不是氧化剂又不是还原剂的是_________ ;
(2)在3BrF3+5H2O=9HF+HBrO3+O2↑+Br2反应中,若有5.4gH2O被氧化,则被还原的BrF3共______________ mol,其中被水还原的BrF3是_______________ mol。
A.Cl2+ H2O +Na2SO3=2HCl + Na2SO4
B.3NO2 + H2O = 2HNO3 + NO↑
C.NaH +H2O = NaOH + H2↑
D.2H2O电解2H2↑+ O2↑
其中,水只是氧化剂的是
(2)在3BrF3+5H2O=9HF+HBrO3+O2↑+Br2反应中,若有5.4gH2O被氧化,则被还原的BrF3共
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氮元素是地球大气中含量最多的元素,请完成下列有关问题
(1)写出氮元素的原子结构示意图:_____ 。
(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现固氮的是_____ 。
(3)写出实验室制取氨气的化学反应方程式_____ 。
(4)如图是实验室制取氨气的装置,请指出图中错误之处:_____ 。

(5)用如图装置进行喷泉实验,挤压滴管的胶头时,现象_____ 。

(6)若实验室要收集一定量的氨气应用什么方法收集:_____ 。
(7)请写出氨气的催化氧化反应方程式:_____ 。
(8)在如图所示的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是_____ (填字母)。

(9)在图示锥形瓶外放一水槽,瓶中加入酒精,水槽中加入水后,再加入足量的下列物质,结果也产生喷泉。水槽中加入的物质可以是_____ (填字母)。

(1)写出氮元素的原子结构示意图:
(2)将空气中的氮气转化为氮的化合物的过程称为固氮。下列能实现固氮的是
| A.N2和H2在一定条件下反应生成NH3 | B.雷雨闪电时空气中的N2和O2化合生成NO |
| C.NH3经过催化氧化生成NO | D.NH3和HNO3反应生成NH4NO3 |
(4)如图是实验室制取氨气的装置,请指出图中错误之处:

(5)用如图装置进行喷泉实验,挤压滴管的胶头时,现象

(6)若实验室要收集一定量的氨气应用什么方法收集:
(7)请写出氨气的催化氧化反应方程式:
(8)在如图所示的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是

| A.Cu与稀盐酸 | B.NaHCO3与NaOH溶液 | C.CaCO3与稀硫酸 | D.NH4HCO3与稀盐酸 |

| A.浓硫酸 | B.食盐 | C.硝酸钾 | D.硫酸 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.完成下列问题
(1)火山喷发中形成的 和
和 也会发生反应形成硫。
也会发生反应形成硫。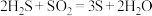
①请标出该反应的电子转移方向和数目__________ ;
②该反应的氧化剂是___________ ,氧化产物和还原产物的比例为___________ 。
(2)大气中的水能结合 生成亚硫酸,被氧化后形成酸雨,请写出生成亚硫酸的方程式为:
生成亚硫酸,被氧化后形成酸雨,请写出生成亚硫酸的方程式为:___________ 。
Ⅱ.氮循环是指氮在自然界中的循环转化过程,是生物圈内基本的物质循环之一,
(3)下列不属于氮的固定的是___________
(4) 与
与 结构相似,
结构相似, 电子式为
电子式为___________ ,  空间构型为
空间构型为___________ 。对“ ” “P”元素及其化合物相关性质进行比较,下列说法不正确的是
” “P”元素及其化合物相关性质进行比较,下列说法不正确的是___________ 。
A.原子半径大小: B.原子得电子的能力:
B.原子得电子的能力:
C.气态氢化物的热稳定性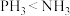 D.最高价氧化物对应水化物的酸性
D.最高价氧化物对应水化物的酸性
(5)下列属于铵态氮肥的是___________。
(6)氮循环和硫循环是自然界中两种重要的元素循环过程。请选出下表中关于这两种循环的正确评价___________ 。任选其中一种错误评价,解释判断理由:_________
(1)火山喷发中形成的
 和
和 也会发生反应形成硫。
也会发生反应形成硫。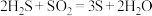
①请标出该反应的电子转移方向和数目
②该反应的氧化剂是
(2)大气中的水能结合
 生成亚硫酸,被氧化后形成酸雨,请写出生成亚硫酸的方程式为:
生成亚硫酸,被氧化后形成酸雨,请写出生成亚硫酸的方程式为:Ⅱ.氮循环是指氮在自然界中的循环转化过程,是生物圈内基本的物质循环之一,
(3)下列不属于氮的固定的是___________
A.N2+O2 2NO 2NO | B. |
C.N2+3H2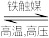 2NH3 2NH3 | D.3Mg+N2 Mg3N2 Mg3N2 |
 与
与 结构相似,
结构相似, 电子式为
电子式为 空间构型为
空间构型为 ” “P”元素及其化合物相关性质进行比较,下列说法不正确的是
” “P”元素及其化合物相关性质进行比较,下列说法不正确的是A.原子半径大小:
 B.原子得电子的能力:
B.原子得电子的能力:
C.气态氢化物的热稳定性
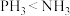 D.最高价氧化物对应水化物的酸性
D.最高价氧化物对应水化物的酸性
(5)下列属于铵态氮肥的是___________。
| A.尿素 | B.硝酸 | C.硝酸铵 | D.氨气 |
| 编号 | 比较 | 氮循环 | 硫循环 |
| A | 异 | 氮元素会进入大气 | 硫循环不会进入大气 |
| B | 氮元素可以有机化合物形式参与循环 | 硫元素都以无机化合物形式参与循环 | |
| C | 同 | 人类活动对氮循环和硫循环都造成了巨大影响 | |
| D | 氮循环和硫循环对环境影响都导致温室效应 | ||
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】近日,菏泽空气质量堪忧,研究SO2、NOx等对改善空气质量具有重要意义。请回答下列问题:
(1)NOx是汽车尾气中的主要污染物之一。
①NOx能形成酸雨,由NO2形成的酸雨中含有的主要离子有_____________ 。
②汽车发动机工作时会引发N2和O2反应,反应的化学方程式是___________ 。
(2)为减少SO2的排放,常采取一些有效措施。
①在含硫煤中加入生石灰可以起到固硫的作用,燃烧过程中,硫元素转化成其最高价态的化合物,该化合物的化学式是______________ 。
②下列物质中,可用于吸收烟气中的SO2的是________ (填序号)。
a.Na2CO3 b.H2SO4 c.NaHSO3 d.NH3·H2O
(3)取某空气样本用蒸馏水处理制成待测液,其中所含的离子及其浓度如下:
根据表中数据计算:a=___________ mol/L。
(1)NOx是汽车尾气中的主要污染物之一。
①NOx能形成酸雨,由NO2形成的酸雨中含有的主要离子有
②汽车发动机工作时会引发N2和O2反应,反应的化学方程式是
(2)为减少SO2的排放,常采取一些有效措施。
①在含硫煤中加入生石灰可以起到固硫的作用,燃烧过程中,硫元素转化成其最高价态的化合物,该化合物的化学式是
②下列物质中,可用于吸收烟气中的SO2的是
a.Na2CO3 b.H2SO4 c.NaHSO3 d.NH3·H2O
(3)取某空气样本用蒸馏水处理制成待测液,其中所含的离子及其浓度如下:
| 离子 | K+ | Na+ | NH | H+ | SO | NO | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | a | 4×10-5 | 3×10-5 | 2×10-5 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】64.0gCu与200mL10.0mol·L-1的浓硝酸反应,标准状况下测得反应产生的NO、NO2混合气体13.44L,且充分反应后铜仍有剩余。请计算:
(1)混合气体中NO与NO2的物质的量之比为___________ ;
(2)向反应后的溶液中滴加稀硫酸可使铜完全溶解,若该过程中只有NO气体生成,则还能产生NO的物质的量为___________ 。
(3)若铜完全反应,最终溶液中铜离子的物质的量浓度是______ (假设溶液体积变化忽略不计)
(1)混合气体中NO与NO2的物质的量之比为
(2)向反应后的溶液中滴加稀硫酸可使铜完全溶解,若该过程中只有NO气体生成,则还能产生NO的物质的量为
(3)若铜完全反应,最终溶液中铜离子的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
(1)电解氧化吸收法可将废气中的 NOx转变为NO 。电解NaCl溶液时,溶液中相关成分的浓度变化与电流强度的关系如下图所示。
。电解NaCl溶液时,溶液中相关成分的浓度变化与电流强度的关系如下图所示。

电解NaCl溶液作为吸收液,若电流强度为4A,吸收NO的反应离子方程式为___________ 。
(2)某氮肥厂处理氨氮废水的方案如图,回答下列问题:
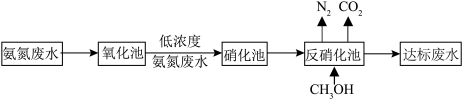
“反硝化池”中发生的变化为:HNO3→ →N2。1 mol HNO3完全转化理论上消耗甲醇的质量为
→N2。1 mol HNO3完全转化理论上消耗甲醇的质量为___________ 。
(3)纳米Fe 可还原去除水中的硝酸盐污染物。转化关系如下:





①检验还原后的溶液中存在 的实验方法是
的实验方法是___________ 。
②溶液初始 pH 较低有利于 的去除,其可能的原因是
的去除,其可能的原因是___________ 。
(1)电解氧化吸收法可将废气中的 NOx转变为NO
 。电解NaCl溶液时,溶液中相关成分的浓度变化与电流强度的关系如下图所示。
。电解NaCl溶液时,溶液中相关成分的浓度变化与电流强度的关系如下图所示。
电解NaCl溶液作为吸收液,若电流强度为4A,吸收NO的反应离子方程式为
(2)某氮肥厂处理氨氮废水的方案如图,回答下列问题:

“反硝化池”中发生的变化为:HNO3→
 →N2。1 mol HNO3完全转化理论上消耗甲醇的质量为
→N2。1 mol HNO3完全转化理论上消耗甲醇的质量为(3)纳米Fe 可还原去除水中的硝酸盐污染物。转化关系如下:





①检验还原后的溶液中存在
 的实验方法是
的实验方法是②溶液初始 pH 较低有利于
 的去除,其可能的原因是
的去除,其可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)SiO2在自然界中广泛存在,它是制备现代通讯材料___________ (写该材料名称)的主要原料;以SiO2为原料,在工业上制备单质硅的化学方程式为___________ ;
(2)在常温下,SiO2可与一种酸发生反应,该反应的化学方程式为___________ 。该反应的重要应用是___________ 。
(3)在一定体积的18 mol/L的浓硫酸加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积___________ (填“大于”“小于”或“等于”)100 mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式___________ 。
(2)在常温下,SiO2可与一种酸发生反应,该反应的化学方程式为
(3)在一定体积的18 mol/L的浓硫酸加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积
您最近一年使用:0次

 溶液中加入氨水的离子方程式
溶液中加入氨水的离子方程式 溶液中加入少量氢氧化钠溶液的离子方程式
溶液中加入少量氢氧化钠溶液的离子方程式 和二氧化碳气体按照6∶5反应的离子方程式
和二氧化碳气体按照6∶5反应的离子方程式 溶液中加入过量
溶液中加入过量 溶液的离子方程式
溶液的离子方程式

