名校
1 . 高铁酸钾 是一种暗紫色固体,在强碱性溶液中稳定,但在
是一种暗紫色固体,在强碱性溶液中稳定,但在 催化作用下会发生分解反应,常用作水处理剂。某兴趣小组利用废铁屑(含少量
催化作用下会发生分解反应,常用作水处理剂。某兴趣小组利用废铁屑(含少量 、
、 等)制备高铁酸钾的工艺流程如图所示:
等)制备高铁酸钾的工艺流程如图所示: 属于
属于______ (填“酸”“碱”“盐”或“氧化物”),其中铁元素的化合价为______ 价。
(2)加入 的目的是调节pH除铝,同时有气体生成,反应的离子方程式为
的目的是调节pH除铝,同时有气体生成,反应的离子方程式为______ 。
(3)“氧化Ⅰ”发生反应的离子方程式为______ 。
(4)“氧化Ⅱ”过程中每生成lmol 转移
转移______ mol电子。
(5)水处理时,加入 作为净水消毒剂,发生反应的化学方程式:
作为净水消毒剂,发生反应的化学方程式:
①将______ 上述氧化还原反应配平;
②由此可知 能用于消毒净水的原因是
能用于消毒净水的原因是______ 。
(6)向 溶液中滴加6
溶液中滴加6 盐酸,产生黄绿色气体,说明
盐酸,产生黄绿色气体,说明 的氧化性
的氧化性______ (填“强”或“弱”)于 。另一种制备
。另一种制备 的反应原理为:
的反应原理为: ,请分析
,请分析 和
和 的氧化性强弱关系相反的原因是
的氧化性强弱关系相反的原因是______ 。
 是一种暗紫色固体,在强碱性溶液中稳定,但在
是一种暗紫色固体,在强碱性溶液中稳定,但在 催化作用下会发生分解反应,常用作水处理剂。某兴趣小组利用废铁屑(含少量
催化作用下会发生分解反应,常用作水处理剂。某兴趣小组利用废铁屑(含少量 、
、 等)制备高铁酸钾的工艺流程如图所示:
等)制备高铁酸钾的工艺流程如图所示:
 属于
属于(2)加入
 的目的是调节pH除铝,同时有气体生成,反应的离子方程式为
的目的是调节pH除铝,同时有气体生成,反应的离子方程式为(3)“氧化Ⅰ”发生反应的离子方程式为
(4)“氧化Ⅱ”过程中每生成lmol
 转移
转移(5)水处理时,加入
 作为净水消毒剂,发生反应的化学方程式:
作为净水消毒剂,发生反应的化学方程式:
①将
②由此可知
 能用于消毒净水的原因是
能用于消毒净水的原因是(6)向
 溶液中滴加6
溶液中滴加6 盐酸,产生黄绿色气体,说明
盐酸,产生黄绿色气体,说明 的氧化性
的氧化性 。另一种制备
。另一种制备 的反应原理为:
的反应原理为: ,请分析
,请分析 和
和 的氧化性强弱关系相反的原因是
的氧化性强弱关系相反的原因是
您最近一年使用:0次
名校
2 .  为阿伏伽德罗常数,下列说法正确的是
为阿伏伽德罗常数,下列说法正确的是
 为阿伏伽德罗常数,下列说法正确的是
为阿伏伽德罗常数,下列说法正确的是A.在22.4L NO、 的混合气体中,N原子数为 的混合气体中,N原子数为 |
B.Cu与足量稀硝酸反应后, ,转移的电子总数为0.2 ,转移的电子总数为0.2 |
C.18g  中的质子数为11 中的质子数为11 |
D.5.6g Fe先与足量盐酸反应,再往反应后的溶液中滴加足量NaOH溶液,静置一段时间后, 、 、 的总数为0.5 的总数为0.5 |
您最近一年使用:0次
3 .  是一种储氢材料,它易与水发生氧化还原反应。缓慢升温至
是一种储氢材料,它易与水发生氧化还原反应。缓慢升温至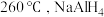 发生如下反应:
发生如下反应:
①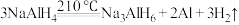
②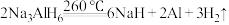
下列说法错误的是
 是一种储氢材料,它易与水发生氧化还原反应。缓慢升温至
是一种储氢材料,它易与水发生氧化还原反应。缓慢升温至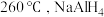 发生如下反应:
发生如下反应:①
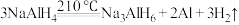
②
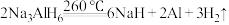
下列说法错误的是
A.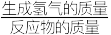 :反应①>反应② :反应①>反应② |
B. 存在离子键、共价键和配位键 存在离子键、共价键和配位键 |
C.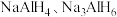 和 和 均易与水反应生成氢气 均易与水反应生成氢气 |
D.反应①生成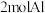 ,有 ,有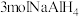 被氧化 被氧化 |
您最近一年使用:0次
2024-04-13更新
|
178次组卷
|
2卷引用:福建省莆田市2024届高三下学期毕业班二模考试化学试题
4 . 已知A为淡黄色固体,C是无色无味气体,T为生活中使用最广泛的金属单质,D是具有磁性的黑色晶体,J为84消毒液有效成分,F为红褐色沉淀。
注:磁性氧化铁中含有Fe3+、Fe2+,其个数之比为2∶1。
I.请回答:
(1)A中阴阳离子个数比是___________ 。
(2)写出D→E先后加入足量盐酸、再与足量M反应发生的离子方程式___________ 、___________ 。
II.高铁酸钠(Na2FeO4)是一种高效多功能的新型非氯绿色消毒剂,主要用于饮用水的处理,可由J、B、F反应制得。
(3)Na2FeO4属于___________ (填字母)。
A.钠盐 B.酸式盐 C.铁盐 D.强电解质 E.弱电解质
(4)高铁酸钠溶液杀菌后可得到氢氧化铁胶体,进而起到净水作用,当有0.5mol Na2FeO4参与杀菌消毒并完全反应时,转移的电子数为___________ 。
(5)下列关于氢氧化铁胶体的说法中正确的是___________ (填字母)。
A.氢氧化铁胶体带正电荷,可以发生电泳现象
B.向氢氧化铁胶体中逐滴滴加稀硫酸,可观察到先出现红褐色沉淀,后沉淀消失
C.实验室制备氢氧化铁胶体的化学方程式为:FeCl3+3H2O Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
D.1mol Na2FeO4完全转化为Fe(OH)3胶体后,含有的胶体粒子数目为NA
E.氢氧化铁胶粒不可以通过滤纸,但可通过半透膜,此为渗析的原理
注:磁性氧化铁中含有Fe3+、Fe2+,其个数之比为2∶1。
I.请回答:
(1)A中阴阳离子个数比是
(2)写出D→E先后加入足量盐酸、再与足量M反应发生的离子方程式
II.高铁酸钠(Na2FeO4)是一种高效多功能的新型非氯绿色消毒剂,主要用于饮用水的处理,可由J、B、F反应制得。
(3)Na2FeO4属于
A.钠盐 B.酸式盐 C.铁盐 D.强电解质 E.弱电解质
(4)高铁酸钠溶液杀菌后可得到氢氧化铁胶体,进而起到净水作用,当有0.5mol Na2FeO4参与杀菌消毒并完全反应时,转移的电子数为
(5)下列关于氢氧化铁胶体的说法中正确的是
A.氢氧化铁胶体带正电荷,可以发生电泳现象
B.向氢氧化铁胶体中逐滴滴加稀硫酸,可观察到先出现红褐色沉淀,后沉淀消失
C.实验室制备氢氧化铁胶体的化学方程式为:FeCl3+3H2O
 Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HClD.1mol Na2FeO4完全转化为Fe(OH)3胶体后,含有的胶体粒子数目为NA
E.氢氧化铁胶粒不可以通过滤纸,但可通过半透膜,此为渗析的原理
您最近一年使用:0次
解题方法
5 . 利用烟气中的SO2可回收废水中的I-,实现碘单质的再生,其反应原理如图所示。下列说法正确的是
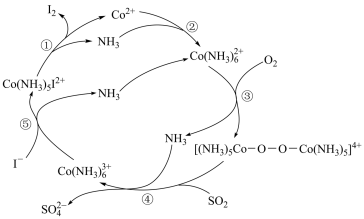

A.1mol SO 中含有电子的数目为48NA 中含有电子的数目为48NA |
| B.NH3溶于水能导电,NH3属于电解质 |
| C.反应①~⑤中均属于氧化还原反应 |
D.总反应离子方程式为: |
您最近一年使用:0次
6 . 反应8NH33Cl2N26NH4Cl,下列说法正确的是
| A.Cl2 发生氧化反应 |
| B.NH3 既是氧化剂又是还原剂 |
| C.每生成22.4L N2,转移的电子数为6NA |
| D.被氧化的NH3与被还原的Cl2的化学计量数之比为 2∶3 |
您最近一年使用:0次
名校
解题方法
7 . 向含有amolCu,bmolCu2O的混合物中滴加3mol/L的稀硝酸溶液至20mL时,固体恰好完全溶解,得到标准状况下224mL气体(纯净物)。下列说法正确的是
| A.a=0.005mol |
| B.a:b=1:1 |
| C.反应过程中转移0.2mol电子 |
| D.被还原的硝酸为0.06mol |
您最近一年使用:0次
解题方法
8 . PtNiFe-LDHGO催化甲醛氧化的反应机理如图:
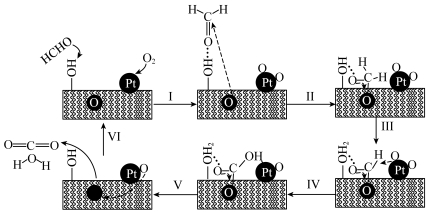
下列说法错误的是

下列说法错误的是
A.步骤Ⅰ中甲醛通过氢键吸附在催化剂表面的 上 上 |
| B.上述反应机理涉及极性键和非极性键的形成 |
C.该反应每生成  ,转移 ,转移 电子 电子 |
| D.PtNiFe-LDHGO降低了该反应的活化能 |
您最近一年使用:0次
2024·湖南常德·一模
9 . 基态锇原子( )的价电子排布式为
)的价电子排布式为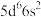 。氧化物
。氧化物 常作烯烃醇化的氧化剂,其重要的氮基锇酸盐有
常作烯烃醇化的氧化剂,其重要的氮基锇酸盐有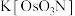 。有关反应如下:
。有关反应如下:
反应I:
反应Ⅱ:
 )的价电子排布式为
)的价电子排布式为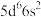 。氧化物
。氧化物 常作烯烃醇化的氧化剂,其重要的氮基锇酸盐有
常作烯烃醇化的氧化剂,其重要的氮基锇酸盐有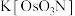 。有关反应如下:
。有关反应如下:反应I:

反应Ⅱ:

反应IⅢ:
A. 的立体异构分子中不存在手性分子 的立体异构分子中不存在手性分子 |
B.反应I中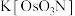 的 的 的化合价为+8 的化合价为+8 |
| C.反应Ⅱ中氧化产物与还原产物的物质的量之比为1∶1 |
D.由反应Ⅲ可推测氧化性: 强于酸性 强于酸性 溶液 溶液 |
您最近一年使用:0次
解题方法
10 .  是化学工业中广泛使用的一种高效的漂白剂和氧化剂,工业上生产它的一种流程如图所示:
是化学工业中广泛使用的一种高效的漂白剂和氧化剂,工业上生产它的一种流程如图所示:

(1) 的名称是
的名称是___________ ,若A是一种纯净物,则A的化学式为___________ 。
(2)“还原1”中应充分搅拌,好处是___________ ,反应中消耗的氧化剂与还原剂物质的量之比为___________ ,“还原2”反应的离子方程式为___________ 。
 是化学工业中广泛使用的一种高效的漂白剂和氧化剂,工业上生产它的一种流程如图所示:
是化学工业中广泛使用的一种高效的漂白剂和氧化剂,工业上生产它的一种流程如图所示:
(1)
 的名称是
的名称是(2)“还原1”中应充分搅拌,好处是
您最近一年使用:0次



