名校
1 . 工业上用 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。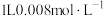 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。
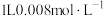 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
A.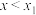 时, 时, 主要被氧化为 主要被氧化为 |
B.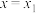 时,生成的 时,生成的 的物质的量为 的物质的量为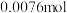 |
C.生成硝氮的离子方程式: |
D. 时,分批加入 时,分批加入 可以降低总氮残余率 可以降低总氮残余率 |
您最近一年使用:0次
名校
解题方法
2 . 处理工业废气中的氮氧化物NOx对于环境保护具有重要的意义。
(1)催化还原法。NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:_______ 。
②用Fe做催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图2所示,脱氮效果最佳的c(NO2)/c(NO)=______ 。按最佳脱氮率,每生成2molN2,转移电子数目为_______ 。
(2)可用NaClO2将氮氧化物转化成NO ,碱性条件下NaClO2去除NO反应的离子方程式为
,碱性条件下NaClO2去除NO反应的离子方程式为_______ 。
(3)对NO和NO2脱除后产生的含NO 溶液可用如图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为
溶液可用如图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为_______ 。
(1)催化还原法。NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:

②用Fe做催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图2所示,脱氮效果最佳的c(NO2)/c(NO)=
(2)可用NaClO2将氮氧化物转化成NO
 ,碱性条件下NaClO2去除NO反应的离子方程式为
,碱性条件下NaClO2去除NO反应的离子方程式为(3)对NO和NO2脱除后产生的含NO
 溶液可用如图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为
溶液可用如图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为
您最近一年使用:0次
名校
解题方法
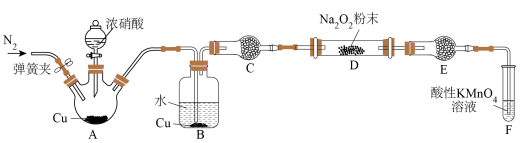
3 . 某研究性学习小组学生用图中所示装置(部分夹持装置略)探究NO与Na2O2反应的情况,提出假设并进行相关实验。 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。
(1)盛装浓硝酸的仪器名称为_______ 。
(2)反应结束后打开弹簧夹,通入过量N2的目的是_______ 。
(3)C、E中所盛装的试剂不能是_______ (填字母编号)。
a.无水硫酸铜 b.无水氯化钙 c.碱石灰
(4)F中发生反应的氧化剂与还原剂的物质的量之比为______ 。
(5)充分反应后,检验D装置中产物的方法是:取D装置中产物少许,_______ ,则产物是NaNO2。
(6)测定NaNO2的纯度:准确称取反应后的固体4.00g于烧杯中,加入煮沸并冷却的蒸馏水溶解,配成250mL的溶液;取出25.00mL的溶液于锥形瓶中,使0.1mol L-1的酸性KMnO4溶液恰好褪色,用去20.00mL的酸性KMnO4溶液。已知:滴定过程中的离子反应方程式为2MnO
L-1的酸性KMnO4溶液恰好褪色,用去20.00mL的酸性KMnO4溶液。已知:滴定过程中的离子反应方程式为2MnO +6H++5NO
+6H++5NO =2Mn2++5NO
=2Mn2++5NO +3H2O。所得固体中NaNO2的纯度(质量分数)为
+3H2O。所得固体中NaNO2的纯度(质量分数)为_______ 。(NaNO2的摩尔质量为69g mol-1)
mol-1)
 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。(1)盛装浓硝酸的仪器名称为
(2)反应结束后打开弹簧夹,通入过量N2的目的是
(3)C、E中所盛装的试剂不能是
a.无水硫酸铜 b.无水氯化钙 c.碱石灰
(4)F中发生反应的氧化剂与还原剂的物质的量之比为
(5)充分反应后,检验D装置中产物的方法是:取D装置中产物少许,
(6)测定NaNO2的纯度:准确称取反应后的固体4.00g于烧杯中,加入煮沸并冷却的蒸馏水溶解,配成250mL的溶液;取出25.00mL的溶液于锥形瓶中,使0.1mol
 L-1的酸性KMnO4溶液恰好褪色,用去20.00mL的酸性KMnO4溶液。已知:滴定过程中的离子反应方程式为2MnO
L-1的酸性KMnO4溶液恰好褪色,用去20.00mL的酸性KMnO4溶液。已知:滴定过程中的离子反应方程式为2MnO +6H++5NO
+6H++5NO =2Mn2++5NO
=2Mn2++5NO +3H2O。所得固体中NaNO2的纯度(质量分数)为
+3H2O。所得固体中NaNO2的纯度(质量分数)为 mol-1)
mol-1)
您最近一年使用:0次
名校
解题方法
4 . 将32gCu和200mL一定浓度的浓HNO3混合,随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO2和NO组成的混合气体8.96L(标准状况)。下列关于该反应的分析错误的是
| A.该反应生成的NO2与NO的体积比为1∶3 |
| B.该反应转移电子数为NA |
| C.该反应共消耗1.4molHNO3 |
D.该浓硝酸浓度一定为7mol L-1 L-1 |
您最近一年使用:0次
名校
5 . 城市污水中含有一定量的 、
、 ,向污水中加入菌体和
,向污水中加入菌体和 溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ,从而实现
溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ,从而实现 、
、 的脱除,其过程如图所示。下列说法正确的是
的脱除,其过程如图所示。下列说法正确的是
 、
、 ,向污水中加入菌体和
,向污水中加入菌体和 溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ,从而实现
溶液,在菌体的作用下依次发生过程Ⅰ、过程Ⅱ,从而实现 、
、 的脱除,其过程如图所示。下列说法正确的是
的脱除,其过程如图所示。下列说法正确的是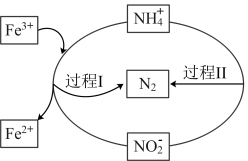
A.“过程Ⅰ”中 为催化剂 为催化剂 |
B. 的氧化性强于 的氧化性强于 |
C.“过程Ⅱ”中氧化产物和还原产物的质量之比为 |
D.“过程Ⅰ”中发生的反应,产物 、 、 的浓度之比为定值 的浓度之比为定值 |
您最近一年使用:0次
名校
6 . 对于反应 ,以下叙述正确的是
,以下叙述正确的是
 ,以下叙述正确的是
,以下叙述正确的是A. 是氧化剂, 是氧化剂, 是还原剂 是还原剂 |
B.被氧化的 原子和被还原的 原子和被还原的 原子的物质的量的比为 原子的物质的量的比为 |
C. 既做氧化剂又做还原剂 既做氧化剂又做还原剂 |
D.氧化剂得电子数与还原剂失电子数之比为 |
您最近一年使用:0次
名校
7 . 下图是以合成氨为基础的传统硝酸生产工艺流程(其中空气等基础原料已略去)。 分子的结构式为
分子的结构式为_______________ 。
(2)吸收装置中,发生的反应为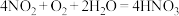 ,若用
,若用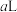
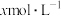 的稀硝酸作为吸收液,反应后得到
的稀硝酸作为吸收液,反应后得到
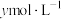 的浓硝酸,则理论上吸收装置中需消耗的
的浓硝酸,则理论上吸收装置中需消耗的 的物质的量为
的物质的量为_______  。
。
(3)实验室常用 溶液吸收
溶液吸收 (
( 和
和 的混合气体),反应的化学方程式如下:
的混合气体),反应的化学方程式如下: ;
; (已知
(已知 不能与
不能与 溶液反应,不考虑
溶液反应,不考虑 与
与 的转化)。
的转化)。
①若 能被
能被 溶液完全吸收,则
溶液完全吸收,则 的取值范围为
的取值范围为_______________ 。
②若
 恰好完全反应,则被吸收的
恰好完全反应,则被吸收的 的体积为
的体积为_________  (标准状况下)。
(标准状况下)。
(4) 催化还原氯氧化物技术(
催化还原氯氧化物技术( )是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示。若催化剂表面参与反应的
)是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示。若催化剂表面参与反应的 和
和 物质的量之比为
物质的量之比为 ,则总反应的化学方程式为
,则总反应的化学方程式为_______________ 。
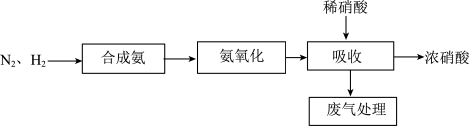
 分子的结构式为
分子的结构式为(2)吸收装置中,发生的反应为
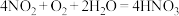 ,若用
,若用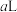
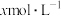 的稀硝酸作为吸收液,反应后得到
的稀硝酸作为吸收液,反应后得到
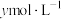 的浓硝酸,则理论上吸收装置中需消耗的
的浓硝酸,则理论上吸收装置中需消耗的 的物质的量为
的物质的量为 。
。(3)实验室常用
 溶液吸收
溶液吸收 (
( 和
和 的混合气体),反应的化学方程式如下:
的混合气体),反应的化学方程式如下: ;
; (已知
(已知 不能与
不能与 溶液反应,不考虑
溶液反应,不考虑 与
与 的转化)。
的转化)。①若
 能被
能被 溶液完全吸收,则
溶液完全吸收,则 的取值范围为
的取值范围为②若

 恰好完全反应,则被吸收的
恰好完全反应,则被吸收的 的体积为
的体积为 (标准状况下)。
(标准状况下)。(4)
 催化还原氯氧化物技术(
催化还原氯氧化物技术( )是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示。若催化剂表面参与反应的
)是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如图所示。若催化剂表面参与反应的 和
和 物质的量之比为
物质的量之比为 ,则总反应的化学方程式为
,则总反应的化学方程式为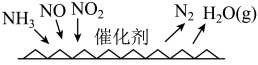
您最近一年使用:0次
名校
解题方法
8 . 已知:含 的酸性溶液
的酸性溶液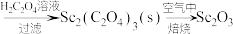 。下列说法正确的是
。下列说法正确的是
 的酸性溶液
的酸性溶液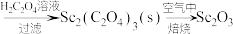 。下列说法正确的是
。下列说法正确的是A.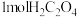 (乙二酸)含有 (乙二酸)含有 键 键 |
B.沸点: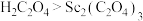 |
C.生成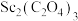 的离子方程式为 的离子方程式为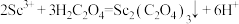 |
D.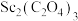 在足量空气中焙烧,消耗 在足量空气中焙烧,消耗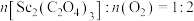 |
您最近一年使用:0次
9 . 某V2O5失活催化剂是重要的含钒二次资源。从酸浸处理之后的浸出液中提取钒的一种工艺流程如图。下列说法错误的是
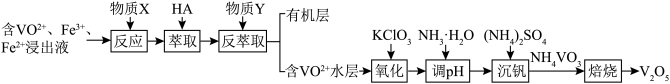
| A.物质X为高锰酸钾溶液 |
| B.反萃取时,物质Y可以选用硫酸 |
| C.氧化过程中,氧化产物与还原产物的物质的量之比为6:1 |
D.调pH时,发生反应:VO +2NH3•H2O +2NH3•H2O VO VO +2NH +2NH +H2O +H2O |
您最近一年使用:0次
10 . 我国长征系列运载火箭的第一、第二级发动机,使用的燃料是偏二甲肼( )和四氧化二氮(
)和四氧化二氮( ),燃烧产物绿色无污染。燃烧的化学反应方程式:
),燃烧产物绿色无污染。燃烧的化学反应方程式: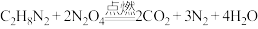 。
。
(1)上述反应中,氧化剂是___________ ;若有30g的 参加反应,需要
参加反应,需要 的物质的量为
的物质的量为___________ mol。
(2) 为
为___________ 色气体。若用 代替
代替 也能与
也能与 发生类似的反应,写出该反应的化学方程式:
发生类似的反应,写出该反应的化学方程式:___________ 。
 )和四氧化二氮(
)和四氧化二氮( ),燃烧产物绿色无污染。燃烧的化学反应方程式:
),燃烧产物绿色无污染。燃烧的化学反应方程式: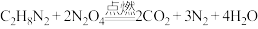 。
。(1)上述反应中,氧化剂是
 参加反应,需要
参加反应,需要 的物质的量为
的物质的量为(2)
 为
为 代替
代替 也能与
也能与 发生类似的反应,写出该反应的化学方程式:
发生类似的反应,写出该反应的化学方程式:
您最近一年使用:0次



