1 . 液氨具有微弱的导电性,钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,如图为钠投入液氨中的溶剂化图。钠沉入液氨中,快速得到深蓝色溶液,并慢慢产生气泡。下列说法错误的是
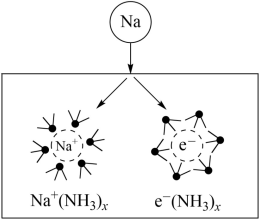

A.液氨能够发生电离,有 和 和 生成 生成 |
| B.溶液的导电性增强 |
C.钠和液氨可发生以下反应: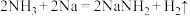 |
D.0.1mol钠投入液氨生成0.01mol 时, 时, 共失去0.02mol电子 共失去0.02mol电子 |
您最近一年使用:0次
2 . 回答下列问题
(1)氨分解反应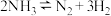 在容积为
在容积为 的密闭容器内进行。已知起始时氨气的物质的量为
的密闭容器内进行。已知起始时氨气的物质的量为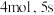 末为
末为 ,则用氨气表示该反应的速率为
,则用氨气表示该反应的速率为______ 氨分解反应的逆反应为合成氨,当消耗 时,放出
时,放出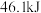 的热量,写出该反应的热化学方程式
的热量,写出该反应的热化学方程式______ 。
(2)如图所示,将锌、铜通过导线连接,置于稀硫酸中。
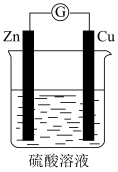
①负极电极反应式为______ 。
②正极电极反应式为______ 。
③溶液中 由
由______ (填“锌”或者“铜”下同)向_______ 移动。
④若反应过程中有 电子发生转移,则生成的氢气在标准状况下的体积为
电子发生转移,则生成的氢气在标准状况下的体积为______ 。
(1)氨分解反应
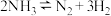 在容积为
在容积为 的密闭容器内进行。已知起始时氨气的物质的量为
的密闭容器内进行。已知起始时氨气的物质的量为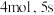 末为
末为 ,则用氨气表示该反应的速率为
,则用氨气表示该反应的速率为 时,放出
时,放出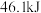 的热量,写出该反应的热化学方程式
的热量,写出该反应的热化学方程式(2)如图所示,将锌、铜通过导线连接,置于稀硫酸中。

①负极电极反应式为
②正极电极反应式为
③溶液中
 由
由④若反应过程中有
 电子发生转移,则生成的氢气在标准状况下的体积为
电子发生转移,则生成的氢气在标准状况下的体积为
您最近一年使用:0次
名校
3 . 已知 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是
 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是A.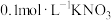 溶液中离子总数大于 溶液中离子总数大于 |
B.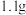 的 的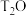 ,含有的质子数为 ,含有的质子数为 |
C. 与足量的 与足量的 反应转移的电子数为 反应转移的电子数为 |
D. 和 和 充分反应,转移电子数为 充分反应,转移电子数为 |
您最近一年使用:0次
2024-03-10更新
|
111次组卷
|
2卷引用:福建省莆田第一中学2023-2024学年高一上学期期末考试化学试题
名校
4 .  和
和 可用于烟气中的大量氮氧化物
可用于烟气中的大量氮氧化物 转化为无害物质.将NO与
转化为无害物质.将NO与 的混合气体通入
的混合气体通入 和
和 的混合溶液中,发生以下转化过程.下列说法
的混合溶液中,发生以下转化过程.下列说法错误 的是
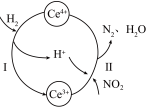
 和
和 可用于烟气中的大量氮氧化物
可用于烟气中的大量氮氧化物 转化为无害物质.将NO与
转化为无害物质.将NO与 的混合气体通入
的混合气体通入 和
和 的混合溶液中,发生以下转化过程.下列说法
的混合溶液中,发生以下转化过程.下列说法
A.反应前后溶液中 和 和 的总物质的量不变 的总物质的量不变 |
| B.参加反应Ⅰ的氧化剂与还原剂的个数之比为2∶1 |
C.反应Ⅱ的离子方程式为 |
D.反应过程中消耗 与生成 与生成 的体积(标况下)相等 的体积(标况下)相等 |
您最近一年使用:0次
5 . 完成下列问题。
(1)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: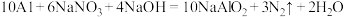 。
。
①上述反应中,被还原的元素是_______ (填写元素符号);氧化产物是_______ (写化学式);若反应生成 (标况下)的
(标况下)的 ,该反应转移电子的数目为
,该反应转移电子的数目为___  。
。
②用双线桥法表示反应中电子转移的方向和数目:________  。
。
③请配平下列离子方程式:____ 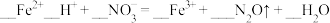 。
。
(2)食品工业经常使用 和
和 作膨松剂。室温下,向含
作膨松剂。室温下,向含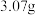 某膨松剂试样(
某膨松剂试样(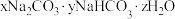 )溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随
)溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随 变化的图象如图所示。
变化的图象如图所示。
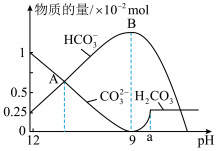
①图中B点溶液溶质的主要成分为________ (填化学式)。
②图中A点所含 的物质的量为
的物质的量为_____ mol。(提醒:注意纵坐标的数量级)
③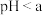 时发生反应的离子反应方程式为
时发生反应的离子反应方程式为_________ 。
④某同学用酒精灯对该试样固体充分加热至恒重,从开始至恒重固体失重______ g。
(1)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: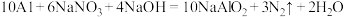 。
。①上述反应中,被还原的元素是
 (标况下)的
(标况下)的 ,该反应转移电子的数目为
,该反应转移电子的数目为 。
。②用双线桥法表示反应中电子转移的方向和数目:
 。
。③请配平下列离子方程式:
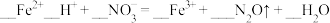 。
。(2)食品工业经常使用
 和
和 作膨松剂。室温下,向含
作膨松剂。室温下,向含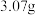 某膨松剂试样(
某膨松剂试样(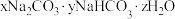 )溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随
)溶液中逐滴加入稀盐酸,反应过程中含碳元素微粒的物质的量随 变化的图象如图所示。
变化的图象如图所示。
①图中B点溶液溶质的主要成分为
②图中A点所含
 的物质的量为
的物质的量为③
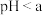 时发生反应的离子反应方程式为
时发生反应的离子反应方程式为④某同学用酒精灯对该试样固体充分加热至恒重,从开始至恒重固体失重
您最近一年使用:0次
2024-03-04更新
|
70次组卷
|
2卷引用:福建省莆田第一中学2023-2024学年高一上学期期末考试化学试题
6 . 实验室中利用固体KMnO4进行如图实验,下列说法错误的是
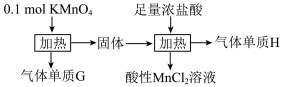

| A.G与H均为氧化产物 | B.Mn元素至少参与了3个氧化还原反应 |
| C.氧化性MnO2>Cl2 | D.G与H的物质的量之和为0.25mol |
您最近一年使用:0次
7 . 油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄( )褪色的主要原因是发生了以下两种化学反应:
)褪色的主要原因是发生了以下两种化学反应:
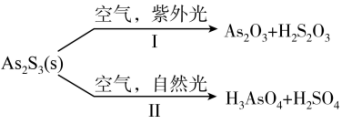
下列说法正确的是
 )褪色的主要原因是发生了以下两种化学反应:
)褪色的主要原因是发生了以下两种化学反应:
下列说法正确的是
A.反应Ⅰ和Ⅱ中,氧化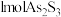 转移的电子数之比为 转移的电子数之比为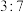 |
B. 和 和 的空间结构都是正四面体形 的空间结构都是正四面体形 |
C.元素 和 和 形成的气态氢化物,键角 形成的气态氢化物,键角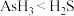 |
D.酸性: |
您最近一年使用:0次
名校
8 . 建筑工地常用的 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O
能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O
(1)配平上述化学方程式,并用双线桥表示电子转移情况____ 。
(2)上述反应的氧化剂是____ ;若有1mol的还原剂被氧化,则反应中转移电子的数目是_______ 。
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别 和
和 ,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。
,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。
(4)某厂废液中,含有2%~5%的 ,直接排放会造成污染,使用
,直接排放会造成污染,使用 处理,能使
处理,能使 转化为不引起二次污染的
转化为不引起二次污染的 ,反应的化学方程式为
,反应的化学方程式为______ 。
(5)以过氧化氢作还原剂,在硫酸介质中还原NaClO3制备ClO2,并将制得的ClO2处理含CN-废水。ClO2处理含CN-废水的离子方程式为______ 。
 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O
能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O(1)配平上述化学方程式,并用双线桥表示电子转移情况
(2)上述反应的氧化剂是
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别
 和
和 ,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。
,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。| A.③⑤ | B.②④ | C.②⑤ | D.①②③⑤ |
 ,直接排放会造成污染,使用
,直接排放会造成污染,使用 处理,能使
处理,能使 转化为不引起二次污染的
转化为不引起二次污染的 ,反应的化学方程式为
,反应的化学方程式为(5)以过氧化氢作还原剂,在硫酸介质中还原NaClO3制备ClO2,并将制得的ClO2处理含CN-废水。ClO2处理含CN-废水的离子方程式为
您最近一年使用:0次
9 . 过二硫酸钾( )是工业上一种重要的消毒剂和织物漂白剂,可通过电解
)是工业上一种重要的消毒剂和织物漂白剂,可通过电解 溶液制备。它在
溶液制备。它在 下能发生分解反应:
下能发生分解反应: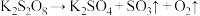 (未配平),设
(未配平),设 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是
 )是工业上一种重要的消毒剂和织物漂白剂,可通过电解
)是工业上一种重要的消毒剂和织物漂白剂,可通过电解 溶液制备。它在
溶液制备。它在 下能发生分解反应:
下能发生分解反应: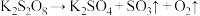 (未配平),设
(未配平),设 是阿伏加德罗常数的值。下列说法错误的是
是阿伏加德罗常数的值。下列说法错误的是A.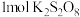 中存在 中存在 个非极性共价键 个非极性共价键 |
B.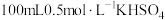 溶液的离子总数为 溶液的离子总数为 |
C.标准状况下,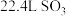 含有的原子数大于 含有的原子数大于 |
D.上述反应,每生成 ,转移 ,转移 个电子 个电子 |
您最近一年使用:0次
2024-02-27更新
|
540次组卷
|
3卷引用:福建省福州市福建师范大学附属中学2024届高三一模化学试题
10 . 从废旧CPU中回收Au(金)、Ag、Cu的部分流程如下: 。下列说法正确的是
。下列说法正确的是
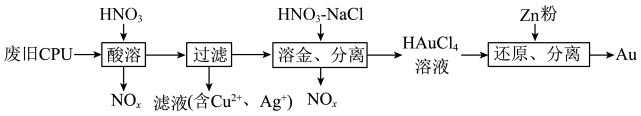
 。下列说法正确的是
。下列说法正确的是| A.酸溶时,溶解相同的原料,使用浓硝酸产生的氮氧化物比使用稀硝酸的少 |
| B.向过滤所得滤液中加入过量浓氨水,可以分离Cu2+、Ag+ |
| C.用浓盐酸和浓NaNO3溶液的混合液也可以溶解金 |
| D.向1 mol HAuCl4中加入过量Zn使其完全还原为Au,只需消耗1.5 mol Zn |
您最近一年使用:0次
2024-02-24更新
|
488次组卷
|
4卷引用:福建省泉州市泉港区第二中学2024届高三下学期第一次模拟预测化学试题



