1 . 我国长征系列运载火箭的第一、第二级发动机,使用的燃料是偏二甲肼( )和四氧化二氮(
)和四氧化二氮( ),燃烧产物绿色无污染。燃烧的化学反应方程式:
),燃烧产物绿色无污染。燃烧的化学反应方程式: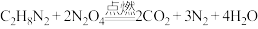 。
。
(1)上述反应中,氧化剂是___________ ;若有30g的 参加反应,需要
参加反应,需要 的物质的量为
的物质的量为___________ mol。
(2) 为
为___________ 色气体。若用 代替
代替 也能与
也能与 发生类似的反应,写出该反应的化学方程式:
发生类似的反应,写出该反应的化学方程式:___________ 。
 )和四氧化二氮(
)和四氧化二氮( ),燃烧产物绿色无污染。燃烧的化学反应方程式:
),燃烧产物绿色无污染。燃烧的化学反应方程式: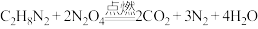 。
。(1)上述反应中,氧化剂是
 参加反应,需要
参加反应,需要 的物质的量为
的物质的量为(2)
 为
为 代替
代替 也能与
也能与 发生类似的反应,写出该反应的化学方程式:
发生类似的反应,写出该反应的化学方程式:
您最近一年使用:0次
名校
解题方法
2 . N2O5中N元素的化合价为
| A.0 | B.+1 | C.+3 | D.+5 |
您最近一年使用:0次
2020-07-17更新
|
368次组卷
|
6卷引用:2020年6月福建省普通高中学业水平合格性考试化学试题
名校
解题方法
3 . 实验室制备并收集干燥、纯净氯气的装置如图所示:
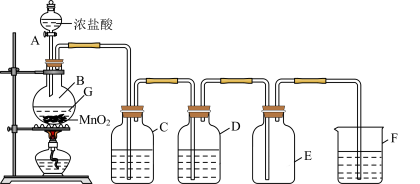
(1)写出实验室制备Cl2的化学方程式:___ 。
(2)写出指定试剂的名称,C__ ,D__ 。
(3)C的作用是__ ,D的作用是__ ,F的作用是___ 。
(4)检验氯气是否收集满的操作:___ 。
(5)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,其中该反应中HCl的作用是___ ,若反应产生0.5mol Cl2,则消耗的氧化剂的物质的量为___ mol,反应转移的电子数是___ 。

(1)写出实验室制备Cl2的化学方程式:
(2)写出指定试剂的名称,C
(3)C的作用是
(4)检验氯气是否收集满的操作:
(5)实验室除了可用二氧化锰和浓盐酸反应制取氯气外,还可以用其他很多方法制取氯气,其中用高锰酸钾和浓盐酸反应制备氯气的化学方程式可表示为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,其中该反应中HCl的作用是
您最近一年使用:0次
2020-01-02更新
|
396次组卷
|
5卷引用:福建省三明市第二中学2021-2022学年高一下学期会考模拟卷(一)化学试题
4 . 银是一种在工业、生活上有广泛用途的金属。
已知:①金属在水中存在如下溶解平衡过程:M Mx+ + xe-,
Mx+ + xe-,
氢气在水溶液中也存在如下平衡过程:H2 2H++ 2e-
2H++ 2e-
②Ag2S 的Ksp=6.7×10-50; AgCl的Ksp=1.6×10-10
据此回答下列有关问题:
(1)银质餐具可杀菌消毒,原因是_________________ (用适当的方程式和文字表述说明);金属银与氢硫酸可反应生成黑色固体和无色气体,写出该反应的化学方程式_______________
(2)金属银与硝酸银溶液组成电池示意图如右,a电极的反应为________________ ,NO3-从电池________ 侧溶液向电池_______ 侧溶液移动 (填“左”或“右”)。

(3)硝酸银见光或受热易分解为Ag、NO2、O2,反应中生成NO2、O2的 物质的量之比为___________ ,将混合气体通过水吸收后,剩余气体为________________
(4)已知:Ag+(aq) + 2NH3•H2O(aq) [Ag(NH3)2]+(aq) + 2H2O K=1.6×107,写出AgCl溶于氨水的离子方程式
[Ag(NH3)2]+(aq) + 2H2O K=1.6×107,写出AgCl溶于氨水的离子方程式________________________ ;计算该反应的平衡常数K=___________ 。在氯化银溶于氨水后的溶液中滴加稀硝酸,会再产生白色氯化银沉淀,滴加硝酸至刚好沉淀完全,取上层清液测其pH,发现呈酸性,主要原因是_______________ (用离子方程式表示)。
已知:①金属在水中存在如下溶解平衡过程:M
 Mx+ + xe-,
Mx+ + xe-,氢气在水溶液中也存在如下平衡过程:H2
 2H++ 2e-
2H++ 2e-②Ag2S 的Ksp=6.7×10-50; AgCl的Ksp=1.6×10-10
据此回答下列有关问题:
(1)银质餐具可杀菌消毒,原因是
(2)金属银与硝酸银溶液组成电池示意图如右,a电极的反应为

(3)硝酸银见光或受热易分解为Ag、NO2、O2,反应中生成NO2、O2的 物质的量之比为
(4)已知:Ag+(aq) + 2NH3•H2O(aq)
 [Ag(NH3)2]+(aq) + 2H2O K=1.6×107,写出AgCl溶于氨水的离子方程式
[Ag(NH3)2]+(aq) + 2H2O K=1.6×107,写出AgCl溶于氨水的离子方程式
您最近一年使用:0次
2016-12-09更新
|
541次组卷
|
2卷引用:2016届福建省晨曦、冷曦、正曦、岐滨四校高三第二次联考理综化学试卷



