1 . 已知反应 ,
, 为阿伏加德罗常数的值,若生成22.4L
为阿伏加德罗常数的值,若生成22.4L (标况),下列说法错误的是
(标况),下列说法错误的是
 ,
, 为阿伏加德罗常数的值,若生成22.4L
为阿伏加德罗常数的值,若生成22.4L (标况),下列说法错误的是
(标况),下列说法错误的是A.转移的电子数目为 |
B. 是由非极性共价键形成的非极性分子 是由非极性共价键形成的非极性分子 |
C.参与反应的 含有孤电子对数为 含有孤电子对数为 |
| D.生成的还原产物质量为56g |
您最近半年使用:0次
2 . 工业上常用纯碱溶液吸收尾气中的NO、NO2,反应如下:
反应1:NO+NO2+Na2CO3=2NaNO2+CO2
反应2:2NO2+Na2CO3=NaNO2+NaNO3+CO2
已知:CO2与水的反应类似SO2和H2O的反应。若NA代表阿伏加德罗常数的值。下列叙述正确的是
反应1:NO+NO2+Na2CO3=2NaNO2+CO2
反应2:2NO2+Na2CO3=NaNO2+NaNO3+CO2
已知:CO2与水的反应类似SO2和H2O的反应。若NA代表阿伏加德罗常数的值。下列叙述正确的是
| A.反应1中放出2.24LCO2时,NO、NO2参与反应的总分子数为0.2NA |
| B.1L0.5mol·L-1Na2CO3溶液恰好完全反应时,作氧化剂的分子数为0.5NA |
| C.将反应2中9.2gNO2完全反应产生的CO2通入足量水中生成的H2CO3分子数为0.1NA |
| D.上述制备的化工品(NaNO2、NaNO3)中含N元素的质量为28g,则所含的Na+数一定为NA |
您最近半年使用:0次
3 . CuCl在有机合成中常用作催化剂或还原剂,其一种制备方法为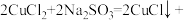
 ,下列说法错误的是
,下列说法错误的是
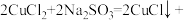
 ,下列说法错误的是
,下列说法错误的是| A.氧化剂和还原剂的物质的量之比为2∶1 |
| B.还原产物为CuCl |
C.电子转移的方向和数目可表示为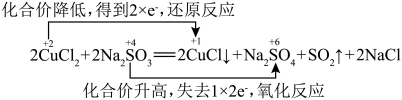 |
D.每转移1 mol ,生成 ,生成 的质量为142 g 的质量为142 g |
您最近半年使用:0次
名校
解题方法
4 . 向含有 的混合物中滴加
的混合物中滴加 的稀硝酸溶液至
的稀硝酸溶液至 时,固体恰好完全溶解,得到标准状况下
时,固体恰好完全溶解,得到标准状况下 NO。下列说法正确的是
NO。下列说法正确的是
 的混合物中滴加
的混合物中滴加 的稀硝酸溶液至
的稀硝酸溶液至 时,固体恰好完全溶解,得到标准状况下
时,固体恰好完全溶解,得到标准状况下 NO。下列说法正确的是
NO。下列说法正确的是A.反应过程中转移 电子 电子 |
B.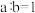 :1 :1 |
C.被还原的硝酸为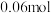 |
D.等量上述稀硝酸中最多能溶解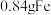 |
您最近半年使用:0次
名校
解题方法
5 . 某处工厂排出的烟道气中含氮氧化物(主要为NO、 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式______________ ;若反应后尾气无残留,则参加反应的 、NO物质的量比值为
、NO物质的量比值为_____ (填字母)。
a.≥1 b.≤1 c.任意值
(2)可使用适量酸性 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(4)有氧条件下,NO在催化剂作用下可被 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是___________ 。
(5)羟基自由基( )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程:______________ 。 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加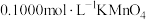 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗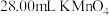 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数__________ 。(写出计算过程)
 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: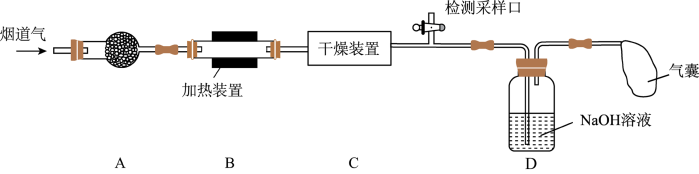
 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式 、NO物质的量比值为
、NO物质的量比值为a.≥1 b.≤1 c.任意值
(2)可使用适量酸性
 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性
 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是(4)有氧条件下,NO在催化剂作用下可被
 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: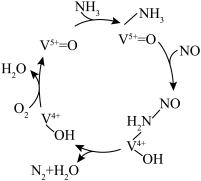
 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是(5)羟基自由基(
 )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程: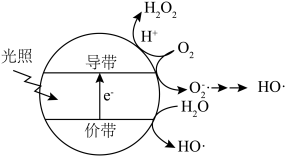
 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加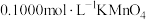 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗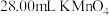 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数
您最近半年使用:0次
2024-05-03更新
|
186次组卷
|
3卷引用:河南省焦作市博爱县第一中学2023-2024学年高一下学期4月期中考试化学试题
解题方法
6 . 如图是乙烯催化氧化的过程(部分配平相关离子未画出),下列描述错误的是
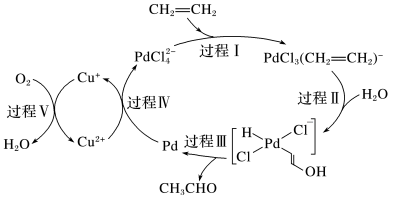
| A.“过程Ⅰ”中涉及到非极性键的断裂 |
B.反应过程中部分碳原子杂化类型由 |
C. 分子中 分子中 键与 键与 键数目之比为6:1 键数目之比为6:1 |
| D.“过程V”中消耗的氧化剂与还原剂物质的量之比为1:4 |
您最近半年使用:0次
解题方法
7 . 高铁酸钠(Na2FeO4)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。工业上制备高铁酸钠有多种方法。
(1)电解法。以铁为阳极,石墨为阴极,在通电条件下,发生反应: ,物质X的化学式为
,物质X的化学式为___________ 。
(2)高温熔融氧化法。将过氧化钠与硫酸亚铁加热至700℃,发生反应: ,其中,氧化产物是
,其中,氧化产物是___________ ,用生成1mol氧气所转移的电子数为___________ 。
(3)次氯酸钠氧化法___________ 。
②副产品的成分为___________ 。
(1)电解法。以铁为阳极,石墨为阴极,在通电条件下,发生反应:
 ,物质X的化学式为
,物质X的化学式为(2)高温熔融氧化法。将过氧化钠与硫酸亚铁加热至700℃,发生反应:
 ,其中,氧化产物是
,其中,氧化产物是(3)次氯酸钠氧化法
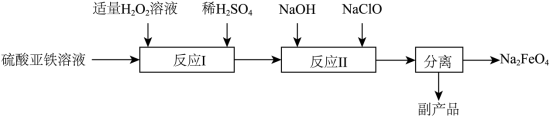
②副产品的成分为
您最近半年使用:0次
解题方法
8 . 已知某物质的XO(OH) 与Na2SO3反应时, XO(OH)
与Na2SO3反应时, XO(OH) 作氧化剂,Na2SO3被氧化为Na2SO4。经测得4分子XO(OH)
作氧化剂,Na2SO3被氧化为Na2SO4。经测得4分子XO(OH) 与2分子的Na2SO3恰好完全作用。试问XO(OH)
与2分子的Na2SO3恰好完全作用。试问XO(OH) 还原后X的最终价态是
还原后X的最终价态是
 与Na2SO3反应时, XO(OH)
与Na2SO3反应时, XO(OH) 作氧化剂,Na2SO3被氧化为Na2SO4。经测得4分子XO(OH)
作氧化剂,Na2SO3被氧化为Na2SO4。经测得4分子XO(OH) 与2分子的Na2SO3恰好完全作用。试问XO(OH)
与2分子的Na2SO3恰好完全作用。试问XO(OH) 还原后X的最终价态是
还原后X的最终价态是| A.+3 | B.+4 | C.+5 | D.0 |
您最近半年使用:0次
9 . 氯化亚铜(CuCl)微溶于水,难溶于乙醇,易被氧化,广泛应用于医药、有机合成催化剂等工业。以废铜渣(主要含Cu、CuO,还有少量其他难溶物)为原料制备CuCl的工艺流程如图所示。 被还原为
被还原为 ,该过程中发生氧化还原反应的离子方程式为
,该过程中发生氧化还原反应的离子方程式为____________ 。
(2)若“浸出”过程中0.2 mol 参加反应时,转移1 mol电子,则还原产物为
参加反应时,转移1 mol电子,则还原产物为______ (填化学式)。
(3)“还原”过程中逐滴加入 、
、 溶液,初始时生成沉淀反应的离子方程式是
溶液,初始时生成沉淀反应的离子方程式是____________ 。“还原”过程中 溶液加入至过量的原因:一是让
溶液加入至过量的原因:一是让 全部被还原,二是
全部被还原,二是____________ 。
(4)“还原”过程中加入 溶液的体积(V)与溶液pH的关系如图所示。
溶液的体积(V)与溶液pH的关系如图所示。 溶液体积大于一定量时,溶液pH增大的原因是
溶液体积大于一定量时,溶液pH增大的原因是____________ 。
(5)用无水乙醇洗涤CuCl的优点是____________ (填一条)。
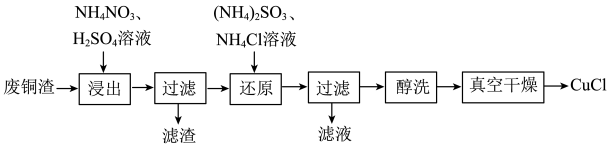
 被还原为
被还原为 ,该过程中发生氧化还原反应的离子方程式为
,该过程中发生氧化还原反应的离子方程式为(2)若“浸出”过程中0.2 mol
 参加反应时,转移1 mol电子,则还原产物为
参加反应时,转移1 mol电子,则还原产物为(3)“还原”过程中逐滴加入
 、
、 溶液,初始时生成沉淀反应的离子方程式是
溶液,初始时生成沉淀反应的离子方程式是 溶液加入至过量的原因:一是让
溶液加入至过量的原因:一是让 全部被还原,二是
全部被还原,二是(4)“还原”过程中加入
 溶液的体积(V)与溶液pH的关系如图所示。
溶液的体积(V)与溶液pH的关系如图所示。
 溶液体积大于一定量时,溶液pH增大的原因是
溶液体积大于一定量时,溶液pH增大的原因是(5)用无水乙醇洗涤CuCl的优点是
您最近半年使用:0次
名校
10 . 二氧化碳、甲烷的捕集、转化与利用对环境和能源具有重要意义。
Ⅰ. 的捕集
的捕集
(1)地球上最高效的碳捕捉过程是绿色植物的______ ,该过程中能量的转化形式为______ 。
(2)用碱液吸收 。
。
①用足量NaOH溶液吸收 ,该过程中溶液的温度
,该过程中溶液的温度______ (填“上升”或“下降”)。
②若用100 mL 5 mol⋅L 的NaOH溶液吸收
的NaOH溶液吸收 后,测得吸收液中的
后,测得吸收液中的 ,则吸收的
,则吸收的 在标准状况下的体积为
在标准状况下的体积为______ L。
Ⅱ. 、
、 的转化
的转化
(3)在一定条件下,在催化剂表面将 转化为
转化为 ,其原理如图所示:
,其原理如图所示: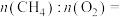
______ 。
Ⅲ. 、
、 的利用
的利用
(4)一种将 转化为合成气(
转化为合成气( 和CO)的原理如图所示:
和CO)的原理如图所示:____________ 。
②理论上,2.24 L (标准状况)通过以上两步反应最多可制得
(标准状况)通过以上两步反应最多可制得 的物质的量为
的物质的量为______ 。
(5)通过人工光合作用可实现对 的再利用,以
的再利用,以 和
和 为原料制备甲酸(HCOOH),工作原理如图所示:
为原料制备甲酸(HCOOH),工作原理如图所示: 的移动方向是左
的移动方向是左______ 右(填“→”或“←”)。
②电极b上的电极反应式为____________ 。
Ⅰ.
 的捕集
的捕集(1)地球上最高效的碳捕捉过程是绿色植物的
(2)用碱液吸收
 。
。①用足量NaOH溶液吸收
 ,该过程中溶液的温度
,该过程中溶液的温度②若用100 mL 5 mol⋅L
 的NaOH溶液吸收
的NaOH溶液吸收 后,测得吸收液中的
后,测得吸收液中的 ,则吸收的
,则吸收的 在标准状况下的体积为
在标准状况下的体积为Ⅱ.
 、
、 的转化
的转化(3)在一定条件下,在催化剂表面将
 转化为
转化为 ,其原理如图所示:
,其原理如图所示: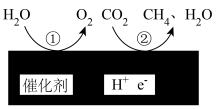
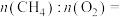
Ⅲ.
 、
、 的利用
的利用(4)一种将
 转化为合成气(
转化为合成气( 和CO)的原理如图所示:
和CO)的原理如图所示: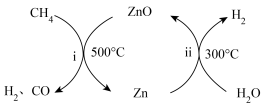
②理论上,2.24 L
 (标准状况)通过以上两步反应最多可制得
(标准状况)通过以上两步反应最多可制得 的物质的量为
的物质的量为(5)通过人工光合作用可实现对
 的再利用,以
的再利用,以 和
和 为原料制备甲酸(HCOOH),工作原理如图所示:
为原料制备甲酸(HCOOH),工作原理如图所示: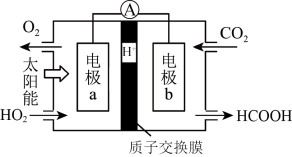
 的移动方向是左
的移动方向是左②电极b上的电极反应式为
您最近半年使用:0次



