1 . 化学与生产、生活息息相关。回答下列问题:
(1)小苏打在面包行业,不仅可以做膨松剂,还可以调节酸度。写出用小苏打调节酸度时发生反应的离子方程式:___________ 。
(2)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为___________ 。
(3)补铁剂中的铁元素化合价为___________ ,常和维生素 C 一起服用,说明维 C 具有 ___________ 性。
(4)我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为 。该反应中被还原的元素是
。该反应中被还原的元素是___________ (填元素符号)。
(5)安全气囊弹出时发生反应: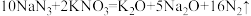 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为___________ 。标准状况下生成 44.8LN2时转移电子个数为 ___________ NA ( NA为阿伏加德罗常数的值)。
(1)小苏打在面包行业,不仅可以做膨松剂,还可以调节酸度。写出用小苏打调节酸度时发生反应的离子方程式:
(2)沾有水的铁锅在高温火焰上灼烧会发黑,该反应的化学方程式为
(3)补铁剂中的铁元素化合价为
(4)我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为
 。该反应中被还原的元素是
。该反应中被还原的元素是(5)安全气囊弹出时发生反应:
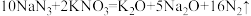 ,该反应中氧化产物与还原产物的物质的量之比为
,该反应中氧化产物与还原产物的物质的量之比为
您最近一年使用:0次
名校
解题方法
2 . 下列计算结果正确且合理的是
| A.0.5 L、8 mol/L浓盐酸与足量MnO2完全反应产生22.4 L(标准状况下)Cl2 |
B. 反应中氧化产物与还原产物的物质的量之比为1∶2 反应中氧化产物与还原产物的物质的量之比为1∶2 |
C.将NO2和O2等体积混合充满一试管,倒置于水槽中,充分反应后,试管中剩余气体占试管容积的 |
D.标准状况下,用一充满NH3气体的干燥烧瓶做喷泉实验,当水充满整个烧瓶后(假设溶液不外溢),烧瓶内溶液的物质的量的浓度为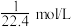 |
您最近一年使用:0次
2024-03-28更新
|
147次组卷
|
3卷引用:河南省郑州市宇华实验学校2023-2024学年高一下学期4月期中考试化学试题
名校
3 . 硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。___________ 、___________ 。
(2) 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是___________ 。
(3)已知 能被酸性
能被酸性 氧化为
氧化为 ,则
,则 的
的 溶液与
溶液与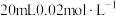 的
的 溶液恰好反应时,发生的离子方程式为:
溶液恰好反应时,发生的离子方程式为:___________ 。
(4)过二硫酸钠( )有强氧化性,在碱性条件下
)有强氧化性,在碱性条件下 溶液能将
溶液能将 氧化成
氧化成 ,且反应后的溶液滴入
,且反应后的溶液滴入 溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为
溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为___________ 。
(5)雌黄( )和雄黄(
)和雄黄( )在自然界中共生且可以相互转化(两者的硫元素价态均为
)在自然界中共生且可以相互转化(两者的硫元素价态均为 价)。
价)。
① 和
和 在盐酸中恰好完全反应转化为
在盐酸中恰好完全反应转化为 和
和 并放出
并放出 气体。则参加反应的
气体。则参加反应的 和
和 的物质的量之比为
的物质的量之比为___________ 。
② 和
和 可以相互转化,转化过程中存在如图所示的步骤。若
可以相互转化,转化过程中存在如图所示的步骤。若 参加反应时,转移
参加反应时,转移 电子,则物质a为
电子,则物质a为___________ 。

(2)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是(3)已知
 能被酸性
能被酸性 氧化为
氧化为 ,则
,则 的
的 溶液与
溶液与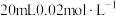 的
的 溶液恰好反应时,发生的离子方程式为:
溶液恰好反应时,发生的离子方程式为:(4)过二硫酸钠(
 )有强氧化性,在碱性条件下
)有强氧化性,在碱性条件下 溶液能将
溶液能将 氧化成
氧化成 ,且反应后的溶液滴入
,且反应后的溶液滴入 溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为
溶液生成不溶于稀盐酸的白色沉淀,该反应的离子方程式为(5)雌黄(
 )和雄黄(
)和雄黄( )在自然界中共生且可以相互转化(两者的硫元素价态均为
)在自然界中共生且可以相互转化(两者的硫元素价态均为 价)。
价)。①
 和
和 在盐酸中恰好完全反应转化为
在盐酸中恰好完全反应转化为 和
和 并放出
并放出 气体。则参加反应的
气体。则参加反应的 和
和 的物质的量之比为
的物质的量之比为②
 和
和 可以相互转化,转化过程中存在如图所示的步骤。若
可以相互转化,转化过程中存在如图所示的步骤。若 参加反应时,转移
参加反应时,转移 电子,则物质a为
电子,则物质a为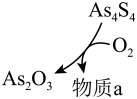
您最近一年使用:0次
2024-03-11更新
|
308次组卷
|
2卷引用:河南省新乡市原阳县实验高级中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
4 . 一定条件下,当溶液中XO 与H2O2分子个数比恰好为2:5时,溶液中XO
与H2O2分子个数比恰好为2:5时,溶液中XO 离子被还原为较低价态,则X元素的化合价为
离子被还原为较低价态,则X元素的化合价为
 与H2O2分子个数比恰好为2:5时,溶液中XO
与H2O2分子个数比恰好为2:5时,溶液中XO 离子被还原为较低价态,则X元素的化合价为
离子被还原为较低价态,则X元素的化合价为| A.+2 | B.+3 | C.+4 | D.+5 |
您最近一年使用:0次
2024-02-26更新
|
80次组卷
|
11卷引用:河南省濮阳市油田一中2022-2023学年高一上学期月考化学试题
河南省濮阳市油田一中2022-2023学年高一上学期月考化学试题(已下线)第11讲 氧化还原反应的应用和配平-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)第一章《物质及其变化》基础过关单元检测-【帮课堂】2022-2023学年高一化学必修第一册精品讲义(人教版2019)天津市耀华中学2022-2023学年高一上学期期末考试化学试题天津市耀华中学2022-2023学年高一上学期期末考试化学试题(已下线)专题08 氧化还原反应方程式的书写及计算-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考通用)(已下线)专题03 物质的量在化学方程式计算中的应用(一题多问)甘肃省天水市第一中学2023-2024学年高一上学期10月月考化学试题河北省石家庄市第十五中学2023-2024学年高一上学期第一次月考化学试题河北省石家庄市第一中学西校区2023-2024高一上学期期末考试化学试题河北省石家庄市西山学校2023-2024学年高一上学期期末考试化学试题
名校
5 . Ⅰ.某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5 μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系________ (填“属于”或“不属于”)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为_____ (填“酸”或“碱”)性,表示该试样酸碱性的c(H+)或c(OH-)=______ mol·L-1。
Ⅱ.氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(3)“维生素C可以将食物中的Fe3+转化为Fe2+,说明维生素C______ 具有(填“氧化性”或“还原性”)。
(4)二氧化氯是一种高效消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中每生成1molClO2分子,转移电子的数目为_____ 。
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是_____ 。
A.O2 B.FeCl2 C.KCl D.KMnO4
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ |  |  |  | Cl- |
| 浓度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
Ⅱ.氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(3)“维生素C可以将食物中的Fe3+转化为Fe2+,说明维生素C
(4)二氧化氯是一种高效消毒剂。工业上制备ClO2的反应为2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl。
①该反应中每生成1molClO2分子,转移电子的数目为
②ClO2在杀菌消毒的过程中会生成副产物亚氯酸盐(
 ),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是
),需要将其转化为Cl-除去,下列试剂能实现其转化过程的是A.O2 B.FeCl2 C.KCl D.KMnO4
您最近一年使用:0次
2024-02-14更新
|
48次组卷
|
2卷引用:河南省漯河市高级中学2023-2024学年高一上学期模拟预测化学试题
6 . 将 气体通入
气体通入 溶液中完全反应后,再滴加溴水,发生如下两个反应:①
溶液中完全反应后,再滴加溴水,发生如下两个反应:①
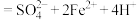 ,②
,② ,下列有关说法错误的是
,下列有关说法错误的是
 气体通入
气体通入 溶液中完全反应后,再滴加溴水,发生如下两个反应:①
溶液中完全反应后,再滴加溴水,发生如下两个反应:①
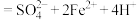 ,②
,② ,下列有关说法错误的是
,下列有关说法错误的是A.还原性: |
B. 气体不能使溴水褪色 气体不能使溴水褪色 |
C.向 溶液中逐滴滴加溴水,溶液变黄 溶液中逐滴滴加溴水,溶液变黄 |
D.反应①中消耗32 g  气体时,转移电子数为 气体时,转移电子数为 |
您最近一年使用:0次
2024-02-12更新
|
440次组卷
|
2卷引用:河南省南阳市六校2023-2024学年高一上学期1月期末化学试题
7 . 将 通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应:
通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应: 。当
。当 完全反应时,下列说法正确的是
完全反应时,下列说法正确的是
 通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应:
通入含amolNaOH的溶液中,反应会放热,温度升高后发生反应: 。当
。当 完全反应时,下列说法正确的是
完全反应时,下列说法正确的是A.反应中作氧化剂的 有 有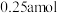 |
B.若反应后溶液中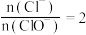 ,则 ,则 |
C. 与 与 的物质的量之和可能为 的物质的量之和可能为 |
D.反应中转移电子的物质的量可能为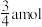 |
您最近一年使用:0次
名校
解题方法
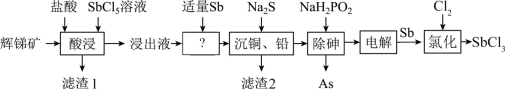
8 . SbCl3用于红外光谱分析以及显像管生产等。工业生产中,以辉锑矿(主要成分为的Sb2S3,还含有As2S3、PbS、CuO和SiO2等)为原料制备SbCl3的工艺流程如下:
②常温下, ,
, ;
;
③溶液中离子浓度小于或等于 mol/L时,认为该离子沉淀完全。
mol/L时,认为该离子沉淀完全。
回答下列问题:
(1)加快辉锑矿“酸浸”的措施有 。
(2)滤渣1中除了S之外,还有__________ 。
(3)浸出液中加入适量Sb的目的是________________________ 。(用化学方程式表示)
(4)已知浸出液中c(Cu2+)=0.01mol/L、c(Pb2+)=0.10mol/L。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是__________ (填化学式);常温下,“除铜、铅”时Cu2+和Pb2+均沉淀完全,此时溶液中 不低于
不低于__________ mol/L,Na2S也不宜过多,其原因为__________________ 。
(5)在“除砷”过程中,氧化产物为H3PO4,则该反应中氧化剂、还原剂的物质的量之比为___________ ;已知在“电解”SbCl3溶液时,无气体生成,被氧化的Sb元素与被还原的Sb元素的质量之比为3:2,可在上述流程中循环利用的物质有_________________ 。
②常温下,
 ,
, ;
;③溶液中离子浓度小于或等于
 mol/L时,认为该离子沉淀完全。
mol/L时,认为该离子沉淀完全。回答下列问题:
(1)加快辉锑矿“酸浸”的措施有 。
| A.将辉锑矿粉碎 | B.用酒精灯加热 | C.用玻璃棒搅拌 | D.适当增加酸液浓度 |
(3)浸出液中加入适量Sb的目的是
(4)已知浸出液中c(Cu2+)=0.01mol/L、c(Pb2+)=0.10mol/L。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是
 不低于
不低于(5)在“除砷”过程中,氧化产物为H3PO4,则该反应中氧化剂、还原剂的物质的量之比为
您最近一年使用:0次
2024-01-13更新
|
449次组卷
|
5卷引用:河南省焦作市博爱县第一中学2023-2024学年高三下学期开学化学试题
9 . 在“天宫课堂”中航天员王亚平介绍了空间站中的生活,在轨演示了水球变气球等一系列炫酷又好玩的实验。
I.“天宫”中水和氧气最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。

(1)“水电解系统”中产生氧气发生反应的化学方程式为___________ ,每转移4mol电子,生成的O2在标况下的体积为___________ 。
(2)在水净化系统中,用臭氧(O3)消毒。氧气在放电条件下转化为臭氧的化学方程式为___________ ,该反应___________ (填“是”或“否”)氧化还原反应,原因是___________ 。
(3)一定条件 “萨巴蒂尔反应器”可除去CO2,该反应化学方程式为___________ 。
Ⅱ.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不逸出,使水球越来越大。
(4)泡腾片在水中发生了如下反应:
H3C6H5O7+3NaHCO3=Na3C6H5O7+3CO2↑+3___________ (补全化学方程式)。
I.“天宫”中水和氧气最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。

(1)“水电解系统”中产生氧气发生反应的化学方程式为
(2)在水净化系统中,用臭氧(O3)消毒。氧气在放电条件下转化为臭氧的化学方程式为
(3)一定条件 “萨巴蒂尔反应器”可除去CO2,该反应化学方程式为
Ⅱ.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不逸出,使水球越来越大。
(4)泡腾片在水中发生了如下反应:
H3C6H5O7+3NaHCO3=Na3C6H5O7+3CO2↑+3
您最近一年使用:0次
2024-01-12更新
|
19次组卷
|
2卷引用:河南省焦作市博爱县第一中学2023-2024学年高二下学期开学化学试题
名校
解题方法
10 . 向含有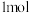
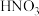 和
和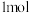
 的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有
的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有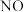 )。下列有关判断不正确的是
)。下列有关判断不正确的是
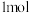
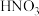 和
和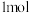
 的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有
的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有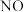 )。下列有关判断不正确的是
)。下列有关判断不正确的是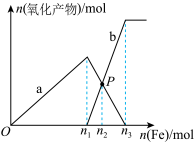
A.a表示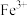 的关系曲线 的关系曲线 |
B. =0.75 =0.75 |
C.P点时,n(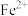 )=0.5625mol )=0.5625mol |
| D.向P点溶液中加入铜粉,最多可溶解14.4g |
您最近一年使用:0次
2024-01-10更新
|
792次组卷
|
16卷引用:河南省商丘市第一高级中学2021-2022学年高一下学期期中考试化学试题
河南省商丘市第一高级中学2021-2022学年高一下学期期中考试化学试题(已下线)2011-2012学年山西省高三上学期第二次阶段性测试化学试卷2016届浙江省杭州高级中学高三上学期月考(三)化学试卷【全国百强校】安徽省合肥市第六中学2018-2019学年高一下学期开学考试化学试题(已下线)2019年8月11日《每日一题》2020年高考一轮复习—— 每周一测(已下线)专题3.3 铁及其重要化合物(练)——2020年高考化学一轮复习讲练测人教版2019必修第二册 第五章 本章复习提升湖南省长沙市第一中学2019-2020学年高一上学期第二次阶段性检测(月考)化学试题辽宁省沈阳市第四十中学2021-2022年高一下学期4月份线上教学效果检测化学试题陕西省西安中学 2023 届高三上学期第二次质量检测化学试题西安市第八十三中学2022-2023学年高一下学期第一次月考化学试题辽宁省重点高中沈阳市郊联体2023-2024学年高一上学期期末考试化学试题新疆乌鲁木齐市新疆生产建设兵团第二中学2023-2024学年高一上学期期末考试化学试卷 (已下线)热点02 氮及其化合物浙江省杭州市源清中学2023-2024学年高一上学期期末考试化学试题黑龙江省双鸭山市第一中学2023-2024学年高一下学期4月月考化学试题



