名校
1 . 火药的发明推进了人类历史发展的进程。火药爆炸的原理为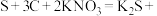
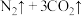 。下列说法错误的是
。下列说法错误的是
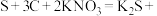
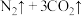 。下列说法错误的是
。下列说法错误的是A.从得失电子角度看,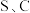 在反应中的作用不同 在反应中的作用不同 |
B.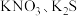 均属于钾盐 均属于钾盐 |
| C.该反应过程属于氮的固定 |
D.该反应每转移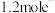 ,生成标准状况下 ,生成标准状况下 气体 气体 |
您最近半年使用:0次
7日内更新
|
65次组卷
|
2卷引用:吉林省白山市抚松县第一中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
2 . 1962年化学家N.Bartlett基于以下两点合成了第一个含有化学键的“惰性气体”化合物——登黄色固体配合物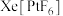 。
。
①一个现象: 能够氧化
能够氧化 生成
生成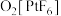 。
。
②一个事实: 的电离能
的电离能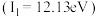 与
与 的电离能
的电离能 相近。
相近。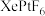 不溶于
不溶于 ,遇水则迅速分解,并放出气体:
,遇水则迅速分解,并放出气体: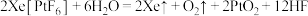 。
。
以 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
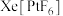 。
。①一个现象:
 能够氧化
能够氧化 生成
生成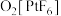 。
。②一个事实:
 的电离能
的电离能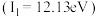 与
与 的电离能
的电离能 相近。
相近。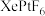 不溶于
不溶于 ,遇水则迅速分解,并放出气体:
,遇水则迅速分解,并放出气体: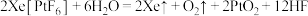 。
。以
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.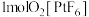 固体中阳离子含有的电子数为 固体中阳离子含有的电子数为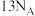 |
B. 中,含有 中,含有 键数为 键数为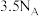 |
C.反应产生 (标况) (标况) ,转移的电子数为 ,转移的电子数为 |
D. 固体中中阴阳离子数共有 固体中中阴阳离子数共有 |
您最近半年使用:0次
名校
3 . 新制氢氧化铜和葡萄糖的反应可用来检验血糖,其反应为:CH2OH(CHOH)4CHO+2Cu(OH)2+NaOH CH2OH(CHOH)4COONa+Cu2O↓+3H2O,设
CH2OH(CHOH)4COONa+Cu2O↓+3H2O,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 CH2OH(CHOH)4COONa+Cu2O↓+3H2O,设
CH2OH(CHOH)4COONa+Cu2O↓+3H2O,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.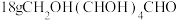 中含有羟基的数目为 中含有羟基的数目为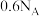 |
B.每消耗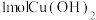 ,转移电子的数目为 ,转移电子的数目为 |
C.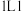   溶液中含有的离子数目为 溶液中含有的离子数目为 |
D.标准状况下,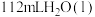 中含有的分子数目约为 中含有的分子数目约为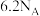 |
您最近半年使用:0次
2024-05-04更新
|
247次组卷
|
2卷引用:2024届吉林省通化市梅河口市第五中学高三下学期二模化学试题
名校
4 . 据研究, 在酸性条件下可用铁屑脱除,反应原理为
在酸性条件下可用铁屑脱除,反应原理为 。设
。设 为阿伏加德罗常数的值,下列叙述中错误的是
为阿伏加德罗常数的值,下列叙述中错误的是
 在酸性条件下可用铁屑脱除,反应原理为
在酸性条件下可用铁屑脱除,反应原理为 。设
。设 为阿伏加德罗常数的值,下列叙述中错误的是
为阿伏加德罗常数的值,下列叙述中错误的是A.酸性条件下的氧化性: |
B.反应过程中溶液的 减小 减小 |
C.脱除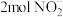 ,转移的电子数为 ,转移的电子数为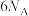 |
| D.该反应可设计成原电池 |
您最近半年使用:0次
名校
解题方法
5 . 硅及其化合物在生产生活中有重要用途。
(1)用氮化硅 陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为
陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为 。
。
① 的电子式为
的电子式为___________ 。
②若该反应转移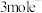 ,生成
,生成 的质量为
的质量为___________ g。
(2)芯片制作中的部分流程如图: 溶液与单晶硅反应生成
溶液与单晶硅反应生成 溶液,
溶液, 溶液俗称水玻璃,水玻璃可用作
溶液俗称水玻璃,水玻璃可用作___________ 。
②扩散制结过程发生反应I. ;反应Ⅱ.
;反应Ⅱ.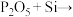
 。
。
配平反应Ⅱ.___________ 
___________ Si=___________ SiO2+___________ P,该反应的反应类型为___________ (填四大基本反应类型)。
③去除磷硅玻璃即除去扩散制结过程中产生的 ,下列试剂合适的为
,下列试剂合适的为___________ (填标号),写出其化学方程式:___________ 。
a.浓硫酸 b.氢氟酸 c.稀硝酸
(1)用氮化硅
 陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为
陶瓷制造发动机,能大幅度提高发动机的热效率。工业上制备氮化硅的原理为 。
。①
 的电子式为
的电子式为②若该反应转移
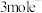 ,生成
,生成 的质量为
的质量为(2)芯片制作中的部分流程如图:

 溶液与单晶硅反应生成
溶液与单晶硅反应生成 溶液,
溶液, 溶液俗称水玻璃,水玻璃可用作
溶液俗称水玻璃,水玻璃可用作②扩散制结过程发生反应I.
 ;反应Ⅱ.
;反应Ⅱ.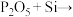
 。
。配平反应Ⅱ.

③去除磷硅玻璃即除去扩散制结过程中产生的
 ,下列试剂合适的为
,下列试剂合适的为a.浓硫酸 b.氢氟酸 c.稀硝酸
您最近半年使用:0次
2024-04-28更新
|
41次组卷
|
2卷引用:吉林省白山市抚松县第一中学2023-2024学年高一下学期4月月考化学试题
名校
6 . 某同学为测定 和
和 混合粉末中
混合粉末中 的含量。将
的含量。将 和
和 混合粉末加入
混合粉末加入 的稀硝酸中,得到
的稀硝酸中,得到 气体
气体 (标准状况下),忽略溶液体积的变化。下列有关说法正确的是
(标准状况下),忽略溶液体积的变化。下列有关说法正确的是
 和
和 混合粉末中
混合粉末中 的含量。将
的含量。将 和
和 混合粉末加入
混合粉末加入 的稀硝酸中,得到
的稀硝酸中,得到 气体
气体 (标准状况下),忽略溶液体积的变化。下列有关说法正确的是
(标准状况下),忽略溶液体积的变化。下列有关说法正确的是| A.反应后有固体剩余 | B.反应后的溶液中 |
C. 单质在混合粉末中的质量分数约为 单质在混合粉末中的质量分数约为 | D.在反应后的溶液中加入足量铁粉,可畳换出 |
您最近半年使用:0次
2024-04-28更新
|
103次组卷
|
2卷引用:吉林省白山市抚松县第一中学2023-2024学年高一下学期4月月考化学试题
名校
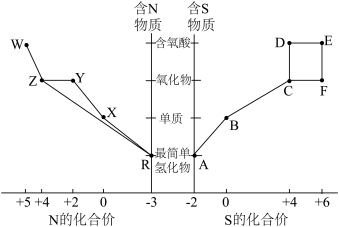
7 . 元素的“价类二维图”体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。回答下列问题: 反应的化学方程式
反应的化学方程式______
(2)下列有关图中所示含N、S物质的叙述,正确的是______ (填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠( ),从氧化还原反应的角度分析,可选择B和D反应
),从氧化还原反应的角度分析,可选择B和D反应
(3)写出B与氢氧化钠溶液反应的离子反应方程式______
(4)将物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是______ 。
(5) (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: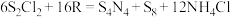 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有______ ,该反应每生成 转移电子
转移电子______ mol。
 反应的化学方程式
反应的化学方程式(2)下列有关图中所示含N、S物质的叙述,正确的是
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与NaOH溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(
 ),从氧化还原反应的角度分析,可选择B和D反应
),从氧化还原反应的角度分析,可选择B和D反应(3)写出B与氢氧化钠溶液反应的离子反应方程式
(4)将物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是
(5)
 (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: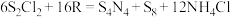 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有 转移电子
转移电子
您最近半年使用:0次
名校
8 . 空气中的灰尘、硫酸、硝酸等颗粒物组成的气溶胶系统造成视觉障碍的叫霾。科研人员提出了雾霾微颗粒中硫酸盐(含SO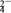 、HSO
、HSO )生成的三个阶段的转化机理,其主要过程示意图如图,下列说法错误的是
)生成的三个阶段的转化机理,其主要过程示意图如图,下列说法错误的是
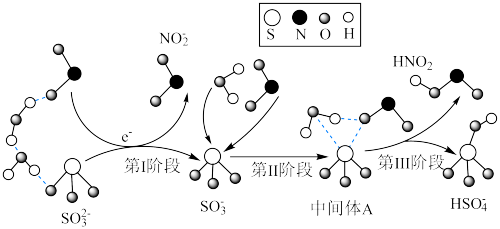
A.SO 和NO 和NO 的中心原子的杂化轨道类型分别是:sp3、sp2 的中心原子的杂化轨道类型分别是:sp3、sp2 |
| B.整个过程中有H2O参加反应,而且包含了硫氧键的断裂与形成 |
C.1molSO 在第Ⅱ、Ⅲ两个阶段共失去电子数目为NA 在第Ⅱ、Ⅲ两个阶段共失去电子数目为NA |
D.硫酸盐转化过程中发生的总反应方程式为:SO +2NO2+H2O=HSO +2NO2+H2O=HSO +NO +NO +HNO2 +HNO2 |
您最近半年使用:0次
2024-04-19更新
|
232次组卷
|
2卷引用:吉林省吉林地区普通高中2024届高三三模考试化学试卷
名校
9 . 常温常压下,电化学合成氨总反应方程式: ,设
,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 ,设
,设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 氮气含有的共用电子对数为 氮气含有的共用电子对数为 |
B.每产生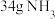 , , 失去电子数为 失去电子数为 |
C. 氨水中,含 氨水中,含 分子数小于 分子数小于 |
D.标况下,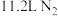 参加反应时,产生 参加反应时,产生 分子数为 分子数为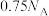 |
您最近半年使用:0次
2024-04-16更新
|
414次组卷
|
4卷引用:吉林省长春市2023-2024学年高三下学期质量监测(三)化学试题
解题方法
10 . 环氧乙烷( ,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如图,一定条件下,反应物按一定流速通过该装置。
,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如图,一定条件下,反应物按一定流速通过该装置。
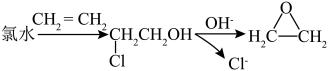
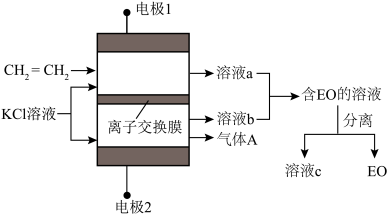
已知:电解效率η(B)= ×100%;
×100%;
下列说法正确的是
 ,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如图,一定条件下,反应物按一定流速通过该装置。
,简称EO)是一种重要的工业原料和消毒剂。由乙烯经电解制备EO的原理示意图如图,一定条件下,反应物按一定流速通过该装置。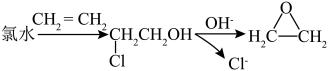

已知:电解效率η(B)=
 ×100%;
×100%;下列说法正确的是
| A.电极1应与电源正极相连,离子交换膜应为阴离子交换膜 |
| B.若η(EO)=100%,则溶液c的溶质为KCl |
| C.不考虑各项损失,理论上生成2g气体A,可得到产品EO88g |
| D.每生成1molEO,理论上电路中转移电子数为NA |
您最近半年使用:0次



