已知 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是
 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是A.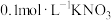 溶液中离子总数大于 溶液中离子总数大于 |
B.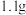 的 的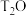 ,含有的质子数为 ,含有的质子数为 |
C. 与足量的 与足量的 反应转移的电子数为 反应转移的电子数为 |
D. 和 和 充分反应,转移电子数为 充分反应,转移电子数为 |
更新时间:2024-03-10 17:30:03
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加德罗常数的值。下列说法正确的是
A.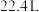 (标准状况)臭氧气体中所含的质子数为18NA (标准状况)臭氧气体中所含的质子数为18NA |
B.  和 和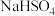 的固体混合物中含有的离子总数为0.4NA 的固体混合物中含有的离子总数为0.4NA |
C.实验室制得  转移的电子数不一定为2NA 转移的电子数不一定为2NA |
D. 氮气与足量金属镁反应,转移的电子数为0.4NA 氮气与足量金属镁反应,转移的电子数为0.4NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设NA为阿伏加 德罗常数的数值,下列说法正确的是( )
| A.电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64 g |
| B.0.1 mol KI与0.1 mol FeCl3在溶液中反应转移的电子数为0.1NA |
| C.1 L 0.5 mol·L-1醋酸钠溶液中阴、阳离子总数目大于NA |
D.0.1 mol环氧乙烷(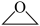 )中含有共价键的总数约为0.3×6.02×1023 )中含有共价键的总数约为0.3×6.02×1023 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】无水 在空气中易潮解,加热易升华。实验室利用反应
在空气中易潮解,加热易升华。实验室利用反应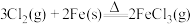 制取无水
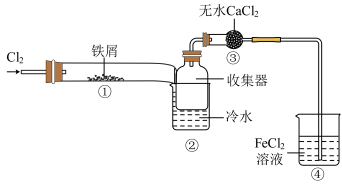
制取无水 ,实验装置如图所示(加热和夹持装置略去)。下列说法正确的是( )
,实验装置如图所示(加热和夹持装置略去)。下列说法正确的是( )
 在空气中易潮解,加热易升华。实验室利用反应
在空气中易潮解,加热易升华。实验室利用反应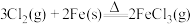 制取无水
制取无水 ,实验装置如图所示(加热和夹持装置略去)。下列说法正确的是( )
,实验装置如图所示(加热和夹持装置略去)。下列说法正确的是( )
A.实验开始时应先加热①处,再通入干燥的 |
B.②处冷水的作用是降低 的溶解度 的溶解度 |
C.装置③可用盛有浓 的洗气瓶代替 的洗气瓶代替 |
D.④中溶液经蒸发后可获得无水 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】NA为阿伏加德罗常数,下列说法正确的是
| A.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
| B.标准状况下,22.4 L NH3中含有电子数为8NA |
| C.1 mol Cl2与足量Fe反应转移电子数为3NA |
| D.1 mol·L-1的AlCl3溶液中, Cl-的数目为3NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】含Ru(钌)化合物可催化 转化为甲酸,其反应机理如图所示。
转化为甲酸,其反应机理如图所示。
 转化为甲酸,其反应机理如图所示。
转化为甲酸,其反应机理如图所示。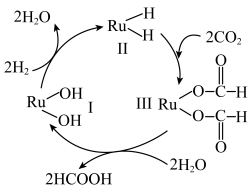
| A.1mol物质Ⅰ转化为物质Ⅱ时,反应过程中转移4mol电子 |
| B.物质Ⅱ→Ⅲ过程中,Ru元素化合价保持不变 |
| C.整个过程中,有非极性键的断裂与形成 |
| D.反应结束后,体系中水的量增多 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:2H2O(l)=2H2(g)+O2(g) ΔH=+571.0 kJ/mol。以太阳能为热源分解Fe3O4,经热化学铁氧化合物循环分解水制H2的过程如下:
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2 kJ/mol
过程Ⅱ:…
过程Ⅰ:2Fe3O4(s)=6FeO(s)+O2(g) ΔH=+313.2 kJ/mol
过程Ⅱ:…
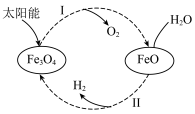
| A.过程Ⅰ中每消耗232 g Fe3O4转移2 mol电子 |
| B.过程Ⅱ的热化学方程式为3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH=+128.9 kJ/mol |
| C.过程Ⅰ、Ⅱ中能量转化的形式依次是太阳能→化学能→热能 |
| D.铁氧化合物循环制H2具有成本低、产物易分离等优点 |
您最近半年使用:0次


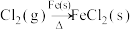


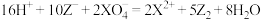 ,②
,②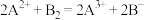 ,③
,③ 。由此推断下列说法不正确的是
。由此推断下列说法不正确的是 具有还原性
具有还原性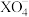 ,转移电子5mol
,转移电子5mol 可以进行
可以进行

