回答下列问题。
(1)神舟十三飞船以 和
和 为动力源,发生反应:
为动力源,发生反应: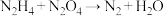 (未配平),反应温度可高达
(未配平),反应温度可高达 ,回答下列问题。
,回答下列问题。
①配平方程式并用双线桥标出电子转移的方向和数目:___________ 。
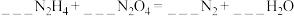 。
。
②氧化产物与还原产物的质量之比为___________ 。
(2)家庭中常用84消毒液(主要成分为 )与洁则灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
)与洁则灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
①“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式:___________ 。
②某届奥运会期间,由于工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(1)神舟十三飞船以
 和
和 为动力源,发生反应:
为动力源,发生反应: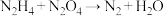 (未配平),反应温度可高达
(未配平),反应温度可高达 ,回答下列问题。
,回答下列问题。①配平方程式并用双线桥标出电子转移的方向和数目:
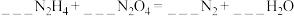 。
。②氧化产物与还原产物的质量之比为
(2)家庭中常用84消毒液(主要成分为
 )与洁则灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。
)与洁则灵(主要成分为盐酸)清洁卫生。某品牌消毒液包装上说明如下图。| 注意事项: 1.本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用 2.密封保存,请勿与洁厕灵同时使用 3.保质期为一年 |
②某届奥运会期间,由于工作人员将84消毒液与双氧水混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是
 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
 (填“>”或“<”)。
(填“>”或“<”)。
更新时间:2024-02-20 16:09:50
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】填空。
(1)请将下列4种物质:N2O、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个化学方程式并配平___________ 。24FeSO4+_______=_______+_____+_______+_____H2O
(2)用单线桥表示电子转移过程___________ 。
(1)请将下列4种物质:N2O、Fe(NO3)3、HNO3和Fe2(SO4)3分别填入下面对应的横线上,组成一个化学方程式并配平
(2)用单线桥表示电子转移过程
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求回答下列问题:
(1)1molNa2O2中约含__ 个氧原子;等物质的量的SO2和O2的质量比是__ ,同温同压下的体积比是___ 。
(2)现有100mLNa2SO4溶液,其中含Na+2.3g,则Na+的物质的量为__ mol,取10mL该溶液稀释至100mL,稀释后SO 的物质的量浓度为
的物质的量浓度为__ mol•L-1。
(3)核内中子数为N的R2+,质子数为A,则该离子的核外电子数为__ ,mg氯化物RCl2的物质的量是__ mol。
(4)镁能在二氧化碳中燃烧,其反应的化学方程式为2Mg+CO2 2MgO+C,该反应的还原剂为
2MgO+C,该反应的还原剂为__ ,请用双线桥法标出该反应电子转移的方向和数目___ 。
(1)1molNa2O2中约含
(2)现有100mLNa2SO4溶液,其中含Na+2.3g,则Na+的物质的量为
 的物质的量浓度为
的物质的量浓度为(3)核内中子数为N的R2+,质子数为A,则该离子的核外电子数为
(4)镁能在二氧化碳中燃烧,其反应的化学方程式为2Mg+CO2
 2MgO+C,该反应的还原剂为
2MgO+C,该反应的还原剂为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】能将KI氧化为I2的若干种氧化剂有H2O2、Cl2、KIO3、HNO3,KClO3、KMnO4等。
(1)上述试剂最适合贴上的一个标签是___ (填序号)。
(2)配平方程式:KClO3+KI+H2SO4=K2SO4+KCl+I2+H2O,___ 。已知过量KClO3会引起副反应:KClO3+I2→KIO3+Cl2,据此判断:KClO3和KIO3相比,氧化性较强的是___ 。
(3)写出KI溶液与Cl2反应的离子方程式___ 。
(4)以单线桥法表示下列氧化还原反应的电子转移:H2O2+2H++3I-=I +2H2O
+2H2O___ 。
(5)已知下列四种氧化剂(氧化KI后)对应的还原产物情况如下:
请判断,等物质的量的四种氧化剂分别与足量KI作用,得到I2最多的是___ 。
(6)根据信息“氧化性Cl2>Br2>HNO3>I2”思考:对于I-、Br-混合溶液,若控制氧化I-而不氧化Br-,请提出两种合理的氧化方案:①加入___ ;②加入___ 。
(1)上述试剂最适合贴上的一个标签是
A. | B. | C. | D. |
(3)写出KI溶液与Cl2反应的离子方程式
(4)以单线桥法表示下列氧化还原反应的电子转移:H2O2+2H++3I-=I
 +2H2O
+2H2O(5)已知下列四种氧化剂(氧化KI后)对应的还原产物情况如下:
| 氧化剂 | KMnO4 | KIO3 | H2O2 | HNO3 |
| 还原产物 | Mn2+ | I2 | H2O | NO |
请判断,等物质的量的四种氧化剂分别与足量KI作用,得到I2最多的是
(6)根据信息“氧化性Cl2>Br2>HNO3>I2”思考:对于I-、Br-混合溶液,若控制氧化I-而不氧化Br-,请提出两种合理的氧化方案:①加入
您最近一年使用:0次
【推荐2】高锰酸钾在不同的条件下发生的反应如下:
①MnO4-+5e-+8H+=Mn2++4H2O ②MnO4-+3e-+2H2O=MnO2↓+4OH-
(1)从上述两个反应中可以看出高锰酸根离子被还原的产物受溶液的__________ 影响。
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为________ →__________ 。
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法不正确的是___________ 。
A.氧化性,PbO2>KMnO4B.还原性:PbO2>KMnO4C.该反应可以用盐酸酸化
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比 为3 : 2,完成下列化学方程式(横线上填系数,括号内填物质):
①_____ KMnO4+_____ K2S+ ______ ( ) =____ K2MnO4+_____ K2SO4+____ S↓+_________ ( ) 。
②若生成6.4g单质硫,反应过程中转移电子的物质的量为____________ 。
①MnO4-+5e-+8H+=Mn2++4H2O ②MnO4-+3e-+2H2O=MnO2↓+4OH-
(1)从上述两个反应中可以看出高锰酸根离子被还原的产物受溶液的
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法不正确的是
A.氧化性,PbO2>KMnO4B.还原性:PbO2>KMnO4C.该反应可以用盐酸酸化
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比 为3 : 2,完成下列化学方程式(横线上填系数,括号内填物质):
①
②若生成6.4g单质硫,反应过程中转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列各题:
(1)相同质量的O2和O3所含氧原子的个数比为______ ,标准状况下气体的体积之比为_______ ;
某19g二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是_______ 。
(2)某反应中反应物与生成物有:NH3、H2SO4、KClO3、K2SO4、HNO3、H2O和一种未知物质X。
①已知 KClO3在反应中得到电子,则该反应的还原剂是____ 。
②已知 0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为____ 。
③根据上述反应可推知还原性: NH3____ X (填>、<符号)。
(3)已知反应:
①SO3+H2O=H2SO4 ②Cl2+H2O=HCl+HClO ③2F2+H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑ ⑤Na2O+H2O=2NaOH ⑥Fe2O3+3H2 2Fe+3H2O
2Fe+3H2O
上述反应中,不属于氧化还原反应的有_________ (填序号,下同);H2O只做氧化剂的是_____ ;属于氧化还原反应,但反应物中的H2O既不被氧化也不被还原的是________ 。
(4)反应2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O能制备氯气,该反应中,氧化剂是______________ 。反应中被氧化的HCl和未被氧化HCl的物质的量之比为________ 。
(5)铜与稀硫酸、双氧水混合能制备硫酸铜,写出反应的离子方程式:_______________________ 。
(1)相同质量的O2和O3所含氧原子的个数比为
某19g二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是
(2)某反应中反应物与生成物有:NH3、H2SO4、KClO3、K2SO4、HNO3、H2O和一种未知物质X。
①已知 KClO3在反应中得到电子,则该反应的还原剂是
②已知 0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为
③根据上述反应可推知还原性: NH3
(3)已知反应:
①SO3+H2O=H2SO4 ②Cl2+H2O=HCl+HClO ③2F2+H2O=4HF+O2
④2Na+2H2O=2NaOH+H2↑ ⑤Na2O+H2O=2NaOH ⑥Fe2O3+3H2
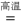 2Fe+3H2O
2Fe+3H2O上述反应中,不属于氧化还原反应的有
(4)反应2KMnO4+16HCl(浓)=2MnCl2+2KCl+5Cl2↑+8H2O能制备氯气,该反应中,氧化剂是
(5)铜与稀硫酸、双氧水混合能制备硫酸铜,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铁是目前产量最大、使用最广泛的金属。
(1)铁元素26号元素,位于周期表第四周期第_______ 族,其原子最外电子层上只有2个电子,次外层上有_______ 个电子。
(2)写出下列反应的化学方程式或离子方程式。
①高温下,铁跟水蒸气反应的化学方程式是:_______ 。
②已知锰元素的常见化合价有+7、+6、+4、+2等,则加热条件下,铁、锰合金粉未跟 反应的化学方程为:
反应的化学方程为:_______ 、_______ 。
③已知 溶液跟
溶液跟 反应有红褐色
反应有红褐色 沉淀生成,且溶液呈棕黄色,则反应的离子方程式为:
沉淀生成,且溶液呈棕黄色,则反应的离子方程式为:_______ 。
(3) 与
与 混合后在缺氧条件下焙烧生成
混合后在缺氧条件下焙烧生成 和
和 ,理论上完全反应消耗的
,理论上完全反应消耗的
_______ ,
(4)石墨稀负载的纳米铁活性强,能迅速有效地吸附和还原污水中的 ,纳米铁还原废水中
,纳米铁还原废水中 的可能反应机理如图表示。纳米铁还原
的可能反应机理如图表示。纳米铁还原 生成
生成 或
或 的过程可描述为:
的过程可描述为:
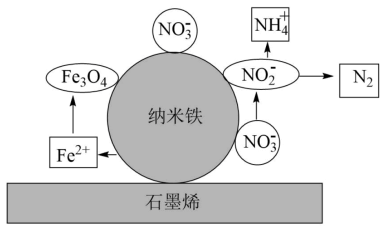
①_______ ,
②吸附在纳米铁表面的 得到的电子还原生成
得到的电子还原生成 ,
,
③_______ 。
(1)铁元素26号元素,位于周期表第四周期第
(2)写出下列反应的化学方程式或离子方程式。
①高温下,铁跟水蒸气反应的化学方程式是:
②已知锰元素的常见化合价有+7、+6、+4、+2等,则加热条件下,铁、锰合金粉未跟
 反应的化学方程为:
反应的化学方程为:③已知
 溶液跟
溶液跟 反应有红褐色
反应有红褐色 沉淀生成,且溶液呈棕黄色,则反应的离子方程式为:
沉淀生成,且溶液呈棕黄色,则反应的离子方程式为:(3)
 与
与 混合后在缺氧条件下焙烧生成
混合后在缺氧条件下焙烧生成 和
和 ,理论上完全反应消耗的
,理论上完全反应消耗的
(4)石墨稀负载的纳米铁活性强,能迅速有效地吸附和还原污水中的
 ,纳米铁还原废水中
,纳米铁还原废水中 的可能反应机理如图表示。纳米铁还原
的可能反应机理如图表示。纳米铁还原 生成
生成 或
或 的过程可描述为:
的过程可描述为:
①
②吸附在纳米铁表面的
 得到的电子还原生成
得到的电子还原生成 ,
,③
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氧化还原反应在物质制备、能量转化方面有重要的应用。
(1)用单线桥法表示下列反应的电子转移方向和数目。___________

(2)反应 常用于测定溶液中I2的含量。反应的还原剂是
常用于测定溶液中I2的含量。反应的还原剂是___________ ,每生成1moLNaI,反应转移电子___________ mol。
(3)反应 KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O中氧化剂与还原剂的物质的量之比为___________ 。
(4)高铁酸钾(K2FeO4)可作为高效、多功能水处理剂。用FeCl3与KClO在强碱条件下反应可制取高铁酸钾,完成反应的离子方程式。___________
2Fe3++______ClO-+______OH-=______FeO +3Cl-+______
+3Cl-+______
(1)用单线桥法表示下列反应的电子转移方向和数目。

(2)反应
 常用于测定溶液中I2的含量。反应的还原剂是
常用于测定溶液中I2的含量。反应的还原剂是(3)反应 KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O中氧化剂与还原剂的物质的量之比为
(4)高铁酸钾(K2FeO4)可作为高效、多功能水处理剂。用FeCl3与KClO在强碱条件下反应可制取高铁酸钾,完成反应的离子方程式。
2Fe3++______ClO-+______OH-=______FeO
 +3Cl-+______
+3Cl-+______
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知反应:①Fe+H2SO4(稀)=FeSO4+H2↑;②Cu+2H2SO4(浓)  CuSO4+SO2↑+2H2O。试回答下列问题:
CuSO4+SO2↑+2H2O。试回答下列问题:
(1)反应①中_______ (填元素符号,下同)被氧化,还原产物为_____ ;反应②中______ 做还原剂,_____ 元素被还原。
(2)当反应①中生成2 g H2时,消耗H2SO4的质量是_____________ g。
(3)当反应②中生成32 g SO2时,消耗H2SO4的质量是_________ ,其中有_________ g H2SO4被还原。
 CuSO4+SO2↑+2H2O。试回答下列问题:
CuSO4+SO2↑+2H2O。试回答下列问题:(1)反应①中
(2)当反应①中生成2 g H2时,消耗H2SO4的质量是
(3)当反应②中生成32 g SO2时,消耗H2SO4的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氯气是一种重要的化工原料,在生产生活中具有广泛的应用。
(1)实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
①写出实验室制取氯气的化学方程式_______ 。若产生标准状况下4.48 LCl2,则反应过程中被氧化的HCl的物质的量是_______ mol。
②为了防止氯气污染环境,需将剩余氯气通入_______ ,发生的化学反应方程式_______ 。
③实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下: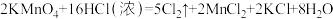 。在此反应中浓盐酸中显示出来的性质是
。在此反应中浓盐酸中显示出来的性质是_______ (填写字母)
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)电解饱和食盐水生产氢气、氯气、氢氧化钠,氯气与石灰乳反应可制取漂白粉。干燥的漂白粉不能发挥漂白效果,请写出漂白粉能发挥漂白效果的化学反应方程式_______ 。
(1)实验室常用二氧化锰和浓盐酸共热的方法制取氯气。根据要求回答下列问题。
①写出实验室制取氯气的化学方程式
②为了防止氯气污染环境,需将剩余氯气通入
③实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
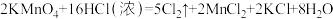 。在此反应中浓盐酸中显示出来的性质是
。在此反应中浓盐酸中显示出来的性质是A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)电解饱和食盐水生产氢气、氯气、氢氧化钠,氯气与石灰乳反应可制取漂白粉。干燥的漂白粉不能发挥漂白效果,请写出漂白粉能发挥漂白效果的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】类比推理是化学学习中的一种分析问题的重要方法,在科学研究中有重要意义。
(1)下列叙述中正确的是___________。
(2)已知铅元素在化合物中的主要化合价有+2、+4两种,且+2价为稳定价态。
① 可以表示为
可以表示为 ,则
,则 可表示为
可表示为___________ 。
② 与浓盐酸在加热条件下反应的化学方程式为
与浓盐酸在加热条件下反应的化学方程式为___________ 。
(3)已知 有强氧化性,可被
有强氧化性,可被 气体还原为
气体还原为 ,请结合硫元素的价类图,按要求写出以下反应方程式:
,请结合硫元素的价类图,按要求写出以下反应方程式:
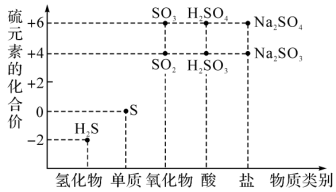
①在 溶液中通入
溶液中通入 气体,该反应的离子方程式为
气体,该反应的离子方程式为___________ 。
② 气体与
气体与 反应的化学方程式为
反应的化学方程式为___________ 。
(1)下列叙述中正确的是___________。
A.在含1mol溶质的 溶液中加入足量NaOH溶液,可生成 溶液中加入足量NaOH溶液,可生成 沉淀,若用等量的 沉淀,若用等量的 溶液,也可制得含 溶液,也可制得含 个胶粒的 个胶粒的 胶体 胶体 |
| B.金属钠与水能剧烈反应,则金属钾与水的反应会更加剧烈 |
C.84消毒液和 均可以用于杀菌消毒,二者混合后杀菌消毒效果更好 均可以用于杀菌消毒,二者混合后杀菌消毒效果更好 |
| D.碱性氧化物均为金属氧化物,酸性氧化物均为非金属氧化物 |
①
 可以表示为
可以表示为 ,则
,则 可表示为
可表示为②
 与浓盐酸在加热条件下反应的化学方程式为
与浓盐酸在加热条件下反应的化学方程式为(3)已知
 有强氧化性,可被
有强氧化性,可被 气体还原为
气体还原为 ,请结合硫元素的价类图,按要求写出以下反应方程式:
,请结合硫元素的价类图,按要求写出以下反应方程式:
①在
 溶液中通入
溶液中通入 气体,该反应的离子方程式为
气体,该反应的离子方程式为②
 气体与
气体与 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氯碱工业是现代化工的基础。
(1)电解饱和食盐水时,氯气在___________ (填电极名称)产生。检验另一电极附近溶液中产物,可选用___________ (填试剂名称)
(2)氯碱工业中,电解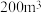
 食盐水,一段时间后,NaCl的浓度变为
食盐水,一段时间后,NaCl的浓度变为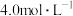 ,则这段时间电解产生的气体在标准状况下的总体积为
,则这段时间电解产生的气体在标准状况下的总体积为___________ 。(不考虑溶液体积变化以及气体溶解损失)
(3)从海水中获取粗盐的方法是___________ 。氯化钠在做焰色反应时焰色为___________ 。
(4)电解饱和食盐水须用高纯度食盐,食盐精制过程中须除去 、
、 、
、 等杂质离子,依次加入的除杂试剂是:
等杂质离子,依次加入的除杂试剂是:___________ (填化学式)。
(5)氯原子的结构示意图为___________ 。氯有 和
和 两种核素,氯元素的相对原子质量为35.5,则
两种核素,氯元素的相对原子质量为35.5,则 的丰度为
的丰度为___________ 。
(6)如图,a处通入氯气。若打开b,d处有色布条不褪色;若关闭b.d处的有色布条褪色。则___________。
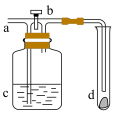
(7)氯水中含有的弱电解质是___________ 。用自来水养金鱼时,应先将水“放置”一段时间,目的是___________ (用化学方程式表示)。
(1)电解饱和食盐水时,氯气在
(2)氯碱工业中,电解
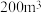
 食盐水,一段时间后,NaCl的浓度变为
食盐水,一段时间后,NaCl的浓度变为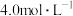 ,则这段时间电解产生的气体在标准状况下的总体积为
,则这段时间电解产生的气体在标准状况下的总体积为(3)从海水中获取粗盐的方法是
(4)电解饱和食盐水须用高纯度食盐,食盐精制过程中须除去
 、
、 、
、 等杂质离子,依次加入的除杂试剂是:
等杂质离子,依次加入的除杂试剂是:(5)氯原子的结构示意图为
 和
和 两种核素,氯元素的相对原子质量为35.5,则
两种核素,氯元素的相对原子质量为35.5,则 的丰度为
的丰度为(6)如图,a处通入氯气。若打开b,d处有色布条不褪色;若关闭b.d处的有色布条褪色。则___________。

| A.a处通入的可能是潮湿的氯 |
| B.c中盛放的可能是浓硫酸或氢氧化钠溶液 |
| C.c中盛放的可能是饱和食盐水 |
| D.d中放置的一定是干燥的有色布条 |
(7)氯水中含有的弱电解质是
您最近一年使用:0次

 碳纳米颗粒
碳纳米颗粒 这种碳纳米颗粒可用氧化气化法提纯
这种碳纳米颗粒可用氧化气化法提纯 标准状况下
标准状况下

