铜及其化合物在生产生活有广泛应用,铜在化合物中的常见化合价有+1、+2.已知 与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
(1)工业上可用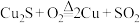 反应制取粗铜,该反应中
反应制取粗铜,该反应中___________ 元素被还原。不考虑杂质的反应,理论上生成1mol的 电子转移的数目为
电子转移的数目为___________
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为___________ 。温度控制在50~60℃的原因除了加快反应速率外,还有___________ 。在 溶液中加入一定量的
溶液中加入一定量的 和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:
和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:___________ 。
(3)现向Cu、 和CuO组成的混合物中,加入2L 0.6
和CuO组成的混合物中,加入2L 0.6
 溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。
溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。 跟稀硝酸反应的离子方程式为
跟稀硝酸反应的离子方程式为___________ 。若将上述混合物用足量的 加热还原,所得到固体的质量为
加热还原,所得到固体的质量为___________ g。若上述混合物中含0.2mol Cu,将该混合物与稀硫酸充分反应,消耗 的物质的量为
的物质的量为___________ mol。
 与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。(1)工业上可用
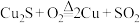 反应制取粗铜,该反应中
反应制取粗铜,该反应中 电子转移的数目为
电子转移的数目为(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入
 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为 溶液中加入一定量的
溶液中加入一定量的 和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:
和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:(3)现向Cu、
 和CuO组成的混合物中,加入2L 0.6
和CuO组成的混合物中,加入2L 0.6
 溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。
溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。 跟稀硝酸反应的离子方程式为
跟稀硝酸反应的离子方程式为 加热还原,所得到固体的质量为
加热还原,所得到固体的质量为 的物质的量为
的物质的量为
更新时间:2024-05-06 14:51:13
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】纳米铁粉可用于处理地下水中的污染物。
(1)一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH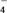 (B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)
(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)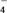 ,其离子方程式为
,其离子方程式为_____________________________________________ 。
(2)纳米铁粉与水中NO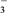 反应的离子方程式为4Fe+ NO
反应的离子方程式为4Fe+ NO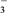 +10H+===4Fe2++NH
+10H+===4Fe2++NH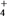 +3H2O,研究发现,若pH偏低将会导致NO
+3H2O,研究发现,若pH偏低将会导致NO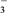 的去除率下降,其原因是
的去除率下降,其原因是_______________________________________ 。
(3)相同条件下,纳米铁粉去除不同水样中NO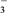 的速率有较大差异(见图),产生该差异的可能原因是
的速率有较大差异(见图),产生该差异的可能原因是____________________________ 。

Ⅰ含50 mg·L-1 NO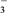 的水样
的水样
Ⅱ含50 mg·L-1 NO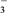 +50 mg·L-1 Cu2+的水样
+50 mg·L-1 Cu2+的水样
(1)一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH
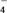 (B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)
(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)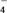 ,其离子方程式为
,其离子方程式为(2)纳米铁粉与水中NO
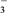 反应的离子方程式为4Fe+ NO
反应的离子方程式为4Fe+ NO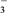 +10H+===4Fe2++NH
+10H+===4Fe2++NH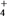 +3H2O,研究发现,若pH偏低将会导致NO
+3H2O,研究发现,若pH偏低将会导致NO 的去除率下降,其原因是
的去除率下降,其原因是(3)相同条件下,纳米铁粉去除不同水样中NO
 的速率有较大差异(见图),产生该差异的可能原因是
的速率有较大差异(见图),产生该差异的可能原因是
Ⅰ含50 mg·L-1 NO
 的水样
的水样Ⅱ含50 mg·L-1 NO
 +50 mg·L-1 Cu2+的水样
+50 mg·L-1 Cu2+的水样
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】硫化钠俗称臭碱,是重要的化工原料,工业上可用氢氧化钠吸收硫化氢气体制备。
(1)已知:
若用硫化钠固体和下列溶液制取硫化氢气体,可选用的试剂为_______ 。
a.硝酸 b.碳酸氢钠 c.硼酸 d.醋酸
将少量CO2通入Na2S溶液中,写出发生反应的离子方程式_______ 。
(2)某小组同学为检验Na2S变质的产物中是否含有Na2S2O3,设计实验:取久置潮解的Na2S固体溶于水,静置,取少量上层清液于试管中,向其中滴加AgNO3溶液,产生黑色沉淀。由此得出结论:Na2S变质的产物中含Na2S2O3。该实验是否合理_______ (填“是”或“否”),请分析原因_______ 。(已知:白色的Ag2S2O3难溶于水,且易转化为黑色Ag2S)
(3)设计实验证明Na2S的还原性比FeCl2的还原性强:_______ (写出必要的实验操作、现象和结论)。
(1)已知:
| H2S | H3BO3 | H2CO3 | CH3COOH |
| Ka1=9.1×10-8 Ka2=1.1×10-12 | Ka=5.8×10-10 | Ka1=4.4×10-7 Ka2=4.7×10-11 | Ka=1.75×10-5 |
若用硫化钠固体和下列溶液制取硫化氢气体,可选用的试剂为
a.硝酸 b.碳酸氢钠 c.硼酸 d.醋酸
将少量CO2通入Na2S溶液中,写出发生反应的离子方程式
(2)某小组同学为检验Na2S变质的产物中是否含有Na2S2O3,设计实验:取久置潮解的Na2S固体溶于水,静置,取少量上层清液于试管中,向其中滴加AgNO3溶液,产生黑色沉淀。由此得出结论:Na2S变质的产物中含Na2S2O3。该实验是否合理
(3)设计实验证明Na2S的还原性比FeCl2的还原性强:
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】I.有反应:
(1)该反应所属的基本反应类型是_____ 。
(2)在反应中铁元素的化合价变化是_____ ,该元素的原子_____ (填“失去”或“得到”)电子。
(3)发生还原反应的是_____ (填化学式)。
II.KClO3和浓盐酸在一定温度下反应会生成黄绿色的有毒气体氯气。其变化可表示为:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
(4)请将上述反应改写成离子方程式_____ 。
(5)浓盐酸在反应中体现出来的性质有_____ (填序号)。
①还原性②酸性③氧化性④碱性

(1)该反应所属的基本反应类型是
(2)在反应中铁元素的化合价变化是
(3)发生还原反应的是
II.KClO3和浓盐酸在一定温度下反应会生成黄绿色的有毒气体氯气。其变化可表示为:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
(4)请将上述反应改写成离子方程式
(5)浓盐酸在反应中体现出来的性质有
①还原性②酸性③氧化性④碱性
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】已知两种相邻周期、相邻主族的短周期非金属元素X、Y,其最高价氧化物的水化物均为强酸。根据如图转化关系(反应条件及部分产物已略去),回答下列问题:

(1)若A、B、C、D均为含X元素的化合物,且A和F的分子均为10电子微粒,则:
①F属于_______ (填“离子化合物”或“共价化合物”)。
②反应I的化学方程式为_______ 。
③将1.92g铜粉与一定量的D的浓溶液反应,当铜粉完全反应时收集到气体1.12L(标准状况),则反应消耗的D的物质的量为_______ mol。
(2)若A、B、C、D均为含Y元素的化合物,其中A由两种元素组成,且A的摩尔质量为34 g/mol,则:
①将铜粉与D的浓溶液反应所得溶液加热蒸干,得到的白色固体物质为_______ (填化学式)。
②将少量Na2Y溶液滴加到次氯酸钠溶液中发生反应,无沉淀生成,请写出该反应的离子反应方程式_______ 。在该反应中若有74.5 g NaClO被还原,则转移电子的物质的量为_______ mol。

(1)若A、B、C、D均为含X元素的化合物,且A和F的分子均为10电子微粒,则:
①F属于
②反应I的化学方程式为
③将1.92g铜粉与一定量的D的浓溶液反应,当铜粉完全反应时收集到气体1.12L(标准状况),则反应消耗的D的物质的量为
(2)若A、B、C、D均为含Y元素的化合物,其中A由两种元素组成,且A的摩尔质量为34 g/mol,则:
①将铜粉与D的浓溶液反应所得溶液加热蒸干,得到的白色固体物质为
②将少量Na2Y溶液滴加到次氯酸钠溶液中发生反应,无沉淀生成,请写出该反应的离子反应方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】 是一种锂离子电池的正极材料。用
是一种锂离子电池的正极材料。用 在一定条件下可制得
在一定条件下可制得 。回答下列问题:
。回答下列问题:
(1)写出 在周期表中的位置
在周期表中的位置___________ 。
(2)将 进行热分解,在
进行热分解,在 时,固体残留率为
时,固体残留率为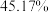 ,写出残留固体(
,写出残留固体( )的化学式
)的化学式___________ (已知:固体残留率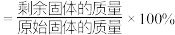 )。
)。
(3)将固体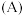 与
与 混合并在空气中煅烧,反应生成
混合并在空气中煅烧,反应生成 ,写出该反应中氧化剂与还原剂物质的之比
,写出该反应中氧化剂与还原剂物质的之比___________ 。
(4)该正极材料充电一段时间后变为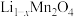 ,为测定
,为测定 的值。称取
的值。称取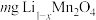 固体,经一系列化学处理,将锂全部转化为
固体,经一系列化学处理,将锂全部转化为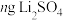 ,写出
,写出 的表达式
的表达式___________ 。
 是一种锂离子电池的正极材料。用
是一种锂离子电池的正极材料。用 在一定条件下可制得
在一定条件下可制得 。回答下列问题:
。回答下列问题:(1)写出
 在周期表中的位置
在周期表中的位置(2)将
 进行热分解,在
进行热分解,在 时,固体残留率为
时,固体残留率为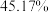 ,写出残留固体(
,写出残留固体( )的化学式
)的化学式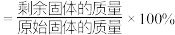 )。
)。(3)将固体
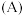 与
与 混合并在空气中煅烧,反应生成
混合并在空气中煅烧,反应生成 ,写出该反应中氧化剂与还原剂物质的之比
,写出该反应中氧化剂与还原剂物质的之比(4)该正极材料充电一段时间后变为
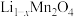 ,为测定
,为测定 的值。称取
的值。称取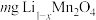 固体,经一系列化学处理,将锂全部转化为
固体,经一系列化学处理,将锂全部转化为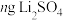 ,写出
,写出 的表达式
的表达式
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】K3[Fe(C2O4)3](三草酸合铁酸钾)可用于摄影和蓝色印刷。工业上以H2C2O4(草酸)、FeC2O4(草酸亚铁)、K2C2O4(草酸钾)、双氧水等为原料制备K3[Fe(C2O4)3]的反应原理如下:
氧化:6FeC2O4+3H2O2+6K2C2O4═4K3[Fe(C2O4)3]+2Fe(OH)3
转化:2Fe(OH)3+3K2C2O4+3H2C2O4═2K3[Fe(C2O4)3]+6H2O
(1)制备1mol三草酸合铁酸钾至少需要H2O2的物质的量为____________ 。
(2)制备过程中需防止草酸被H2O2氧化,写出草酸被H2O2氧化的化学方程式:______________ 。
(3)[K3[Fe(C2O4)3·xH2O](三草酸合铁酸钾晶体)是一种光敏材料,为测定该晶体中草酸根的含量和结晶水的含量,某实验小组进行了如下实验:
①称量9.820g三草酸合铁酸钾晶体,配制成250mL溶液.
②取所配溶液25.00mL于锥形瓶中,滴加KMnO4溶液至C2O42-全部转化成CO2时,恰好消耗24.00mL 0.1000mol/L KMnO4溶液。
计算该晶体的化学式,并写出计算过程______________ 。
氧化:6FeC2O4+3H2O2+6K2C2O4═4K3[Fe(C2O4)3]+2Fe(OH)3
转化:2Fe(OH)3+3K2C2O4+3H2C2O4═2K3[Fe(C2O4)3]+6H2O
(1)制备1mol三草酸合铁酸钾至少需要H2O2的物质的量为
(2)制备过程中需防止草酸被H2O2氧化,写出草酸被H2O2氧化的化学方程式:
(3)[K3[Fe(C2O4)3·xH2O](三草酸合铁酸钾晶体)是一种光敏材料,为测定该晶体中草酸根的含量和结晶水的含量,某实验小组进行了如下实验:
①称量9.820g三草酸合铁酸钾晶体,配制成250mL溶液.
②取所配溶液25.00mL于锥形瓶中,滴加KMnO4溶液至C2O42-全部转化成CO2时,恰好消耗24.00mL 0.1000mol/L KMnO4溶液。
计算该晶体的化学式,并写出计算过程
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】用Cl2消毒会使饮用水中的有机物发生氯化,生成有机氯化合物,于人体有害。世界环保联盟即将全面禁止用氯气对饮用水消毒。建议推广采用广谱性高效消毒剂ClO2气体。
(1)目前,欧洲一些国家用NaClO3氧化浓盐酸制取ClO2,同时有Cl2生成,且Cl2体积为ClO2的一半,该反应的化学方程式是:_______________________________________ 。
(2)我国最近研究成功用氯气氧化亚氯酸钠(NaClO2,N2保护下)制ClO2,其反应的化学方程式为:____________________________________________________________ ,
这一反应的优点是:_____________________________________________________ 。
(3)在H2SO4存在的条件下,用Na2SO3还原NaClO3也可制ClO2,其反应的化学方程式为:______________________________________________________________________ 。
(1)目前,欧洲一些国家用NaClO3氧化浓盐酸制取ClO2,同时有Cl2生成,且Cl2体积为ClO2的一半,该反应的化学方程式是:
(2)我国最近研究成功用氯气氧化亚氯酸钠(NaClO2,N2保护下)制ClO2,其反应的化学方程式为:
这一反应的优点是:
(3)在H2SO4存在的条件下,用Na2SO3还原NaClO3也可制ClO2,其反应的化学方程式为:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】完成下列填空。
(1)已知A、B、C、D为气体,其中A、B为单质,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:
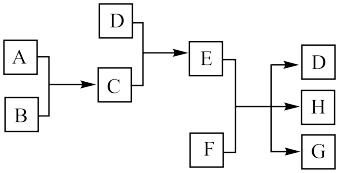
请回答下列问题:
①C的化学式是______ ,D的电子式为______ 。
②如何检验E溶液中阳离子?______ 。
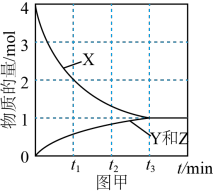
(2)在高压下,NO在 下分解生成两种化合物,体系中各组分的物质的量随时间变化曲线如图甲所示。NO分解的化学方程式为
下分解生成两种化合物,体系中各组分的物质的量随时间变化曲线如图甲所示。NO分解的化学方程式为______ 。
(3)有色金属提取工艺中会产生大量含氰(CN·)废水,对环境造成了极大的负担。在碱性条件下可用ClO-将其氧化成 和
和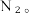 写出反应的离子方程式:
写出反应的离子方程式:______ 。
(4)向酸性废水中加入NaClO,消除 污染。写出相应的离子方程式为
污染。写出相应的离子方程式为______ 。
(5)将软锰矿与硫铁矿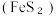 粉碎混合,用硫酸浸取。研究发现,酸浸时,
粉碎混合,用硫酸浸取。研究发现,酸浸时, 和
和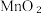 颗粒构成两个原电池反应,其原理如图所示(部分产物未标出)。
颗粒构成两个原电池反应,其原理如图所示(部分产物未标出)。
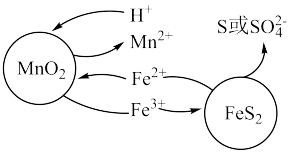
若 原电池中生成单质S,其反应的离子方程式为
原电池中生成单质S,其反应的离子方程式为______ 。
(1)已知A、B、C、D为气体,其中A、B为单质,E、F为固体,G是氯化钙,它们之间的转换关系如下图所示:

请回答下列问题:
①C的化学式是
②如何检验E溶液中阳离子?
(2)在高压下,NO在
 下分解生成两种化合物,体系中各组分的物质的量随时间变化曲线如图甲所示。NO分解的化学方程式为
下分解生成两种化合物,体系中各组分的物质的量随时间变化曲线如图甲所示。NO分解的化学方程式为
(3)有色金属提取工艺中会产生大量含氰(CN·)废水,对环境造成了极大的负担。在碱性条件下可用ClO-将其氧化成
 和
和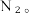 写出反应的离子方程式:
写出反应的离子方程式:(4)向酸性废水中加入NaClO,消除
 污染。写出相应的离子方程式为
污染。写出相应的离子方程式为(5)将软锰矿与硫铁矿
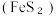 粉碎混合,用硫酸浸取。研究发现,酸浸时,
粉碎混合,用硫酸浸取。研究发现,酸浸时, 和
和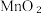 颗粒构成两个原电池反应,其原理如图所示(部分产物未标出)。
颗粒构成两个原电池反应,其原理如图所示(部分产物未标出)。
若
 原电池中生成单质S,其反应的离子方程式为
原电池中生成单质S,其反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】今年春天以来,内蒙古自治区降水较常年偏少、气温偏高。进入7月以后,全区过半地域最高温度超过30℃以上,中西部地区有17个站点,最高温度超过35℃,阿拉善盟极高温度达到40℃。旱情牵动了全国人民的心。水是组成生命体的重要化学物质,有关水的反应有很多。
(1)水分子自身作用会生成阴、阳两种离子,其中阳离子的电子式是______________________ 。
(2)在由水电离产生的c(H+)=1×10-14molL-1的溶液中①NH4+、A13+、Br-、SO42-;②Na+、Mg2+、Cl-、NO3-;③K+、Ba2+、Cl-、NO3-;④K+、 Na+、HCO3-、SO42-四组离子中。一定可以大量共存的是______ (填序号,下同),可能大量共存的是_____________ 。
(3)在下列中,水既不作氧化剂又不作还原剂是_____________ (填序号)。
A.Cl2+H2O=HCl+HClO B.2Na2O2+2H2O==4NaOH+O2↑
C.CaH2+2H2O==Ca(OH)2+2H2↑ D.3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
(4)将钠、钾分别投入有少量相同质量的稀H2SO4中,反应结束后,两种溶液的质量仍相等而金属均无剩余,则投入的钠、钾的质量比为_____________ 。
(5)三氟化氮(NF3)是一种无色无味的气体,27.0mL NF3和水充分反应,生成18.0mLNO(同温、同压下),写出反应的化学方程式:_________________ 。
(1)水分子自身作用会生成阴、阳两种离子,其中阳离子的电子式是
(2)在由水电离产生的c(H+)=1×10-14molL-1的溶液中①NH4+、A13+、Br-、SO42-;②Na+、Mg2+、Cl-、NO3-;③K+、Ba2+、Cl-、NO3-;④K+、 Na+、HCO3-、SO42-四组离子中。一定可以大量共存的是
(3)在下列中,水既不作氧化剂又不作还原剂是
A.Cl2+H2O=HCl+HClO B.2Na2O2+2H2O==4NaOH+O2↑
C.CaH2+2H2O==Ca(OH)2+2H2↑ D.3Fe+4H2O
 Fe3O4+4H2
Fe3O4+4H2(4)将钠、钾分别投入有少量相同质量的稀H2SO4中,反应结束后,两种溶液的质量仍相等而金属均无剩余,则投入的钠、钾的质量比为
(5)三氟化氮(NF3)是一种无色无味的气体,27.0mL NF3和水充分反应,生成18.0mLNO(同温、同压下),写出反应的化学方程式:
您最近一年使用:0次
【推荐1】铜是重要的工业原料,现有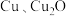 组成的混合物,某研究性学习小组为了探究其组成情况,取
组成的混合物,某研究性学习小组为了探究其组成情况,取 该混合物加入
该混合物加入 的稀硝酸中,固体物质完全反应,溶液中铜元素均为
的稀硝酸中,固体物质完全反应,溶液中铜元素均为 ,且生成
,且生成 (标准状况)的
(标准状况)的 。向所得溶液中加入
。向所得溶液中加入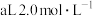 的
的 溶液,恰好使溶液中的
溶液,恰好使溶液中的 沉淀完全。
沉淀完全。
(1) 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为___________ ;
(2)
___________ L。
(3)求混合物中 的质量分数
的质量分数___________ ?(没有计算过程不得分)
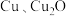 组成的混合物,某研究性学习小组为了探究其组成情况,取
组成的混合物,某研究性学习小组为了探究其组成情况,取 该混合物加入
该混合物加入 的稀硝酸中,固体物质完全反应,溶液中铜元素均为
的稀硝酸中,固体物质完全反应,溶液中铜元素均为 ,且生成
,且生成 (标准状况)的
(标准状况)的 。向所得溶液中加入
。向所得溶液中加入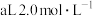 的
的 溶液,恰好使溶液中的
溶液,恰好使溶液中的 沉淀完全。
沉淀完全。(1)
 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为(2)

(3)求混合物中
 的质量分数
的质量分数
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】化学实验 化学是一门以实验为基础的学科。请回答以下问题:
(1)对下列事实的解释正确的是
(2)将盛有 12 mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积是
(3)CuBr 是一种白色晶体,见光或潮湿时受热易分解。实验室制备CuBr的反应原理为SO2+2CuSO4+2NaBr+2H2O=2CuBr+2H2SO4+Na2SO4,用下列装置进行实验,不能达到实验目的的是

(4)实验室中要制取少量蒸馏水,其装置如下图所示:
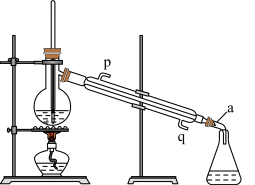
①仪器 a 的名称为_______ ,冷凝水应从_______ (选填“p”或“q”)口进入冷凝管。
②请指出图中装置的一处明显错误:_______ 。
③现需480 mL 0.1 mol/L 的CuSO4溶液,所需的玻璃仪器有烧杯、胶头滴管、_____ 、_____ ; 在配制过程中,需要用电子天平称取胆矾的质量为_______ g。
(5)某校为了改进碳与浓硝酸反应的实验,设计了如图所示的装置。实验步骤:先预热盛有无水氯化钙的烧瓶,然后投入几小块红热的炭块,再缓缓向炭块上滴加浓硝酸,反应即可连续发生。请完成下列空白。
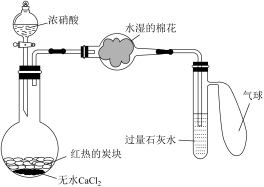
①烧瓶中反应的化学方程式为_______ ,烧瓶中的现象是_______ 。
②水湿棉花的作用是_______ ,气球的作用是_______ 。
(1)对下列事实的解释正确的是
| A.蘸有浓硫酸和蘸有浓氨水的玻璃棒靠近没有白烟,说明硫酸与氨气不反应 |
| B.医疗上可用硫酸钡作 X 射线透视肠胃的内服药,是因为硫酸钡不溶于酸 |
| C.向 50 mL 18 mol·L-1的H2SO4溶液中加入足量的铜片加热充分反应后,被还原的H2SO4的物质的量为0.45 mol |
| D.常温下,浓H2SO4可以用铝制容器贮存,说明铝与浓硫酸不反应 |
| A.1.2mL | B.2.4 mL | C.3.6mL | D.4mL |

| A.用装置甲制取 SO2 | B.用装置乙制取 CuBr |
| C.用装置丙避光将 CuBr 与母液分离 | D.用装置丁干燥 CuBr |

①仪器 a 的名称为
②请指出图中装置的一处明显错误:
③现需480 mL 0.1 mol/L 的CuSO4溶液,所需的玻璃仪器有烧杯、胶头滴管、
(5)某校为了改进碳与浓硝酸反应的实验,设计了如图所示的装置。实验步骤:先预热盛有无水氯化钙的烧瓶,然后投入几小块红热的炭块,再缓缓向炭块上滴加浓硝酸,反应即可连续发生。请完成下列空白。

①烧瓶中反应的化学方程式为
②水湿棉花的作用是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】铁在热的稀 中反应,其主要还原产物为
中反应,其主要还原产物为 ,而在冷的稀
,而在冷的稀 中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为
中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为 。请分析如图,回答有关问题。
。请分析如图,回答有关问题。
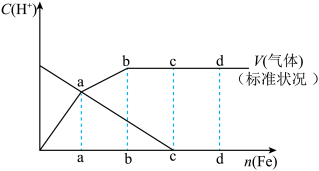
(1)假设在任一气体产生的曲线段内只有一种还原产物,试配平由b点到c点时的化学反应方程式:_____ Fe+____ HNO3—____ Fe(NO3)3+_________ +____ H2O
(2)判断从o点到a点时的还原产物,应是___________
(3)a点到b点时产生还原产物为_________ ,其原因是______________
(4)已知达到d点时反应完全结束,此时溶液中的主要阳离子为____________ 。
 中反应,其主要还原产物为
中反应,其主要还原产物为 ,而在冷的稀
,而在冷的稀 中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为
中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为 。请分析如图,回答有关问题。
。请分析如图,回答有关问题。 
(1)假设在任一气体产生的曲线段内只有一种还原产物,试配平由b点到c点时的化学反应方程式:
(2)判断从o点到a点时的还原产物,应是
(3)a点到b点时产生还原产物为
(4)已知达到d点时反应完全结束,此时溶液中的主要阳离子为
您最近一年使用:0次



