铁在热的稀 中反应,其主要还原产物为
中反应,其主要还原产物为 ,而在冷的稀
,而在冷的稀 中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为
中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为 。请分析如图,回答有关问题。
。请分析如图,回答有关问题。
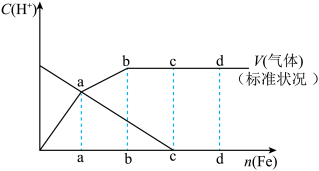
(1)假设在任一气体产生的曲线段内只有一种还原产物,试配平由b点到c点时的化学反应方程式:_____ Fe+____ HNO3—____ Fe(NO3)3+_________ +____ H2O
(2)判断从o点到a点时的还原产物,应是___________
(3)a点到b点时产生还原产物为_________ ,其原因是______________
(4)已知达到d点时反应完全结束,此时溶液中的主要阳离子为____________ 。
 中反应,其主要还原产物为
中反应,其主要还原产物为 ,而在冷的稀
,而在冷的稀 中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为
中反应,其主要还原产物为NO,当溶液更稀时,其还原产物为 。请分析如图,回答有关问题。
。请分析如图,回答有关问题。 
(1)假设在任一气体产生的曲线段内只有一种还原产物,试配平由b点到c点时的化学反应方程式:
(2)判断从o点到a点时的还原产物,应是
(3)a点到b点时产生还原产物为
(4)已知达到d点时反应完全结束,此时溶液中的主要阳离子为
更新时间:2020-01-26 09:04:56
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】次磷酸(H3PO2)是一种精细磷化工产品,具有较强的还原性.回答下列问题:
(1)H3PO2与足量的NaOH溶液反应,生成NaH2PO2,则H3PO2为______ 元酸,其电离方程式是__________ .
(2)H3PO2是中强酸,写出其与NaHCO3溶液反应的离子方程式______________________ .
(3)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银.
①H3PO2中,P元素的化合价为__________ ;
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则其氧化产物为_____________ ;(填化学式)
(4)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式____________ .
(1)H3PO2与足量的NaOH溶液反应,生成NaH2PO2,则H3PO2为
(2)H3PO2是中强酸,写出其与NaHCO3溶液反应的离子方程式
(3)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银.
①H3PO2中,P元素的化合价为
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则其氧化产物为
(4)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4反应,写出白磷与Ba(OH)2溶液反应的化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】I、实验室中可以用高锰酸钾和浓盐酸反应制取氯气,化学反应如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)上述反应中的氧化剂是_________ ,还原剂与还原产物的物质的量之比为______ 。
(2)如果反应生成5mol氯气,则过程中转移的电子数为________ 个。
II、按要求完成离子方程式。
(3)写出向明矾[KAl(SO4)2]溶液中加入氢氧化钡到Al3+完全沉淀的离子方程式:_________ 。
(4)完成以下氧化还原反应的离子方程式:__________________
( )MnO4 -+( )C2O42- +____ =( )Mn2++( )CO2↑+_____
(1)上述反应中的氧化剂是
(2)如果反应生成5mol氯气,则过程中转移的电子数为
II、按要求完成离子方程式。
(3)写出向明矾[KAl(SO4)2]溶液中加入氢氧化钡到Al3+完全沉淀的离子方程式:
(4)完成以下氧化还原反应的离子方程式:
( )MnO4 -+( )C2O42- +____ =( )Mn2++( )CO2↑+_____
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】硫化氢广泛存在于燃气及废水中,热分解或氧化硫化氢有利于环境保护并回收硫资源。回答下列问题:
(1)写出 的电子式:
的电子式:_______ 。
(2) 与
与 溶液反应可生成两种酸式盐,该反应的离子方程式为
溶液反应可生成两种酸式盐,该反应的离子方程式为_______ 。
(3)氯气可用于除去废水中 ,写出反应的化学方程式:
,写出反应的化学方程式:_______ 。
(4)将含 尾气的空气按一定流速通入酸性
尾气的空气按一定流速通入酸性 溶液中,可实现含
溶液中,可实现含 尾气的空气脱硫。在
尾气的空气脱硫。在 溶液吸收
溶液吸收 的过程中也发生了反应
的过程中也发生了反应 ,溶液中的
,溶液中的 及被吸收的
及被吸收的 随时间t的变化如图所示。
随时间t的变化如图所示。

① 时刻前,溶液中
时刻前,溶液中 减小速率较快,
减小速率较快, 时刻后,溶液中
时刻后,溶液中 基本不变,其原因是
基本不变,其原因是_______ 。
②预测 时刻后,
时刻后, 的物质的量变化趋势,并在图中补充完整。
的物质的量变化趋势,并在图中补充完整。_______
(5)科学家设计出质子膜 燃料电池,实现了利用
燃料电池,实现了利用 废气资源回收能量并得到单质硫。质子膜
废气资源回收能量并得到单质硫。质子膜 燃料电池的结构如图所示。
燃料电池的结构如图所示。

①电极b极为_______ (填“正极”或“负极”),写出该电极的电极反应式:_______ 。
②电池工作时, 经质子膜进入
经质子膜进入_______ (填“a极”或“b极”)区。
(1)写出
 的电子式:
的电子式:(2)
 与
与 溶液反应可生成两种酸式盐,该反应的离子方程式为
溶液反应可生成两种酸式盐,该反应的离子方程式为(3)氯气可用于除去废水中
 ,写出反应的化学方程式:
,写出反应的化学方程式:(4)将含
 尾气的空气按一定流速通入酸性
尾气的空气按一定流速通入酸性 溶液中,可实现含
溶液中,可实现含 尾气的空气脱硫。在
尾气的空气脱硫。在 溶液吸收
溶液吸收 的过程中也发生了反应
的过程中也发生了反应 ,溶液中的
,溶液中的 及被吸收的
及被吸收的 随时间t的变化如图所示。
随时间t的变化如图所示。
①
 时刻前,溶液中
时刻前,溶液中 减小速率较快,
减小速率较快, 时刻后,溶液中
时刻后,溶液中 基本不变,其原因是
基本不变,其原因是②预测
 时刻后,
时刻后, 的物质的量变化趋势,并在图中补充完整。
的物质的量变化趋势,并在图中补充完整。(5)科学家设计出质子膜
 燃料电池,实现了利用
燃料电池,实现了利用 废气资源回收能量并得到单质硫。质子膜
废气资源回收能量并得到单质硫。质子膜 燃料电池的结构如图所示。
燃料电池的结构如图所示。
①电极b极为
②电池工作时,
 经质子膜进入
经质子膜进入
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】储氢纳米碳管的研制成功体现了科技的进步。用电弧法合成的纳米碳管常伴有大量的杂质碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,反应中的反应物和生成物有C、CO2、H2SO4、KCr2O7、Cr2(SO4)2、H2O七种物质。
(1)若将碳纳米颗粒分散到一定溶剂中,形成稳定的分散系,所具的性质有_____
①丁达尔效应②加入饱和(NH4)2SO4溶液产生聚沉③可通过半透膜
(2)请用上述物质填空,配平化学方程式,并标出电子转移的方向和数目( ) C+_______ +_____ H2SO4→____ K2SO4+______ +_____ Cr2(SO4)3+____ H2O
(3)将标准状况下4.48 L产生的气体通入适量的NaOH溶液中充分反应后,溶液中生成盐的质量为19.0g。
(I)若要使生成的盐的质量变为25.2 g,则应继续向溶液中通入该气体___ g。
(Ⅱ)向生成的19.0 g的盐溶液中加入一定量某物质,充分反应后,减压低温蒸发得到纯净的21.2 g Na2CO3固体。则:
①若只能加入0.05 mol某物质,则加入的物质可以是______ 或________ 。
②若只能加入0.10 mol某物质,则加入的物质可以是______ 或________ 。
(1)若将碳纳米颗粒分散到一定溶剂中,形成稳定的分散系,所具的性质有
①丁达尔效应②加入饱和(NH4)2SO4溶液产生聚沉③可通过半透膜
(2)请用上述物质填空,配平化学方程式,并标出电子转移的方向和数目
(3)将标准状况下4.48 L产生的气体通入适量的NaOH溶液中充分反应后,溶液中生成盐的质量为19.0g。
(I)若要使生成的盐的质量变为25.2 g,则应继续向溶液中通入该气体
(Ⅱ)向生成的19.0 g的盐溶液中加入一定量某物质,充分反应后,减压低温蒸发得到纯净的21.2 g Na2CO3固体。则:
①若只能加入0.05 mol某物质,则加入的物质可以是
②若只能加入0.10 mol某物质,则加入的物质可以是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】重铬酸钠(Na2Cr2O7)广泛用作氧化剂、鞣革剂等。以铬矿石(主要成分为Cr2O3,还含有FeO、A12O3、SiO2等杂质)为原料制取重铬酸钠的流程如下:

请回答下列问题:
(1)Cr2O3在高温焙烧时反应的化学方程式为_____ 。
(2)生产过程中,调节(含Na2CrO4、Na2SiO3、NaAlO2的溶液)pH的目的是_______ 。
(3)某化工厂采用石墨作电极电解Na2CrO4溶液,实现了Na2CrO4转化为Na2Cr2O7的生产,其原理如下图所示。
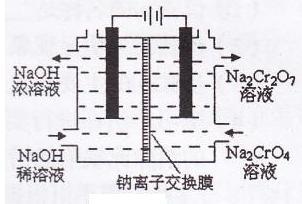
①写出阳极的电极方程式:________ ;
②此生产方法和上述流程相比的优点主要有_____ 。
(4)Na2Cr2O7可用于测定废水的化学耗氧量(即COD,指每升水样中还原性物质被氧化所需要的O2的质量)。现有某水样100.00 mL,酸化后加入clmol/L的Na2Cr2O7溶液V1mL,使水中的还原性物质完全被氧化(还原产物为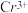 );再用c2 mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2mL。则该水样的COD为
);再用c2 mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2mL。则该水样的COD为___ mg/L。

请回答下列问题:
(1)Cr2O3在高温焙烧时反应的化学方程式为
(2)生产过程中,调节(含Na2CrO4、Na2SiO3、NaAlO2的溶液)pH的目的是
(3)某化工厂采用石墨作电极电解Na2CrO4溶液,实现了Na2CrO4转化为Na2Cr2O7的生产,其原理如下图所示。

①写出阳极的电极方程式:
②此生产方法和上述流程相比的优点主要有
(4)Na2Cr2O7可用于测定废水的化学耗氧量(即COD,指每升水样中还原性物质被氧化所需要的O2的质量)。现有某水样100.00 mL,酸化后加入clmol/L的Na2Cr2O7溶液V1mL,使水中的还原性物质完全被氧化(还原产物为
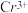 );再用c2 mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2mL。则该水样的COD为
);再用c2 mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2mL。则该水样的COD为
您最近一年使用:0次
【推荐3】按要求填空:
(1)还原铁粉与高温水蒸气反应的化学方程式:_____________________________________ ;
(2)除去Mg粉中的Al粉的试剂是__________ ,反应的离子方程式为:____________ ;
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
____ Fe(OH)3 +____ ClO-+____ OH- =__ FeO42-+___ Cl-+__ ( )
(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是________________ ;还原剂是_______________ ;当有11molP参加反应,转移的电子的物质的量为________ ;1molCuSO4能氧化的P原子的数目为_____________ 。
(1)还原铁粉与高温水蒸气反应的化学方程式:
(2)除去Mg粉中的Al粉的试剂是
(3)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
(4)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】I.根据硫及化合物相关性质回答以下问题:
(1)将 和
和 的混合气体通入
的混合气体通入 、
、 的混合溶液中反应回收
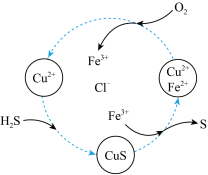
的混合溶液中反应回收 ,物质转化如图所示,下列说法不正确的是___________。
,物质转化如图所示,下列说法不正确的是___________。
(2)过量的锌与一定量㳖 反应,随着硫酸浓度变稀得到的两种气体产物为
反应,随着硫酸浓度变稀得到的两种气体产物为___________ 。使一定质量的Zn与 浓
浓 充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6L,则Zn的质量为
充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6L,则Zn的质量为___________ g。
Ⅱ.某小组用废铁屑和硝酸盐溶液模拟此过程如下。
(3)先用稀硫酸对废铁屑进行适当浸泡,其目的是___________ (用文字或者方程式表示)。
(4)将 溶液的
溶液的 调至2.5,从氧化还原的角度分析调低溶液pH的原因是
调至2.5,从氧化还原的角度分析调低溶液pH的原因是___________ 。已知:pH越小表示溶液中 越大。
越大。
(5)将上述处理过的足量铁屑投入(4)的溶液中。如图表示该反应过程中,体系内相关离子浓度、pH随时间变化的关系。
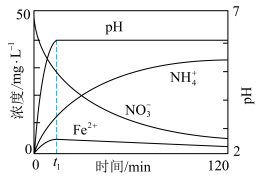
 前该反应的离子方程式是
前该反应的离子方程式是___________ 。
(1)将
 和
和 的混合气体通入
的混合气体通入 、
、 的混合溶液中反应回收
的混合溶液中反应回收 ,物质转化如图所示,下列说法不正确的是___________。
,物质转化如图所示,下列说法不正确的是___________。
A. 和 和 反应的离子方程式为: 反应的离子方程式为: |
B. 在转化过程中发生的反应为: 在转化过程中发生的反应为: |
C.整个反应过程中溶液的pH值变小(不考虑产生的 的稀释效果) 的稀释效果) |
D.提高混合气体中 的比例可防止生成的硫单质中混有 的比例可防止生成的硫单质中混有 |
 反应,随着硫酸浓度变稀得到的两种气体产物为
反应,随着硫酸浓度变稀得到的两种气体产物为 浓
浓 充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6L,则Zn的质量为
充分反应,Zn完全溶解,同时生成标准状况下的混合气体33.6L,则Zn的质量为Ⅱ.某小组用废铁屑和硝酸盐溶液模拟此过程如下。
(3)先用稀硫酸对废铁屑进行适当浸泡,其目的是
(4)将
 溶液的
溶液的 调至2.5,从氧化还原的角度分析调低溶液pH的原因是
调至2.5,从氧化还原的角度分析调低溶液pH的原因是 越大。
越大。(5)将上述处理过的足量铁屑投入(4)的溶液中。如图表示该反应过程中,体系内相关离子浓度、pH随时间变化的关系。

 前该反应的离子方程式是
前该反应的离子方程式是
您最近一年使用:0次
【推荐2】铜是重要的工业原料,现有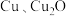 组成的混合物,某研究性学习小组为了探究其组成情况,取
组成的混合物,某研究性学习小组为了探究其组成情况,取 该混合物加入
该混合物加入 的稀硝酸中,固体物质完全反应,溶液中铜元素均为
的稀硝酸中,固体物质完全反应,溶液中铜元素均为 ,且生成
,且生成 (标准状况)的
(标准状况)的 。向所得溶液中加入
。向所得溶液中加入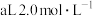 的
的 溶液,恰好使溶液中的
溶液,恰好使溶液中的 沉淀完全。
沉淀完全。
(1) 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为___________ ;
(2)
___________ L。
(3)求混合物中 的质量分数
的质量分数___________ ?(没有计算过程不得分)
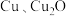 组成的混合物,某研究性学习小组为了探究其组成情况,取
组成的混合物,某研究性学习小组为了探究其组成情况,取 该混合物加入
该混合物加入 的稀硝酸中,固体物质完全反应,溶液中铜元素均为
的稀硝酸中,固体物质完全反应,溶液中铜元素均为 ,且生成
,且生成 (标准状况)的
(标准状况)的 。向所得溶液中加入
。向所得溶液中加入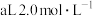 的
的 溶液,恰好使溶液中的
溶液,恰好使溶液中的 沉淀完全。
沉淀完全。(1)
 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为(2)

(3)求混合物中
 的质量分数
的质量分数
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】含氮化合物的处理对环境保护意义重大。研究氮及其化合物的性质,可以有效改善人类的生存环境。
(1)N原子的电子式为___________ 。
(2)用 或CO催化还原NO均能消除污染,反应的氧化产物为
或CO催化还原NO均能消除污染,反应的氧化产物为______ 。
(3)实验室常用NaOH溶液吸收 (NO和
(NO和 的混合气体),反应的化学方程式如下:
的混合气体),反应的化学方程式如下:
 ;
; (已知NO不能与NaOH溶液反应,不考虑
(已知NO不能与NaOH溶液反应,不考虑 与
与 的转化)。
的转化)。
①若 能被NaOH溶液完全吸收,则x的取值范围为
能被NaOH溶液完全吸收,则x的取值范围为______ 。
②若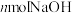 恰好完全反应,则被吸收的
恰好完全反应,则被吸收的 的体积为
的体积为______ L(标准状况)。
③将这两个反应中的产物进行分类,分类方法错误的是______ 。
A.强电解质和弱电解质 B.盐和氧化物
C.离子化合物和共价化合物 D.氧化产物和还原产物
(4)将32.64g铜与200mL一定浓度的硝酸反应,铜完全溶解,产生的NO和 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:
①NO的物质的量为___________ mol, 的体积为
的体积为___________ L(标准状况)。
②待产生的气体全部释放后,向溶液中加入 的NaOH溶液,恰好使溶液中的
的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为___________  。
。
(1)N原子的电子式为
(2)用
 或CO催化还原NO均能消除污染,反应的氧化产物为
或CO催化还原NO均能消除污染,反应的氧化产物为(3)实验室常用NaOH溶液吸收
 (NO和
(NO和 的混合气体),反应的化学方程式如下:
的混合气体),反应的化学方程式如下: ;
; (已知NO不能与NaOH溶液反应,不考虑
(已知NO不能与NaOH溶液反应,不考虑 与
与 的转化)。
的转化)。①若
 能被NaOH溶液完全吸收,则x的取值范围为
能被NaOH溶液完全吸收,则x的取值范围为②若
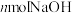 恰好完全反应,则被吸收的
恰好完全反应,则被吸收的 的体积为
的体积为③将这两个反应中的产物进行分类,分类方法错误的是
A.强电解质和弱电解质 B.盐和氧化物
C.离子化合物和共价化合物 D.氧化产物和还原产物
(4)将32.64g铜与200mL一定浓度的硝酸反应,铜完全溶解,产生的NO和
 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:①NO的物质的量为
 的体积为
的体积为②待产生的气体全部释放后,向溶液中加入
 的NaOH溶液,恰好使溶液中的
的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为 。
。
您最近一年使用:0次
【推荐1】硝酸是一种重要的化工原料,用来制取一系列硝酸盐类氮肥,如硝酸铵、硝酸钾等;也用来制取含硝基的炸药等。试回答下列问题:
(1)某同学对铁与稀硝酸的反应进行探究,若HNO3只被还原成NO,则:
①写出铁与过量稀硝酸反应的离子方程式:__ 。
②写出过量铁与稀硝酸反应的离子方程式:__ 。
③若28g铁与含1.6mol硝酸的稀硝酸恰好完全反应,则生成的Fe3+和Fe2+的物质的量之比为__ 。上述反应结束后,向反应后的溶液中加足量氢氧化钠溶液,滤出沉淀洗涤后,在空气中灼烧至质量不变,最终得到的固体质量为__ g。
(2)饮用水中NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO3-还原为N2。
①配平方程式:__ Al+__ NO3-+__ OH-+__ =__ [Al(OH)4]-+__ N2↑。
②上述反应中,还原剂与还原产物的物质的量之比是__ ,反应中转移电子0.3mol,生成__ mL(标准状况下)N2。
(1)某同学对铁与稀硝酸的反应进行探究,若HNO3只被还原成NO,则:
①写出铁与过量稀硝酸反应的离子方程式:
②写出过量铁与稀硝酸反应的离子方程式:
③若28g铁与含1.6mol硝酸的稀硝酸恰好完全反应,则生成的Fe3+和Fe2+的物质的量之比为
(2)饮用水中NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO3-还原为N2。
①配平方程式:
②上述反应中,还原剂与还原产物的物质的量之比是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】向含有0.8 mol的稀硝酸中慢慢加入22.4 g的铁粉,假设反应分为两个阶段。
第一阶段为:Fe+HNO3(稀)→Fe(NO3)3+NO↑+H2O
(1)写出这两个阶段发生反应的离子方程式:
第一阶段:_______________________________________________ 。
第二阶段:_______________________________________________ 。
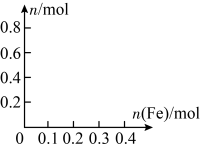
(2)在图中画出溶液中Fe2+、Fe3+、 的物质的量随加入铁粉的物质的量变化的关系图象(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量)
的物质的量随加入铁粉的物质的量变化的关系图象(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量) ________ 。
第一阶段为:Fe+HNO3(稀)→Fe(NO3)3+NO↑+H2O
(1)写出这两个阶段发生反应的离子方程式:
第一阶段:
第二阶段:
(2)在图中画出溶液中Fe2+、Fe3+、
 的物质的量随加入铁粉的物质的量变化的关系图象(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量)
的物质的量随加入铁粉的物质的量变化的关系图象(横坐标为加入铁粉的物质的量,纵坐标是溶液中离子的物质的量) 
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】回答下列问题
(1)金属与硝酸反应通常不能生成H2,用3mol/L HNO3与过量铁粉反应,HNO3的还原产物主要是NO,请写出反应的离子方程式:___________ 。
有同学在查阅文献时发现文献有记载:HNO3与铁反应能产生H2。于是其小组进行了金属铁与硝酸反应能否产生H2及其有利条件的探究。
实验I:20℃,将过量铁粉溶于0.5mol·L-1 HNO3中,立即有无色气体生成,充分反应后,溶液几乎无色。
(2)检验气体:方法如图所示。
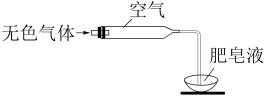
确认气体是H2,不含NO。实验证据是___________ 。
(3)检验溶液:取上层清液,等分两份
①向一份滴加K3[Fe(CN)6]溶液,___________ (填现象),说明含有Fe2+。
②向另一份加入NaOH溶液,产生灰绿色沉淀;加热至沸,有刺激性气味气体逸出,用湿润红色石蕊试纸检验,试纸变蓝。综合①、②,说明实验I中发生的反应有Fe+2H+=Fe2++H2↑,另外还有___________ (写出离子方程式)。
对H2产生的原因提出假设:在稀的酸性溶液中,HNO3中H+的氧化性大于NO ,验证如下:
,验证如下:
(4)实验II:将铜粉溶于0.5mol/L HNO3中。经检测,发现没有___________ 生成,初步证实假设不成立。
(5)再次查阅文献发现:在酸性介质中,尽管电极电势数据显示NO 离子是个颇强的氧化剂,然而动力学原因导致它在稀酸中的反应一般都很慢。于是小组改变条件重复实验I,向2mL 0.5mol·L-1 HNO3中加入过量铁粉,结果如下:
离子是个颇强的氧化剂,然而动力学原因导致它在稀酸中的反应一般都很慢。于是小组改变条件重复实验I,向2mL 0.5mol·L-1 HNO3中加入过量铁粉,结果如下:
经检验,实验III、IV、V中,NO 的还原产物与实验I相同。
的还原产物与实验I相同。
从反应速率的角度解释温度升高H2体积减少的原因___________ 。
(6)综上所述,有利于金属与硝酸反应生成氢气的条件是___________ 。
(1)金属与硝酸反应通常不能生成H2,用3mol/L HNO3与过量铁粉反应,HNO3的还原产物主要是NO,请写出反应的离子方程式:
有同学在查阅文献时发现文献有记载:HNO3与铁反应能产生H2。于是其小组进行了金属铁与硝酸反应能否产生H2及其有利条件的探究。
实验I:20℃,将过量铁粉溶于0.5mol·L-1 HNO3中,立即有无色气体生成,充分反应后,溶液几乎无色。
(2)检验气体:方法如图所示。

确认气体是H2,不含NO。实验证据是
(3)检验溶液:取上层清液,等分两份
①向一份滴加K3[Fe(CN)6]溶液,
②向另一份加入NaOH溶液,产生灰绿色沉淀;加热至沸,有刺激性气味气体逸出,用湿润红色石蕊试纸检验,试纸变蓝。综合①、②,说明实验I中发生的反应有Fe+2H+=Fe2++H2↑,另外还有
对H2产生的原因提出假设:在稀的酸性溶液中,HNO3中H+的氧化性大于NO
 ,验证如下:
,验证如下:(4)实验II:将铜粉溶于0.5mol/L HNO3中。经检测,发现没有
(5)再次查阅文献发现:在酸性介质中,尽管电极电势数据显示NO
 离子是个颇强的氧化剂,然而动力学原因导致它在稀酸中的反应一般都很慢。于是小组改变条件重复实验I,向2mL 0.5mol·L-1 HNO3中加入过量铁粉,结果如下:
离子是个颇强的氧化剂,然而动力学原因导致它在稀酸中的反应一般都很慢。于是小组改变条件重复实验I,向2mL 0.5mol·L-1 HNO3中加入过量铁粉,结果如下:| 实验序号 | Ⅲ | Ⅳ | Ⅴ |
| 温度 | 20℃ | 40℃ | 60℃ |
| 生成H2体积 | 6.0mL | 3.4mL | 2.6mL |
经检验,实验III、IV、V中,NO
 的还原产物与实验I相同。
的还原产物与实验I相同。从反应速率的角度解释温度升高H2体积减少的原因
(6)综上所述,有利于金属与硝酸反应生成氢气的条件是
您最近一年使用:0次



