今年春天以来,内蒙古自治区降水较常年偏少、气温偏高。进入7月以后,全区过半地域最高温度超过30℃以上,中西部地区有17个站点,最高温度超过35℃,阿拉善盟极高温度达到40℃。旱情牵动了全国人民的心。水是组成生命体的重要化学物质,有关水的反应有很多。
(1)水分子自身作用会生成阴、阳两种离子,其中阳离子的电子式是______________________ 。
(2)在由水电离产生的c(H+)=1×10-14molL-1的溶液中①NH4+、A13+、Br-、SO42-;②Na+、Mg2+、Cl-、NO3-;③K+、Ba2+、Cl-、NO3-;④K+、 Na+、HCO3-、SO42-四组离子中。一定可以大量共存的是______ (填序号,下同),可能大量共存的是_____________ 。
(3)在下列中,水既不作氧化剂又不作还原剂是_____________ (填序号)。
A.Cl2+H2O=HCl+HClO B.2Na2O2+2H2O==4NaOH+O2↑
C.CaH2+2H2O==Ca(OH)2+2H2↑ D.3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
(4)将钠、钾分别投入有少量相同质量的稀H2SO4中,反应结束后,两种溶液的质量仍相等而金属均无剩余,则投入的钠、钾的质量比为_____________ 。
(5)三氟化氮(NF3)是一种无色无味的气体,27.0mL NF3和水充分反应,生成18.0mLNO(同温、同压下),写出反应的化学方程式:_________________ 。
(1)水分子自身作用会生成阴、阳两种离子,其中阳离子的电子式是
(2)在由水电离产生的c(H+)=1×10-14molL-1的溶液中①NH4+、A13+、Br-、SO42-;②Na+、Mg2+、Cl-、NO3-;③K+、Ba2+、Cl-、NO3-;④K+、 Na+、HCO3-、SO42-四组离子中。一定可以大量共存的是
(3)在下列中,水既不作氧化剂又不作还原剂是
A.Cl2+H2O=HCl+HClO B.2Na2O2+2H2O==4NaOH+O2↑
C.CaH2+2H2O==Ca(OH)2+2H2↑ D.3Fe+4H2O
 Fe3O4+4H2
Fe3O4+4H2(4)将钠、钾分别投入有少量相同质量的稀H2SO4中,反应结束后,两种溶液的质量仍相等而金属均无剩余,则投入的钠、钾的质量比为
(5)三氟化氮(NF3)是一种无色无味的气体,27.0mL NF3和水充分反应,生成18.0mLNO(同温、同压下),写出反应的化学方程式:
17-18高三上·云南曲靖·阶段练习 查看更多[2]
更新时间:2017-11-14 14:53:16
|
相似题推荐
填空题
|
较难
(0.4)
解题方法
【推荐1】某无色透明滚液可能大量存在Ag+、Mg2+、Al3+、Cu2+、Fe3+中的几种:
(1)不做任何实验就可以肯定原溶液中不存在的离子是______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是_____ ;取上述反应中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有____ ;有关出现白色沉淀的离子方程式为______ 。
(3)往原无色透明溶液中加入足量Zn粉,析出的物质是_____ 。
(4)原溶液可能大量存在的阴离子是下列选项中的____
(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)往原无色透明溶液中加入足量Zn粉,析出的物质是
(4)原溶液可能大量存在的阴离子是下列选项中的
| A.Cl- | B.NO3- | C.CO32- | D.OH- |
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】按要求回答下列问题:
(1)某有色电解质溶液中,可能大量存在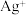 、
、 、
、 、
、 、
、 、
、 、
、 、
、 ,你认为一定含有的离子是
,你认为一定含有的离子是_______ (用离子符号表示,下同),一定没有的离子是_______ ,还需进一步确认的离子是_______ 。
(2)某溶液的溶质可能由下列离子组成: 、
、 、
、 、
、 、
、 、
、 ,某同学进行了如下实验:
,某同学进行了如下实验:
I.向溶液中加入过量的 溶液,有白色沉淀产生,过滤;
溶液,有白色沉淀产生,过滤;
II.向I中滤液中加入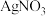 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;
III.将I中的沉淀加入足量稀盐酸中,沉淀消失,有气体产生。
依据以上实验可以推断,原溶液中一定含有_______ ;一定没有_______ ,检验可能存在的离子的试剂为_______ 。
(1)某有色电解质溶液中,可能大量存在
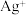 、
、 、
、 、
、 、
、 、
、 、
、 、
、 ,你认为一定含有的离子是
,你认为一定含有的离子是(2)某溶液的溶质可能由下列离子组成:
 、
、 、
、 、
、 、
、 、
、 ,某同学进行了如下实验:
,某同学进行了如下实验:I.向溶液中加入过量的
 溶液,有白色沉淀产生,过滤;
溶液,有白色沉淀产生,过滤;II.向I中滤液中加入
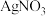 溶液,有白色沉淀产生;
溶液,有白色沉淀产生;III.将I中的沉淀加入足量稀盐酸中,沉淀消失,有气体产生。
依据以上实验可以推断,原溶液中一定含有
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】铝是地壳中含量最多的金属元素,其单质和化合物广泛应用于日常生活中。
(1)可以用电镀法在钢制品上电镀铝,为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应消耗2mol NaOH时,所得气体的物质的量为_______ mol。
(2)双羟基铝碳酸钠[NaAl(OH)2CO3]是一种常用的抗酸药,它与胃酸反应的化学方程式为_______ 。
(3)如图是从铝土矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并生产AlN的工艺流程:
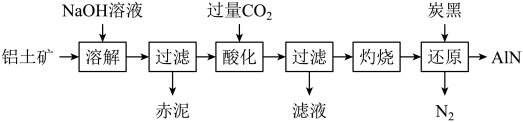
①“溶解”时,SiO2与NaOH溶液反应生成的硅酸钠与溶液中偏铝酸钠发生反应: ,“赤泥”的主要成分为
,“赤泥”的主要成分为_______ (写出化学式)。
②“酸化”时,通入过量CO2与NaAlO2反应,生成滤液的主要成分是_______ (写化学式)。
③“还原”时,炭黑在高温下被氧化为CO,反应的化学方程式为_______ 。
(4)1L某混合溶液,可能含有的离子如下表:
往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示。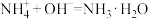
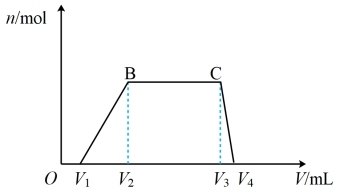
①该溶液中一定不含有的离子是_______ 。
②V1、V2、V3、V4之间的关系为_______ 。
(1)可以用电镀法在钢制品上电镀铝,为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应消耗2mol NaOH时,所得气体的物质的量为
(2)双羟基铝碳酸钠[NaAl(OH)2CO3]是一种常用的抗酸药,它与胃酸反应的化学方程式为
(3)如图是从铝土矿(主要成分为Al2O3,还含有少量SiO2、Fe2O3等杂质)中提取Al2O3并生产AlN的工艺流程:

①“溶解”时,SiO2与NaOH溶液反应生成的硅酸钠与溶液中偏铝酸钠发生反应:
 ,“赤泥”的主要成分为
,“赤泥”的主要成分为②“酸化”时,通入过量CO2与NaAlO2反应,生成滤液的主要成分是
③“还原”时,炭黑在高温下被氧化为CO,反应的化学方程式为
(4)1L某混合溶液,可能含有的离子如下表:
| 可能大量含有的阳离子 | H+、Mg2+、Al3+、 |
| 可能大量含有的阴离子 | Cl-、 |
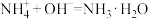

①该溶液中一定不含有的离子是
②V1、V2、V3、V4之间的关系为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】雄黄(AS4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
⑴As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,该反应的化学方程式为_______________ 。
⑵上述反应中的氧化剂是________ ,反应产生的气体可用_____ 吸收。
⑶As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3—=2H3AsO4+ 3S+10NO2↑+ 2H2O,若生成2mol H3AsO4,则反应中转移电子的物质的量为________ 。若将该反应设计成一原电池,则NO2应该在____ 极附近逸出。
⑷将⑶中反应产物NO2充满干燥的烧瓶,然后将烧瓶倒立于少水槽中,向烧瓶中通入一定量的氧气,气体恰好完全溶于水(假设溶液没有扩散),则烧瓶中溶液溶质的物质的量浓度为_______ (设该条件下的气体摩尔体积为23.8 ,结果保留到小数点后三位)。
,结果保留到小数点后三位)。
⑴As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,该反应的化学方程式为
⑵上述反应中的氧化剂是
⑶As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3—=2H3AsO4+ 3S+10NO2↑+ 2H2O,若生成2mol H3AsO4,则反应中转移电子的物质的量为
⑷将⑶中反应产物NO2充满干燥的烧瓶,然后将烧瓶倒立于少水槽中,向烧瓶中通入一定量的氧气,气体恰好完全溶于水(假设溶液没有扩散),则烧瓶中溶液溶质的物质的量浓度为
 ,结果保留到小数点后三位)。
,结果保留到小数点后三位)。
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】NH3和Cl2在常温下可快速反应生成氮气:2NH3+3Cl2 →N2+6HCl。当Cl2和 NH3 比例不同时,产物有差异。
(1)该反应可用于检验化工生产中氯气是否泄漏。如氯气有少量泄漏,用氨气检验时的现象为_____________________________ 。
(2)若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,Cl2和NH3的最佳比例为_____ 。
(3)常温常压下,取总物质的量为12mol的氯气和氨气的混合气体,完全反应后,气体物质的量保持不变。求:① 反应前氯气和氨气的物质的量之比______________
② 反应后生成的氧化产物的质量_______________ 。
(4)若将总体积为100L的NH3和Cl2混合,实验精确测得充分反应后无色混合气体中N2占混合气体的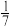 ,求生成氧化产物的物质的量
,求生成氧化产物的物质的量_____________ 。(该实验数据在标准状况下测定)
(1)该反应可用于检验化工生产中氯气是否泄漏。如氯气有少量泄漏,用氨气检验时的现象为
(2)若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,Cl2和NH3的最佳比例为
(3)常温常压下,取总物质的量为12mol的氯气和氨气的混合气体,完全反应后,气体物质的量保持不变。求:① 反应前氯气和氨气的物质的量之比
② 反应后生成的氧化产物的质量
(4)若将总体积为100L的NH3和Cl2混合,实验精确测得充分反应后无色混合气体中N2占混合气体的
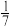 ,求生成氧化产物的物质的量
,求生成氧化产物的物质的量
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】硫酸工业生产应考虑综合经济效益问题。
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在___________ 的郊区(填选项的标号)
a. 有丰富黄铁矿资源的城市 b. 风光秀丽的旅游城市
c. 消耗硫酸甚多的工业城市 d. 人口稠密的文化、商业中心城市
(2)据测算,接触法制硫酸过程中,若反应热都未被利用,则每生产1t 98%硫酸需消耗3.6×105kJ能量。请通过计算判断,若反应:SO2(g)+1/2O2(g) ⇌SO3(g);△H=-98.3kJ·mol-1;放出的热量能在生产过程中得到充分利用,则每生产1t98%硫酸只需外界提供(或可向外界输出)__________ 千焦能量;
(3)CuFeS2是黄铁矿的另一成分,煅烧时,CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为____________________ 。
(4)由硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3在沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)
已知CuSO4在低于660℃时不会分解,请简要分析上表中CuSO4的质量分数随温度升高而降低的原因________________________________________ 。
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在
a. 有丰富黄铁矿资源的城市 b. 风光秀丽的旅游城市
c. 消耗硫酸甚多的工业城市 d. 人口稠密的文化、商业中心城市
(2)据测算,接触法制硫酸过程中,若反应热都未被利用,则每生产1t 98%硫酸需消耗3.6×105kJ能量。请通过计算判断,若反应:SO2(g)+1/2O2(g) ⇌SO3(g);△H=-98.3kJ·mol-1;放出的热量能在生产过程中得到充分利用,则每生产1t98%硫酸只需外界提供(或可向外界输出)
(3)CuFeS2是黄铁矿的另一成分,煅烧时,CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为
(4)由硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3在沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)
| 沸腾炉温度/℃ | 600 | 620 | 640 | 660 |
| 矿渣中CuSO4的质量分数/% | 9.3 | 9.2 | 9.0 | 8.4 |
已知CuSO4在低于660℃时不会分解,请简要分析上表中CuSO4的质量分数随温度升高而降低的原因
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】根据要求回答下列问题:
(1)氯气与氢氧化钠在70℃时反应,生成物中 和NaClO的物质的量之比为3:1的离子方程式为
和NaClO的物质的量之比为3:1的离子方程式为_______ 。
(2) 与
与 按照1:1反应的离子方程式为
按照1:1反应的离子方程式为_______ 。
(3) 及
及 均可将溶液中的Ag+还原为银,从而可用于化学镀银。
均可将溶液中的Ag+还原为银,从而可用于化学镀银。
① 中,P元素的化合价为
中,P元素的化合价为_______ 。
②利用 进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为
进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为_______ (填化学式)。
(4)取300mL0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是_______ mol。
(5)在 溶液中加入
溶液中加入 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是
溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是_______ ,又变为棕黄色的原因是_______ (用离子方程式解释)。
(1)氯气与氢氧化钠在70℃时反应,生成物中
 和NaClO的物质的量之比为3:1的离子方程式为
和NaClO的物质的量之比为3:1的离子方程式为(2)
 与
与 按照1:1反应的离子方程式为
按照1:1反应的离子方程式为(3)
 及
及 均可将溶液中的Ag+还原为银,从而可用于化学镀银。
均可将溶液中的Ag+还原为银,从而可用于化学镀银。①
 中,P元素的化合价为
中,P元素的化合价为②利用
 进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为
进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为(4)取300mL0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是
(5)在
 溶液中加入
溶液中加入 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是
溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】某强酸性溶液X含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行实验,实验内容如下:
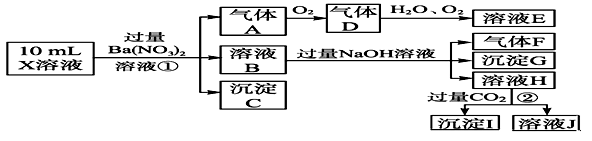
根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是______________________________ ;
(2)写出有关离子方程式:
步骤①中生成A__________________ ;步骤②生成沉淀I__________________ 。
(3)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H+)=0.04 mol,若沉淀C物质的量大于0.07 mol,溶液X中还一定含有的离子是______ ;若而沉淀C物质的量小于0.07 mol,溶液X中还一定含有的离子是______ 。

根据以上信息,回答下列问题:
(1)溶液X中除H+外还肯定含有的离子是
(2)写出有关离子方程式:
步骤①中生成A
(3)假设测定A、F、I均为0.01 mol,10 mL X溶液中n(H+)=0.04 mol,若沉淀C物质的量大于0.07 mol,溶液X中还一定含有的离子是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】铜及其化合物在生产生活有广泛应用,铜在化合物中的常见化合价有+1、+2.已知 与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
(1)工业上可用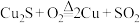 反应制取粗铜,该反应中
反应制取粗铜,该反应中___________ 元素被还原。不考虑杂质的反应,理论上生成1mol的 电子转移的数目为
电子转移的数目为___________
(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为___________ 。温度控制在50~60℃的原因除了加快反应速率外,还有___________ 。在 溶液中加入一定量的
溶液中加入一定量的 和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:
和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:___________ 。
(3)现向Cu、 和CuO组成的混合物中,加入2L 0.6
和CuO组成的混合物中,加入2L 0.6
 溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。
溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。 跟稀硝酸反应的离子方程式为
跟稀硝酸反应的离子方程式为___________ 。若将上述混合物用足量的 加热还原,所得到固体的质量为
加热还原,所得到固体的质量为___________ g。若上述混合物中含0.2mol Cu,将该混合物与稀硫酸充分反应,消耗 的物质的量为
的物质的量为___________ mol。
 与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。
与稀硫酸反应,溶液呈蓝色并有紫红色固体析出。(1)工业上可用
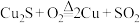 反应制取粗铜,该反应中
反应制取粗铜,该反应中 电子转移的数目为
电子转移的数目为(2)将少量铜丝放入适量的稀硫酸中,温度控制在50℃,加入
 溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为
溶液,一段时间后,升温到60℃,再反应一段时间后可制得硫酸铜,该反应的离子方程式为 溶液中加入一定量的
溶液中加入一定量的 和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:
和NaCl溶液,加热,生成CuCl沉淀,写出生成CuCl的离子方程式:(3)现向Cu、
 和CuO组成的混合物中,加入2L 0.6
和CuO组成的混合物中,加入2L 0.6
 溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。
溶液恰好使混合物溶解,同时收集到4480mL NO气体(标准状况)。 跟稀硝酸反应的离子方程式为
跟稀硝酸反应的离子方程式为 加热还原,所得到固体的质量为
加热还原,所得到固体的质量为 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】实验表明,液态时,纯硫酸的电离能力强于硝酸,纯硫酸的导电性也显著强于纯水。已知液态纯酸都能像水那样进行自身电离H2O+H2O H3O++OH-而建立平衡,且在一定温度下都有各自的离子积常数,据此回答:
H3O++OH-而建立平衡,且在一定温度下都有各自的离子积常数,据此回答:
(1)纯硫酸在液态时自身电离的方程式是_______ ,纯硝酸的离子积常数表达式为_______ 。
(2)在25℃时,液态纯H2SO4的离子积常数K(H2SO4)_______ 1×10-14(填“大于”、“小于”或“等于”)。
(3)在纯硫酸和纯硝酸的液态混合酸中,存在的阴离子主要是_______ ,这是因为混合酸中不仅存在硫酸和硝酸各自电离的两个电离平衡,而且还因硫酸的酸性大于硝酸,又在无水条件下,混酸中必然发生(写离子方程式)_______ 反应而造成的。
 H3O++OH-而建立平衡,且在一定温度下都有各自的离子积常数,据此回答:
H3O++OH-而建立平衡,且在一定温度下都有各自的离子积常数,据此回答:(1)纯硫酸在液态时自身电离的方程式是
(2)在25℃时,液态纯H2SO4的离子积常数K(H2SO4)
(3)在纯硫酸和纯硝酸的液态混合酸中,存在的阴离子主要是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】水是极弱的电解质,其中存在电离平衡H2O⇌H++OH-,回答下列问题:
(1)常温下,某电解质溶解在水中后,溶液中水电离的c(H+)=1×10-9,则该电解质可能是_______ (填序号)。
A.CuSO4 B.HCl C.Na2S D.NaOH E.K2SO4
(2)常温时,取0.1mol·L-1 HX溶液与0.1mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH=8。
①混合溶液中由水电离出的c(OH-)与0.1mol/LNaOH溶液中由水电离出的c(OH-)之比为_______ 。
②已知NH4X溶液呈中性,将HX溶液加入到Na2CO3溶液中有气体放出。试推断NH4HCO3溶液的pH_______ 7(填“>”“<”或“=”)。
(3)T℃时,测得0.01mol·L-1 NaOH溶液的pH=10,则此温度下水的Kw=_______ 。在此温度下,将0.01mol·L-1 H2SO4溶液VaL与pH=12的NaOH溶液VbL混合,若所得混合液pH=11,则Va∶Vb=_______ (忽略溶液混合时体积的变化)。
(1)常温下,某电解质溶解在水中后,溶液中水电离的c(H+)=1×10-9,则该电解质可能是
A.CuSO4 B.HCl C.Na2S D.NaOH E.K2SO4
(2)常温时,取0.1mol·L-1 HX溶液与0.1mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH=8。
①混合溶液中由水电离出的c(OH-)与0.1mol/LNaOH溶液中由水电离出的c(OH-)之比为
②已知NH4X溶液呈中性,将HX溶液加入到Na2CO3溶液中有气体放出。试推断NH4HCO3溶液的pH
(3)T℃时,测得0.01mol·L-1 NaOH溶液的pH=10,则此温度下水的Kw=
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】Ⅰ.现有NH4Cl和氨水组成的混合溶液。请回答下列问题(填“>”、“<”或“=”):
(1)若溶液的pH=7,则该溶液中c(NH4+)________ c(Cl-)。
(2)若溶液中pH>7,则该溶液中c(NH4+)________ c(Cl-)。
Ⅱ.常温下有浓度均为0.1mol•L-1的三种溶液:①Na2CO3、②NaHCO3、③HCl
(1)溶液②中按物质的量浓度由大到小顺序排列该溶液中各离子浓度__________________ ;
(2)溶液②中,c(CO32-)+c(HCO3-)+c(H2CO3)=__________ mol•L-1;
(3)将10mL溶液③加水稀释至100mL,则此时溶液中由水电离出的c( H+)=_____ mol•L-1。
(1)若溶液的pH=7,则该溶液中c(NH4+)
(2)若溶液中pH>7,则该溶液中c(NH4+)
Ⅱ.常温下有浓度均为0.1mol•L-1的三种溶液:①Na2CO3、②NaHCO3、③HCl
(1)溶液②中按物质的量浓度由大到小顺序排列该溶液中各离子浓度
(2)溶液②中,c(CO32-)+c(HCO3-)+c(H2CO3)=
(3)将10mL溶液③加水稀释至100mL,则此时溶液中由水电离出的c( H+)=
您最近一年使用:0次



