名校
1 . 利用如下流程可从废光盘中回收金属层中的银(金属层中其他金属含量过低,对实验影响可忽略):
已知: 溶液在加热时易分解生成
溶液在加热时易分解生成 和
和 。下列说法不正确的是
。下列说法不正确的是
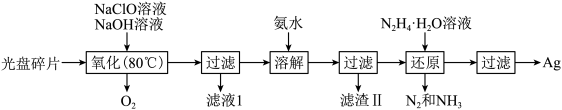
已知:
 溶液在加热时易分解生成
溶液在加热时易分解生成 和
和 。下列说法不正确的是
。下列说法不正确的是
| A.若省略第一次过滤,会使氨水的用量增加 |
B.若“还原”工序利用原电池来实现,则 是正极产物 是正极产物 |
C.“还原”时,每生成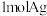 ,理论上消耗 ,理论上消耗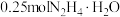 |
D.“溶解”工序发生的反应: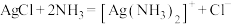 |
您最近一年使用:0次
2 . 已知 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.反应中每生成  ,转移的电子数为 ,转移的电子数为 |
B.常温常压下,  中含有的原子数为 中含有的原子数为 |
C.常温下, 的硫酸溶液中含有的 的硫酸溶液中含有的 数为 数为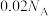 |
D.标准状况下,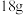  中含有的共价键数为 中含有的共价键数为 |
您最近一年使用:0次
真题
名校
3 . 我国古代四大发明之一黑火药的爆炸反应为: 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 含 含 键数目为 键数目为 | B.每生成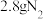 转移电子数目为 转移电子数目为 |
C.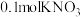 晶体中含离子数目为 晶体中含离子数目为 | D.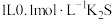 溶液中含 溶液中含 数目为 数目为 |
您最近一年使用:0次
2023-06-13更新
|
12047次组卷
|
25卷引用:内蒙古呼和浩特市剑桥中学2023-2024学年高二下学期3月月考化学试题
内蒙古呼和浩特市剑桥中学2023-2024学年高二下学期3月月考化学试题江西省清江中学2022-2023学年高二下学期期末考试化学试题湖北省恩施一中、建始一中、咸丰一中三校2023-2024学年高二上学期9月联考化学试题湖南省 邵阳市第二中学2023-2024学年高二上学期1月期末化学试题2023年高考辽宁卷化学真题(已下线)T5-阿伏伽德罗常数(已下线)2023年高考化学真题完全解读(辽宁卷)(已下线)专题03 阿伏伽德罗常数的应用(已下线)专题03 阿伏伽德罗常数的应用(已下线)专题03 阿伏伽德罗常数的应用(已下线)第3讲 氧化还原反应(已下线)考点06 物质的量 气体摩尔体积(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点02 物质的量 气体摩尔体积(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第8讲 物质的量与气体摩尔体积(已下线)专题03 化学计量-2023年高考化学真题题源解密(全国通用)(已下线)专题03 阿伏加德罗常数与化学计算 -2023年高考化学真题题源解密(新高考专用)吉林省长春外国语学校2023-2024学年高三上学期开学考试化学试题福建省宁德第一中学2024届高三上学期第一次检测化学试题(已下线)题型01 物质的组成与分类 传统文化 化学用语-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)题型02 阿伏加德罗常数的判断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)甘肃省白银市会宁县第四中学2023-2024学年高三上学期第三次月考化学试题湖南省长沙市弘益高级中学2023-2024学年高三上学期第四次月考化学试卷山东省菏泽市郓城县第一中学(英华校区)2023-2024学年高三上学期10月阶段性考试化学试题福建省福州第三中学2023-2024学年高三下学期第十六次检测(三模)化学试题测试辽宁化学 请勿下载
名校
解题方法
4 . 科学研究人员最近发现了一种“水”电池,在海水中电池总反应可表示为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列有关说法正确的是
| A.正极反应式:Ag - e- + Cl- = AgCl |
| B.AgCl是还原产物 |
| C.生成1 mol Na2Mn5O10转移2 mol电子 |
| D.Na+不断向“水”电池的负极移动 |
您最近一年使用:0次
2023-04-26更新
|
132次组卷
|
94卷引用:2016-2017学年内蒙古鄂尔多斯一中高二上期中化学卷
2016-2017学年内蒙古鄂尔多斯一中高二上期中化学卷(已下线)2011-2012学年江西省白鹭洲中学高二上学期期中考试化学(理)试卷(已下线)2011-2012学年福建师大附中高二上学期期末考试化学试卷(已下线)2011-2012学年浙江省温州中学高二下学期期中考试化学试卷(已下线)2011-2012学年浙江东阳中学、兰溪一中高二下学期期中考试化学卷(已下线)2013-2014云南省玉溪一中高二下学期第二次月考化学试卷(已下线)2013-2014湖北省荆州中学高二上学期期末考试化学试卷2014-2015重庆市重庆一中高二上学期期中化学(理)试卷2014-2015山东省临沭二中高二1月月考化学试卷2014-2015山西省原平市一中高二上学期期末考试化学试卷2016-2017学年湖南省娄底市双峰一中等五校高二上期中化学卷浙江省名校协作体2016-2017学年高二下学期考试化学试题河北省鸡泽县第一中学2017-2018学年高二上学期第一次月考化学试题陕西省西安市长安区第一中学2017-2018学年高二上学期第二次月考化学试题北京师范大学附属中学2017-2018学年高二上学期期末考试化学试题【全国校级联考】浙江省宁波市六校2017-2018学年高二下学期期末联考化学试题安徽省宣城市郎溪县郎溪中学2018-2019学年高二上学期返校考化学试题福建省莆田市第八中学2018-2019学年高二(理)上学期期中考试化学试题【校级联考】江西省赣州市南康中学、于都中学2018-2019学年高二上学期第三次月考化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二上学期期末考试化学试题湖南省邵东县第一中学、娄底三中2019-2020学年高二上学期第一次月考化学试题湖南省长沙市长沙县第九中学2018-2019学年高二下学期期末考试化学试题云南省武定民族中学2019-2020学年高二上学期期末考试化学试题辽宁省六校协作体2020-2021学年高二上学期期初考试化学试题(已下线)第01章 化学反应与能量转化(B卷能力提升篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)山东省滕州市第一中2020-2021学年高二上学期10月月考化学试题广东省珠海市第二中学2019-2020学年高二上学期期中考试化学试题鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第2节 化学能转化为电能——电池 课时2 化学电源福建省莆田第十五中学2018-2019学年高二上学期期中考试化学试题山西省运城市临猗县临晋中学2020-2021学年高二上学期12月月考化学试题福建省莆田第十五中学2019-2020学年高二上学期期中考试化学试题吉林省前郭尔罗斯蒙古族自治县蒙古族中学2020-2021学年高二上学期期末考试化学试题江西省吉安市吉安县第三中学、安福二中2021-2022学年高二入学考试化学试题安徽省淮北市第一中学 2021-2022学年高二上学期第一次月考化学试题北京市石景山区第九中学2021-2022学年高二上学期期中考试化学试题山东省实验中学2022-2023学年高二上学期10月月考化学试题山东省威海大光华学校2023-2024学年高二11月月考化学试题(已下线)2012届四川省成都外国语学校高三上学期8月月考化学试卷(已下线)2012届山东省枣庄十八中高三10月份质量检测化学试卷(已下线)2014高考名师推荐化学原电池的工作原理、电极反应式的书写2014-2015江西省白鹭洲中学高一下学期期中考试化学试卷2014-2015学年山西省孝义市高一下学期升级考试化学试卷2016届河北省唐山市迁安二中高三上学期期末化学试卷2015-2016学年北大附中河南分校高一下3月月考化学试卷2015-2016学年浙江省绍兴一中高一下期中化学试卷2015-2016学年河北省石家庄市辛集中学高一下期中理科化学试卷2015-2016学年中国石油天然气管道局中学高一下第二次月考化学试卷2015-2016学年甘肃省天水一中高一下期末理科化学试卷2015-2016学年山东省烟台市招远二中高一下3月月考化学试卷2017届四川省广元市苍溪县高三零诊理综化学试卷2017届四川省双流中学高三12月月考化学卷2016-2017学年湖北省重点高中联考协作体高一下学期期中考试化学试卷河北省定州中学2017届高三下学期第二次月考(4月)化学试题2【全国百强校】河北省定州中学2017届高三下学期第二次月考(4月)化学试题天津市南开区2017届高三高考二模化学试卷山西省怀仁县第一中学2016-2017学年高一下学期第三次(5月)月考化学试题江西省南昌市八一中学、洪都中学、麻丘中学等六校2016-2017学年高一5月联考化学试题湖北省沙市中学、恩施高中、郧阳中学2016-2017学年高一下学期阶段性联考化学试题甘肃省天水市第一中学2016-2017学年高一下学期第二次月考(B卷)化学试题湖南省衡阳市第八中学2016-2017学年高一下学期五科联赛(6月)理综化学试题浙江省金华市东阳中学2016-2017学年高一6月月考化学试题浙江省东阳中学2016-2017学年高一5月月考化学试题浙江省2018版考前特训(2017年10月)学考70快练:原电池福建省晋江市季延中学2018届高三上学期第二阶段检测化学试题【全国百强校】北京师范大学附属中学2017-2018学年高一下学期期中考试化学试题(已下线)考点09 原电池原理及其应用——备战2019年浙江新高考化学考点【全国百强校】湖南省衡阳市衡阳县第一中学2018-2019学年高一下学期第一次月考化学试题【全国百强校】广西壮族自治区桂林市第十八中学2018-2019学年高一下学期期中段考化学试题【全国百强校】江西省新余市第一中学2018-2019学年高一下学期第二次(5月)段考化学试题【校级联考】浙江省台州市联谊五校2018-2019学年高一下学期期中考试化学试题黑龙江省大庆十中2018-2019学年高一下学期第二次月考化学试题甘肃省玉门一中2018-2019学年高一下学期期末考试化学试题福建省福州市长乐高级中学2020届高三上学期第一次月考化学试题山东省济宁市鱼台县第一中学2020届高三10月月考化学试题(已下线)【新东方】高中化学5029浙江省宁波诺丁汉大学附属中学2018-2019学年高一下学期期中考试(实验班)化学试题2020春(新教材)人教化学第二册第6章 化学反应与能量练习课时2 发展中的化学电源——A学习区 夯实基础(人教版必修2)课时3 化学电源——A学习区 夯实基础(鲁科版(2019)第二册)安徽省滁州市明光市明光中学2019-2020高一下学期第二次月考化学试题安徽省淮北市第一中学2019-2020学年高一下学期期中考试化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第四次综合测试化学试题吉林省白城市洮南市第一中学2019-2020学年高一下学期第三次月考化学试题吉林省长春外国语学校2019-2020学年高一下学期期末考试化学(理)试题河南省鹤壁市外国语中学2019-2020学年高一下学期段考化学试题(已下线)专题讲座(六)新型电源及电极反应式的书写(精练)-2021年高考化学一轮复习讲练测黑龙江宾县第一中学2021届高三上学期第二次月考化学试题云南省玉溪市2020-2021学年高一下学期期末教学质量检测化学试题浙江省磐安县第二中学2019-2020学年高一下学期返校考试化学试题河北省定州中学2017届高三下学期第二次月考(4月)化学试题1(已下线)第06讲 化学电源-【寒假自学课】2022年高一化学寒假精品课(苏教版必修第二册)北京市第一七一中学2021-2022学年高一下学期期中考试化学试题北京市汇文中学2021-2022学年高一下学期期中考试化学试题北京市丰台区2022-2023学年高一下学期期中练习化学试题
5 . 中国科学家研究在Pd/SVG催化剂上H2还原NO生成N2和NH3的路径,各基元反应及活化能Ea(kJ/mol)如图所示,下列说法错误的是
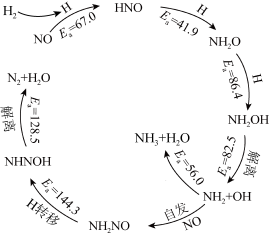

| A.生成NH3的各基元反应中,N元素均被还原 |
B.生成NH3的总反应方程式为5H2+2NO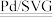 2H2O+2NH3 2H2O+2NH3 |
| C.决定NO生成NH3速率的基元反应为NH2O+H→NH2OH |
| D.在Pd/SVG催化剂上,NO更容易被H2还原为N2 |
您最近一年使用:0次
2023-01-16更新
|
450次组卷
|
9卷引用:内蒙古赤峰二中2022-2023学年高二上学期期末考试化学试题
解题方法
6 . 某研究性学习小组拟用如下装置设计实验,来探究纯净、干燥的氯气与氨气的反应。按要求回答下列问题:

(1)装置A中盛装浓盐酸的仪器名称是_______ ;装置D的作用是_______ ;装置E中饱和食盐水的作用是_______ ;
(2)导气管的正确连接顺序中,a与_______ 连接(填小写字母);
(3)装置F中发生8NH3+3Cl2=6NH4Cl+N2,该反应中氧化剂与还原剂的物质的量之比是_______ ,为使两种气体充分接触,明显地看到_______ 现象,则装置F中j与_______ 连接(填小写字母);
(4)装置B中所发生反应的化学方程式是_______ ;
(5)该学习小组研究发现,整套实验方案的主要缺陷是缺少_______ 装置。

(1)装置A中盛装浓盐酸的仪器名称是
(2)导气管的正确连接顺序中,a与
(3)装置F中发生8NH3+3Cl2=6NH4Cl+N2,该反应中氧化剂与还原剂的物质的量之比是
(4)装置B中所发生反应的化学方程式是
(5)该学习小组研究发现,整套实验方案的主要缺陷是缺少
您最近一年使用:0次
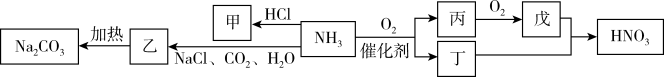
7 .  是一种重要的化工原料,可发生如下转化。下列有关表述正确的是
是一种重要的化工原料,可发生如下转化。下列有关表述正确的是
 是一种重要的化工原料,可发生如下转化。下列有关表述正确的是
是一种重要的化工原料,可发生如下转化。下列有关表述正确的是
| A.甲中含有离子键、极性共价键和氢键 |
| B.戊与丁反应时,氧化剂与还原剂的物质的量之比为2∶1 |
| C.浓硝酸见光易分解且易挥发,应用棕色试剂瓶盛放 |
D.向饱和 溶液中依次通入过量的 溶液中依次通入过量的 和 和 ,然后过滤可制得乙 ,然后过滤可制得乙 |
您最近一年使用:0次
8 . 铜、铁、铝是重要的金属材料,铜、铁、铝及其化合物有非常重要的用途。
(1)铁元素与氯元素可形成 和
和 两种化合物,下列说法正确的是
两种化合物,下列说法正确的是_______ (填序号)
①保存 溶液时,需向溶液中加入少量Fe
溶液时,需向溶液中加入少量Fe
② 只能通过置换反应生成,
只能通过置换反应生成, 只能通过化合反应生成
只能通过化合反应生成
③铜片、碳棒和 溶液组成原电池,电子由铜片沿导线流向碳棒
溶液组成原电池,电子由铜片沿导线流向碳棒
④制备 、
、 、
、 均能采用将溶液直接蒸干的方法
均能采用将溶液直接蒸干的方法
⑤含 的溶液和含
的溶液和含 的溶液,无论正滴和反滴,生成
的溶液,无论正滴和反滴,生成 的质量相等
的质量相等
(2)高铁酸钾( )是一种高效多功能水处理剂。
)是一种高效多功能水处理剂。 可以铁为电极,通过电解浓的KOH溶液来制取,写出电解法制取
可以铁为电极,通过电解浓的KOH溶液来制取,写出电解法制取 的阳极反应式:
的阳极反应式:_______ ;
(3)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为 ,有
,有 参加反应,转移
参加反应,转移_______ mol电子;
(4)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为_______ ;从腐蚀废液回收得到金属铜,还需要的试剂是_______ ;
(5)工业上常用铝土矿(含 等杂质)生产铝。从
等杂质)生产铝。从 和
和 混合溶液中制得
混合溶液中制得 ,需要从下列试剂中选择两种,选用的试剂组合最好是
,需要从下列试剂中选择两种,选用的试剂组合最好是_______ ;
a.NaOH溶液 b.氨水 c. d.盐酸
d.盐酸
(6)已知25℃时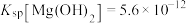 ,
,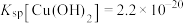 ,
,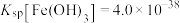 ,
,
①在25℃下,向浓度均为 的
的 和
和 混合溶液中逐滴加入氨水,先生成
混合溶液中逐滴加入氨水,先生成_______ 沉淀(填化学式);
②用 、
、 的混合溶液(A)与过量氨水(B)反应,为使
的混合溶液(A)与过量氨水(B)反应,为使 、
、 同时生成沉淀,应先向沉淀反应器中加入
同时生成沉淀,应先向沉淀反应器中加入_______ (填“A”或“B”),再滴加另一反应物;
③溶液中某离子物质的量浓度低于 时,可认为已沉淀完全。现向一定浓度的
时,可认为已沉淀完全。现向一定浓度的 和
和 的混合溶液中逐滴加入氨水,当
的混合溶液中逐滴加入氨水,当 完全沉淀时,测定
完全沉淀时,测定 。此时所得沉淀中
。此时所得沉淀中_______  (填“还含有”或“不含有”)。
(填“还含有”或“不含有”)。
(1)铁元素与氯元素可形成
 和
和 两种化合物,下列说法正确的是
两种化合物,下列说法正确的是①保存
 溶液时,需向溶液中加入少量Fe
溶液时,需向溶液中加入少量Fe②
 只能通过置换反应生成,
只能通过置换反应生成, 只能通过化合反应生成
只能通过化合反应生成③铜片、碳棒和
 溶液组成原电池,电子由铜片沿导线流向碳棒
溶液组成原电池,电子由铜片沿导线流向碳棒④制备
 、
、 、
、 均能采用将溶液直接蒸干的方法
均能采用将溶液直接蒸干的方法⑤含
 的溶液和含
的溶液和含 的溶液,无论正滴和反滴,生成
的溶液,无论正滴和反滴,生成 的质量相等
的质量相等(2)高铁酸钾(
 )是一种高效多功能水处理剂。
)是一种高效多功能水处理剂。 可以铁为电极,通过电解浓的KOH溶液来制取,写出电解法制取
可以铁为电极,通过电解浓的KOH溶液来制取,写出电解法制取 的阳极反应式:
的阳极反应式:(3)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料。其中一个反应为
 ,有
,有 参加反应,转移
参加反应,转移(4)氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为
(5)工业上常用铝土矿(含
 等杂质)生产铝。从
等杂质)生产铝。从 和
和 混合溶液中制得
混合溶液中制得 ,需要从下列试剂中选择两种,选用的试剂组合最好是
,需要从下列试剂中选择两种,选用的试剂组合最好是a.NaOH溶液 b.氨水 c.
 d.盐酸
d.盐酸(6)已知25℃时
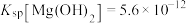 ,
,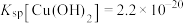 ,
,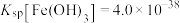 ,
,
①在25℃下,向浓度均为
 的
的 和
和 混合溶液中逐滴加入氨水,先生成
混合溶液中逐滴加入氨水,先生成②用
 、
、 的混合溶液(A)与过量氨水(B)反应,为使
的混合溶液(A)与过量氨水(B)反应,为使 、
、 同时生成沉淀,应先向沉淀反应器中加入
同时生成沉淀,应先向沉淀反应器中加入③溶液中某离子物质的量浓度低于
 时,可认为已沉淀完全。现向一定浓度的
时,可认为已沉淀完全。现向一定浓度的 和
和 的混合溶液中逐滴加入氨水,当
的混合溶液中逐滴加入氨水,当 完全沉淀时,测定
完全沉淀时,测定 。此时所得沉淀中
。此时所得沉淀中 (填“还含有”或“不含有”)。
(填“还含有”或“不含有”)。
您最近一年使用:0次
名校
解题方法
9 . 新型陶瓷AlN可通过反应: 合成。下列叙述正确的是
合成。下列叙述正确的是
 合成。下列叙述正确的是
合成。下列叙述正确的是| A.上述反应中,N2是还原剂,Al2O3是氧化剂 |
| B.AlN中氮元素的化合价为+3 |
| C.上述反应中,每生成1molAlN需转移3mol电子 |
| D.AlN的摩尔质量为41g |
您最近一年使用:0次
2021-04-12更新
|
520次组卷
|
61卷引用:内蒙古包头市包钢第四中学2018-2019学年高二下学期期末考试化学试题
内蒙古包头市包钢第四中学2018-2019学年高二下学期期末考试化学试题(已下线)2012年人教版高中化学选修1 3.3玻璃、陶瓷和水泥练习卷(已下线)2013-2014学年上海市吴淞中学高二上学期期中考试化学试卷吉林省松原市乾安七中2020-2021学年高二下学期第七次质量检测化学试题浙江省湖州市长兴县等三县2017-2018学年高二上学期期中考试化学试题(已下线)2010年宁夏银川一中高一上学期期中考试化学卷(已下线)2010年重庆市万州二中高一12月月考化学试卷(已下线)2010—2011年福建省厦门市杏南中学高一12月月考化学卷(已下线)2012届河北省定州二中高三第一次月考化学试卷(已下线)2011-2012学年浙江省余姚中学高一上学期期中化学(理)试卷(化学实验班)(已下线)2011-2012学年浙江省瑞安中学高一上学期期中考试化学试卷(已下线)2011-2012年江西赣州市十一县(市)高一下学期期中联考化学试卷(已下线)2012-2013学年浙江省舟山二中等三校高一上学期期末联考化学试卷(已下线)2015届北京市东城区普通校高三11月联考化学试卷2014-2015浙江省严州中学高一1月月考化学试卷2017届山东省实验中学高三第一次诊断性考试化学试卷2017届山西大学附中高三上10月模块诊断化学试卷2016-2017学年安徽省亳州市涡阳县第一中学高一3月月考化学试卷江西省上饶市上饶中学2019届高三上学期开学(实验、重点、特长班)检测化学试题【全国百强校】陕西省西安市第一中学2019届高三上学期第一次月考化学试题云南省丘北县第二中学2018-2019学年高一上学期10月月考化学试题新疆自治区北京大学附属中学新疆分校2019届高三上学期10月月考化学试题辽宁省大连市第103中学2017-2018学年高一上学期期中考试化学试题【校级联考】湖南省醴陵二中、醴陵四中2018-2019学年高一上学期期中联考化学试题新疆维吾尔自治区石河子第二中学2018-2019学年高一上学期第二次月考化学试题广东省揭阳市惠来县第一中学2018-2019学年高一上学期期中考试化学试题贵州省毕节市纳雍县第一中学2018-2019学年高一下学期期末考试化学试题鲁科版(2019)新教材化学同步2.3.2 氧化还原反应的应用 练习吉林省吉林地区普通高中友好学校联合体第三十一届2019-2020学年高一上学期期中考试化学试题天津市耀华中学2019-2020学年高一上学期期中考试化学试题福建省莆田市第十一中学2019-2020学年高三上学期期中考试化学试题吉林省公主岭市范家屯镇第一中学2019-2020学年高一上学期第二次月考化学试题宁夏石嘴山市第三中学2019-2020学年高一上学期第二次(12月)月考化学试题甘肃省张掖市第二中学2019-2020学年高一上学期期中考试化学试题云南省普洱市景东彝族自治县第一中学2019-2020学年高一上学期12月月考化学试题新疆维吾尔自治区乌鲁木齐市第130中学2018-2019学年高一上学期期中考试化学试题鲁教版高中化学必修1第二章《元素与物质世界》测试卷3广西龙州县高级中学2019-2020学年高一上学期期末考试化学试题(已下线)上海建平中学2013年2月高三开学模拟考试化学试题陕西省宝鸡市金台区2019-2020学年高一上学期期中检测化学试题(已下线)衔接点08 氧化还原反应的一般规律-2020年【衔接教材·暑假作业】初高中衔接化学(已下线)2.3.2 氧化还原反应的应用 练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)陕西省黄陵县中学2020-2021学年高一上学期期中考试化学试题(高新部)四川省冕宁中学2020-2021学年高一上学期期中考试化学试题福建省南平市高级中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】90河北省石家庄外国语学校2020-2021学年高一上学期第二阶段考试化学试卷浙江省嘉兴市2020-2021学年高一上学期期末测试化学试题(已下线)【浙江新东方】在线化学60高一下(已下线)【浙江新东方】在线化学52高一上(已下线)【浙江新东方】高中化学20210429—009【2021】【高一下】广东省连平县忠信中学2020-2021学年高一下学期第二次段考化学试题(已下线)衔接点08 氧化还原反应的一般规律-2021年初升高化学无忧衔接(已下线)单科化学-2021年秋季高三开学摸底考试卷01(课标全国专用)吉林省吉林市第二中学2022届高三上学期9月月考化学试题陕西省西安市第一中学2022届高三上学期期中考试化学试题(已下线)第11讲 氧化还原反应的应用和配平-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)云南省丽江市2021-2022学年高一上学期9月测试化学试题 天津市武清区2022-2023学年高一上学期期中考试化学试题天津市第五十五中学2023-2024学年高一上学期期中检测化学试题浙江省湖州市2023-2024学年高一上学期1月期末化学试题
名校
10 . 利用微生物燃料电池进行废水处理,实现碳氮联合转化。其工作原理如图所示,其中M。N为厌氧微生物电极。下列有关叙述正确的是
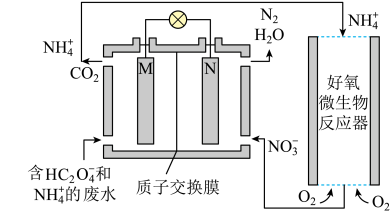

A.负极的电极反应为: |
B.电池工作时, 由N极移向M极 由N极移向M极 |
C.好氧微生物反应器中发生的反应为: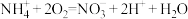 |
D.相同条件下,产生的 和消耗的 和消耗的 体积之比为5:2 体积之比为5:2 |
您最近一年使用:0次
2021-02-04更新
|
328次组卷
|
4卷引用:内蒙古自治区包头市第九中学2022-2023学年高二上学期期末考试化学试题
内蒙古自治区包头市第九中学2022-2023学年高二上学期期末考试化学试题浙江省慈溪市2020-2021学年高二上学期期末测试化学试题(已下线)课时30 新型原电池装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)热点题型训练 新型化学电源及其应用



