29. 海水中蕴藏着丰富的资源。海水综合利用的流程图如下。
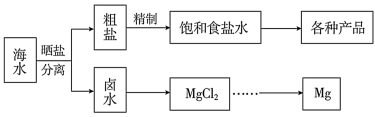
(1)用NaCl作原料可以得到多种产品。
①工业上由NaCl制备金属钠的化学方程式是
______。
②写出产物氯气制备“84”消毒液的离子方程式:
______。
③NaCl也是侯氏制碱法的重要反应物之一,写出侯氏制碱法过程中涉及到的两个主要方程式:
__________ ,
__________。
(2)采用“空气吹出法”从浓海水吹出Br
2,并用纯碱吸收。碱吸收溴的主要反应是Br
2+Na
2CO
3+H
2O―→NaBr+NaBrO
3+NaHCO
3,吸收1 mol Br
2时,转移的电子数为
________mol。
(3)海水提镁的一段工艺流程如下图:
卤水

Mg(OH)
2
MgCl
2溶液→MgCl
2·6H
2O→MgCl
2
Mg
①采用石墨电极电解熔融的氯化镁,发生反应的化学方程式
_________;
②电解时,若有少量水存在,则不能得到镁单质,写出有关反应的化学方程式
__________。
(4)分离出粗盐后的卤水中蕴含着丰富的镁资源,经过下列途径可获得金属镁:其中,由MgCl
2·6H
2O制取无水MgCl
2的部分装置(铁架台、酒精灯已略)如下:
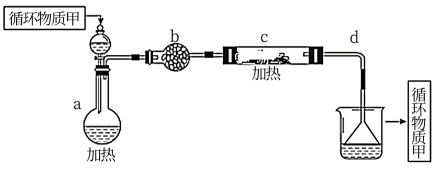
①上图中,装置a由
________、
________、双孔塞和导管组成。
②循环物质甲的名称是
________。
③制取无水氯化镁必须在氯化氢存在的条件下进行,原因是
______。