21. 回答下列问题。
(1)食盐中含有KIO
3,可加入稀硫酸酸化的淀粉碘化钾溶液检测,若变蓝,则说明含有KIO
3,写出相应反应的离子方程式
_____________。
(2) “84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓HCl)不能混用,写出相应反应的离子方程式
_____________。
(3)将32g铜与140mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO
2混合气体在标准状况下的体积为11.2 L。试求:①参加反应的HNO
3的物质的量是
____ mol。②欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为NaNO
3,至少需要通入O
2________mol。
(4)图中所示是用于气体制备、干燥(或除杂质)、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去,各装置可重复使用也可不用)。请根据下列要求回答问题。
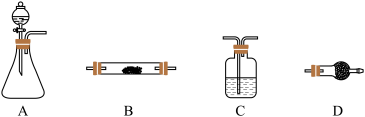
①为验证氯气不能使干燥的红布条褪色,置红布条于B中,按A-C-B-D连接成实验装置体系。A锥形瓶中试剂选用高锰酸钾晶体,则分液漏斗中的液体是浓盐酸;A中发生的化学方程式是
____________,C中试剂是
________,
②为了进行氨的催化氧化实验,若锥形瓶中盛装足量的Na
2O
2粉末,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,产生的气体通过红热的铂粉,各仪器装置按气流方向从左到右连接顺序是(填字母)
_________;装置B中发生反应的化学方程式为
:______。