1 . 钛酸亚铁通过以下反应转化为TiCl4: 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是
 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是| A.12g金刚石中含有C—C键数为4 NA |
| B.标准状况下1.12L CO含有质子数为0.7 NA |
| C.每生成2mol TiCl4转移电子数为12 NA |
| D.1L 0.1mol/L的FeCl3溶液中,阳离子数目为0.1 NA |
您最近一年使用:0次
名校
2 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下 氨气溶于水后所得溶液中 氨气溶于水后所得溶液中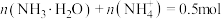 |
B.标准状况下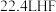 的质量为 的质量为 |
C. 与稀硝酸反应,铁完全溶解转移电子数目一定是 与稀硝酸反应,铁完全溶解转移电子数目一定是 |
D.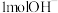 含有电子的数目为 含有电子的数目为 |
您最近一年使用:0次
3 . 氮氧化铝(AlON)是一种透明高硬度防弹材料。其中氧元素的化合价为-2价,可以由反应 合成,下列有关说法正确的是
合成,下列有关说法正确的是
 合成,下列有关说法正确的是
合成,下列有关说法正确的是| A.氮氧化铝中氮元素的化合价是-1价 | B.反应中氮气作还原剂 |
C.反应中每生成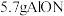 同时生成 同时生成 | D.反应中 是氧化剂 是氧化剂 |
您最近一年使用:0次
4 . 氮及其化合物的转化过程如左图所示,其中右图为反应①过程中能量变化的曲线图。下列分析合理的是
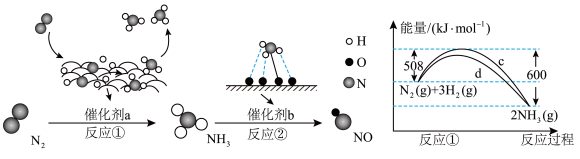

| A.图中c曲线是加入催化剂a时的能量变化曲线 |
| B.增加催化剂a的量能增大①反应的焓变 |
| C.在反应②中,若有1.25mol电子发生转移,则参加反应的NH3的体积为5.6L |
D.反应①的热化学方程式为: |
您最近一年使用:0次
5 . 在焊接铜器时常用 溶液除去铜器表面的氧化铜,其反应为
溶液除去铜器表面的氧化铜,其反应为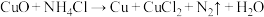 (未配平)。下列说法正确的是
(未配平)。下列说法正确的是
 溶液除去铜器表面的氧化铜,其反应为
溶液除去铜器表面的氧化铜,其反应为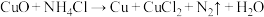 (未配平)。下列说法正确的是
(未配平)。下列说法正确的是A.该反应中 被还原 被还原 |
B.该反应中氧化剂和还原剂的物质的量之比为 |
C.该反应中产生 时,转移 时,转移 电子 电子 |
D.该反应中被还原的 占参与反应的 占参与反应的 的 的 |
您最近一年使用:0次
名校
解题方法
6 . 关于非金属单质及化合物的性质,下列说法不正确的是


| A.常温下向浓HNO3投入铁片会产生大量红棕色气体 |
| B.除去NO中少量的NO2,可以通过盛有水的洗气瓶 |
| C.上图路线Ⅰ、Ⅱ、Ⅲ是雷电固氮生成硝酸的主要途径 |
| D.上图路线①②③是工业生产硝酸的主要途径,①中氧化剂与还原剂的物质的量之比为5:4 |
您最近一年使用:0次
7 . 亚氯酸钠( )是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如图所示。下列说法错误的是
)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如图所示。下列说法错误的是
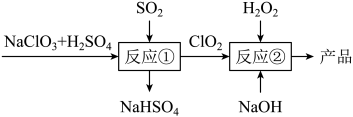
 )是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如图所示。下列说法错误的是
)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathieson)法制备亚氯酸钠的流程如图所示。下列说法错误的是
A. 中氯元素的化合价是+3价 中氯元素的化合价是+3价 |
B.反应②中 被还原 被还原 |
C.若生成 ,理论上消耗 ,理论上消耗 |
D.反应①,参加反应的 和 和 的物质的量之比为 的物质的量之比为 |
您最近一年使用:0次
解题方法
8 . 我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(主要成分为ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:

相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
请回答下列问题:
(1)焙烧过程中产生的气体化学式_______ 。
(2)溶浸时,提高浸出率的方法有_______ 。(至少写出两种)
(3)利用Fe(OH)3悬浊液与含SO2的烟气反应生成FeSO4,可以使烟气脱硫,该反应的离子方程式为_______ 。产物FeSO4在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为_______ 。
(4)氧化除杂时,加入ZnO调节溶液pH,当用广泛pH试纸测得pH值为_______时,可认为已达除杂目的。
(5)滤渣3成分为_______ 。

相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
(1)焙烧过程中产生的气体化学式
(2)溶浸时,提高浸出率的方法有
(3)利用Fe(OH)3悬浊液与含SO2的烟气反应生成FeSO4,可以使烟气脱硫,该反应的离子方程式为
(4)氧化除杂时,加入ZnO调节溶液pH,当用广泛pH试纸测得pH值为_______时,可认为已达除杂目的。
| A.2 | B.2.8 | C.4 | D.6.2 |
您最近一年使用:0次
解题方法
9 . 工业上可利用反应Na2SO4 + 2C Na2S + 2CO2↑来制备硫化钠,下列说法错误的是
Na2S + 2CO2↑来制备硫化钠,下列说法错误的是
 Na2S + 2CO2↑来制备硫化钠,下列说法错误的是
Na2S + 2CO2↑来制备硫化钠,下列说法错误的是| A.该反应中氧化剂和还原剂的物质的量比为1∶2 |
| B.反应中,生成1 mol Na2S时,转移8 mol电子 |
| C.反应中,消耗1 mol碳时,可生成22.4 L 标准状况下的CO2 |
| D.Na2S溶液显碱性是由于S2-+ 2H2O⇌H2S + 2OH- |
您最近一年使用:0次
解题方法
10 . 科学家发现某些生物酶体系可以促进H+和e-的转移(如a、b和c),能将海洋中的NO 转化为N2进入大气层,反应过程如图所示。下列说法正确的是
转化为N2进入大气层,反应过程如图所示。下列说法正确的是

 转化为N2进入大气层,反应过程如图所示。下列说法正确的是
转化为N2进入大气层,反应过程如图所示。下列说法正确的是
A.过程Ⅰ中NO 发生氧化反应 发生氧化反应 |
| B.a和b中转移的e-数目相等 |
C.过程Ⅱ中参与反应的n(NO)∶n(NH ) =1∶1 ) =1∶1 |
D.过程Ⅱ-Ⅲ的总反应NO +NH +NH =N2↑+2H2O =N2↑+2H2O |
您最近一年使用:0次
2023-05-25更新
|
294次组卷
|
2卷引用:2023年第37届中国化学奥林匹克广西预选赛化学试题



