解题方法
1 . 按要求,回答下列问题:
(1)实验室用二氧化锰和浓盐酸反应制取氯气,反应的离子方程式是___________ 。
(2)氯气可用湿润的淀粉碘化钾试纸检验,请用化学方程式解释原因:___________ 。
(3)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是___________ 。
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________。
(5)某同学在探究漂白粉溶液性质时,在漂白粉溶液中加入几滴无色酚酞溶液,发现溶液呈红色,随后溶液迅速褪色,说明漂白粉溶液呈___________ 性,并具有___________ 性。
(6)实验室也可用 固体和浓盐酸反应制氯气,反应方程式如下:
固体和浓盐酸反应制氯气,反应方程式如下: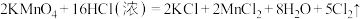 ,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
,若反应中有0.5mol电子转移,被氧化HCl的物质的量为___________ 。
(1)实验室用二氧化锰和浓盐酸反应制取氯气,反应的离子方程式是
(2)氯气可用湿润的淀粉碘化钾试纸检验,请用化学方程式解释原因:
(3)由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入少量的物质是___________。
| A.食醋 | B.食盐 | C.烧碱 | D.纯碱 |
(6)实验室也可用
 固体和浓盐酸反应制氯气,反应方程式如下:
固体和浓盐酸反应制氯气,反应方程式如下: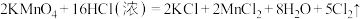 ,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
,若反应中有0.5mol电子转移,被氧化HCl的物质的量为
您最近半年使用:0次
解题方法
2 . 汽车剧烈碰撞时,安全气囊中发生反应 。有关该反应,下列叙述正确的是
。有关该反应,下列叙述正确的是
 。有关该反应,下列叙述正确的是
。有关该反应,下列叙述正确的是A.上述反应中 是还原剂 是还原剂 |
B.每生成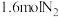 ,转移的电子为2mol ,转移的电子为2mol |
C. 中N的化合价为-3价 中N的化合价为-3价 |
| D.若被氧化的N原子的物质的量为3mol,则氧化产物比还原产物多1.4mol |
您最近半年使用:0次
解题方法
3 . 下列有关 说法正确的是
说法正确的是
 说法正确的是
说法正确的是A. 中阴阳离子的个数比为1:1 中阴阳离子的个数比为1:1 |
B. 体现强氧化性,可以用作呼吸面具的供氧剂 体现强氧化性,可以用作呼吸面具的供氧剂 |
C. 由钠在常温下与氧气反应得到 由钠在常温下与氧气反应得到 |
D. 与 与 反应,产生标准状况下 反应,产生标准状况下 ,转移 ,转移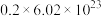 个电子 个电子 |
您最近半年使用:0次
名校
4 . 火箭推进发生反应的化学方程式为: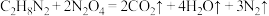 (
( 中C、N元素的化合价相等),下列说法正确的是
中C、N元素的化合价相等),下列说法正确的是
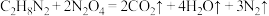 (
( 中C、N元素的化合价相等),下列说法正确的是
中C、N元素的化合价相等),下列说法正确的是A. 是氧化剂 是氧化剂 | B.氧化产物与还原产物之比为2∶3 |
C. 被氧化 被氧化 | D.1mol 完全反应,转移电子数为 完全反应,转移电子数为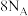 |
您最近半年使用:0次
5 . 将一定量的锌与 浓硫酸充分反应后,锌完全溶解,同时生成气体
浓硫酸充分反应后,锌完全溶解,同时生成气体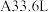 (标准状况)。将反应后的溶液稀释至
(标准状况)。将反应后的溶液稀释至 ,测得溶液的
,测得溶液的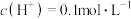 ,则下列叙述中正确的是
,则下列叙述中正确的是
 浓硫酸充分反应后,锌完全溶解,同时生成气体
浓硫酸充分反应后,锌完全溶解,同时生成气体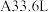 (标准状况)。将反应后的溶液稀释至
(标准状况)。将反应后的溶液稀释至 ,测得溶液的
,测得溶液的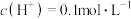 ,则下列叙述中正确的是
,则下列叙述中正确的是A.气体 为 为 |
B.稀释后所得溶液中硫酸根的浓度为 |
| C.该反应若不加热,锌会被钝化 |
D.反应中共转移 电子 电子 |
您最近半年使用:0次
6 . 从元素化合价和物质类别两个角度学习,研究物质的性质,是一种行之有效的方法。下图为氮元素的价类二维图。下列说法错误 的是

A. 的浓溶液与 的浓溶液与 的浓溶液靠近会产生白烟 的浓溶液靠近会产生白烟 |
B. 在一定条件下与氧气反应可直接生成 在一定条件下与氧气反应可直接生成 |
C. 与氧气按一定比例混合溶于水能得到 与氧气按一定比例混合溶于水能得到 |
D.若 为 为 ,碱性条件下由 ,碱性条件下由 、 、 制备 制备 的反应中氧化剂与还原剂的物质的量之比为 的反应中氧化剂与还原剂的物质的量之比为 |
您最近半年使用:0次
7 . 在无氧环境下,将 通入足量
通入足量 稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,并有气体产生。关于上述变化,下列说法
稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,并有气体产生。关于上述变化,下列说法错误 的是
 通入足量
通入足量 稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,并有气体产生。关于上述变化,下列说法
稀溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,并有气体产生。关于上述变化,下列说法A.最终被还原的是 |
B.氧化性: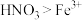 |
C.最终所得溶液中不存在 |
D.同温、同压下, 和逸出气体的体积比为 和逸出气体的体积比为 |
您最近半年使用:0次
解题方法
8 . 废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备 和
和 的部分实验步骤如下:
的部分实验步骤如下: ”步骤中,为加快溶解速率,可采取的措施是
”步骤中,为加快溶解速率,可采取的措施是___________ 。(任写一种方法)。
(2)从“滤液 ”中提取
”中提取 的实验步骤依次为
的实验步骤依次为___________ 、过滤、冰水洗涤、低温干燥,其中冰水洗涤晶体的目的是___________ 。
(3)在“溶解 ”步骤中,发生反应的化学方程式为
”步骤中,发生反应的化学方程式为___________ 。
(4)为测定产品中 的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
 溶液至刚好完全反应,消耗
溶液至刚好完全反应,消耗 溶液25.00mL。
溶液25.00mL。
已知: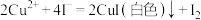 ,
, 。请依据实验数据计算样品中
。请依据实验数据计算样品中 的质量分数
的质量分数___________ (写出计算过程,结果保留2位小数)。
 和
和 的部分实验步骤如下:
的部分实验步骤如下: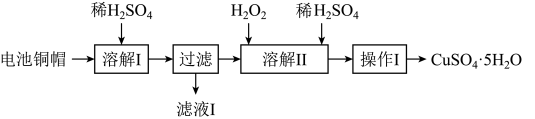
 ”步骤中,为加快溶解速率,可采取的措施是
”步骤中,为加快溶解速率,可采取的措施是(2)从“滤液
 ”中提取
”中提取 的实验步骤依次为
的实验步骤依次为(3)在“溶解
 ”步骤中,发生反应的化学方程式为
”步骤中,发生反应的化学方程式为(4)为测定产品中
 的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000
 溶液至刚好完全反应,消耗
溶液至刚好完全反应,消耗 溶液25.00mL。
溶液25.00mL。已知:
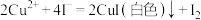 ,
, 。请依据实验数据计算样品中
。请依据实验数据计算样品中 的质量分数
的质量分数
您最近半年使用:0次
9 . 研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是
| A.正极反应式:Ag+Cl--e-=AgCl |
| B.每生成1mol Na2Mn5O10转移2 mol电子 |
| C.Na+不断向“水”电池的负极移动 |
| D.AgCl是还原产物 |
您最近半年使用:0次
名校
10 . 一种处理温室气体二氧化碳的方法: ,
, 代表阿伏加德罗常数的值。下列说法
代表阿伏加德罗常数的值。下列说法不正确 的是
 ,
, 代表阿伏加德罗常数的值。下列说法
代表阿伏加德罗常数的值。下列说法A.标准状况下,2.24 L  中共用的电子对数为 中共用的电子对数为 |
B.0.1 mol 中含有的电子数为 中含有的电子数为 |
C.生成18 g 转移电子数为 转移电子数为 |
D.1 mol  和2 mol 和2 mol  充分反应生成 充分反应生成 的分子数为 的分子数为 |
您最近半年使用:0次



