名校
解题方法
1 . 38.4gCu与一定量浓硝酸恰好完全反应生成氮的氧化物,这些氧化物恰好溶解在NaOH溶液中得到 和
和 的混合溶液,反应过程及有关数据如图所示
的混合溶液,反应过程及有关数据如图所示
 和
和 的混合溶液,反应过程及有关数据如图所示
的混合溶液,反应过程及有关数据如图所示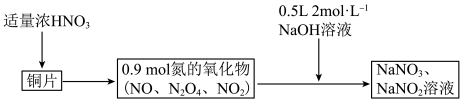
| A.硝酸在反应中既体现氧化性又体现酸性 |
| B.氮的氧化物和NaOH溶液反应时,NO作还原剂 |
C.混合气体中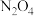 的物质的量是0.2mol 的物质的量是0.2mol |
| D.若浓硝酸体积为200mL,则其物质的量浓度为11mol/L |
您最近半年使用:0次
2024-02-17更新
|
1261次组卷
|
12卷引用:陕西省西安铁一中学2023-2024学年高一上学期期末考试化学试题
陕西省西安铁一中学2023-2024学年高一上学期期末考试化学试题重庆市第七中学校2023-2024学年高一下学期第一次月考化学试卷广东省佛山市顺德区容山中学2023-2024学年高一下学期3月月考化学试题(已下线)安徽省皖北县中联盟2023-2024学年高一下学期3月月考化学试题内蒙古自治区乌兰浩特第一中学2023-2024学年高一下学期第一次月考化学试题山东省临沂第四中学2023-2024学年高一下学期3月月考化学试题江西省抚州市金溪县第一中学2023-2024学年高一下学期第一次月考化学试卷江西省宜春市丰城中学2023-2024学年高一下学期3月月考化学试题陕西省商洛市商州区高级中学2023-2024学年高一下学期3月月考化学试题安徽省淮南市第二中2023-2024学年高一下学期第一次月考化学试题四川省射洪中学校强基班2023-2024学年高一下学期4月第一次月考化学试题黑龙江省哈尔滨市第六中学校2023-2024学年高一下学期4月测试化学试卷
名校
解题方法
2 . 五氟化锑主要用作氟化工的催化剂,也用作纺织工业物阻燃剂,在染料工业中用于制造染料中间体,此外,还用于制备高纯度金属锑、无机离子交换材料和胶体五氧化二锑。以某锑矿(主要成分为 ,含有少量
,含有少量 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如下图:
的工艺流程如下图:
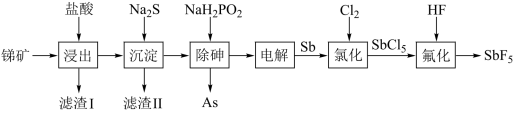
已知:Ⅰ. 、
、 的
的 分别为
分别为 、
、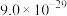 ;
;
Ⅱ. 微溶于水、
微溶于水、 难溶于水,它们均为两性氧化物;
难溶于水,它们均为两性氧化物; 难溶于水。
难溶于水。
回答下列问题:
(1)已知锑与氮元同素主族,原子序数为51,写出锑的价电子排布图_______ 。
(2)“浸出”时少量 转化为“滤渣1”。其成分为
转化为“滤渣1”。其成分为 ,加入氨水“除氯”,同时将其转化为
,加入氨水“除氯”,同时将其转化为 ,能否用
,能否用 溶液代替氨水
溶液代替氨水_______ ,(填“能”或“否”),原因是_______ 。
(3)“沉淀”的过程是加入极稀的 溶液,其目的是使
溶液,其目的是使 和
和 转化为相应的硫化物而除去,当
转化为相应的硫化物而除去,当 、
、 共沉时,
共沉时,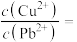
_______ 。
(4)“除砷”时, 转化为H3PO4,该反应中氧化剂和还原剂的物质的量比是
转化为H3PO4,该反应中氧化剂和还原剂的物质的量比是_______ 。
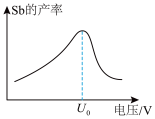
(5)“电解”中锑的产率与电压大小关系如下图所示。当电压未超过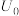 V时,阴极反应方程式为
V时,阴极反应方程式为
 ,当电压超过
,当电压超过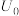 V时,锑的产率降低,阴极还可能发生了
V时,锑的产率降低,阴极还可能发生了_______ 反应。(写出电极反应式)
(6) 与
与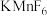 反应。首次实现了用化学方法制取
反应。首次实现了用化学方法制取 ,同时生成
,同时生成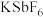 和
和 ,化学反应方程式为
,化学反应方程式为_______ 。
 ,含有少量
,含有少量 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如下图:
的工艺流程如下图:
已知:Ⅰ.
 、
、 的
的 分别为
分别为 、
、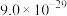 ;
;Ⅱ.
 微溶于水、
微溶于水、 难溶于水,它们均为两性氧化物;
难溶于水,它们均为两性氧化物; 难溶于水。
难溶于水。回答下列问题:
(1)已知锑与氮元同素主族,原子序数为51,写出锑的价电子排布图
(2)“浸出”时少量
 转化为“滤渣1”。其成分为
转化为“滤渣1”。其成分为 ,加入氨水“除氯”,同时将其转化为
,加入氨水“除氯”,同时将其转化为 ,能否用
,能否用 溶液代替氨水
溶液代替氨水(3)“沉淀”的过程是加入极稀的
 溶液,其目的是使
溶液,其目的是使 和
和 转化为相应的硫化物而除去,当
转化为相应的硫化物而除去,当 、
、 共沉时,
共沉时,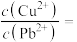
(4)“除砷”时,
 转化为H3PO4,该反应中氧化剂和还原剂的物质的量比是
转化为H3PO4,该反应中氧化剂和还原剂的物质的量比是(5)“电解”中锑的产率与电压大小关系如下图所示。当电压未超过
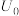 V时,阴极反应方程式为
V时,阴极反应方程式为
 ,当电压超过
,当电压超过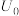 V时,锑的产率降低,阴极还可能发生了
V时,锑的产率降低,阴极还可能发生了
(6)
 与
与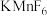 反应。首次实现了用化学方法制取
反应。首次实现了用化学方法制取 ,同时生成
,同时生成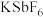 和
和 ,化学反应方程式为
,化学反应方程式为
您最近半年使用:0次
名校
3 . 在反应3Cl2+6KOH(浓) KClO3+5KCl+3H2O中,氧化剂与还原剂的物质的量之比为
KClO3+5KCl+3H2O中,氧化剂与还原剂的物质的量之比为
 KClO3+5KCl+3H2O中,氧化剂与还原剂的物质的量之比为
KClO3+5KCl+3H2O中,氧化剂与还原剂的物质的量之比为| A.5∶1 | B.4∶1 | C.1∶5 | D.1∶1 |
您最近半年使用:0次
解题方法
4 . 四氢铝钠( )是强还原剂和供氢剂,高铁酸钠(
)是强还原剂和供氢剂,高铁酸钠( )是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为
)是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为 、
、 和
和 含少量
含少量 )为原料制备四氢铝钠和高铁酸钠的流程如下(已知
)为原料制备四氢铝钠和高铁酸钠的流程如下(已知 是难溶于水的酸性氧化物):
是难溶于水的酸性氧化物):

回答下列问题:
(1) 中氢的化合价为
中氢的化合价为_______ 。
(2)浸渣的主要成分是_______ (填化学式);“转化”中 的具体作用是
的具体作用是_______ 。
(3)由 制备
制备 的离子方程式为
的离子方程式为_______ ;“分离”中铝元素转化成_______ (填离子符号)。
(4)“沉铝”后所得滤液经蒸干、灼烧得到固体是_______ 。
(5)“合成”中乙醚作溶剂,发生反应的化学方程式为_______ 。
(6)“有效氢”指单位质量(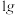 )含氢还原剂的还原能力相当于多少克氢气的还原能力。
)含氢还原剂的还原能力相当于多少克氢气的还原能力。 、
、 的“有效氢”如图所示,则乙代表
的“有效氢”如图所示,则乙代表_______ (填化学式)。

 )是强还原剂和供氢剂,高铁酸钠(
)是强还原剂和供氢剂,高铁酸钠( )是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为
)是一种绿色净水剂。以工业制备硫酸的烧渣(主要成分为 、
、 和
和 含少量
含少量 )为原料制备四氢铝钠和高铁酸钠的流程如下(已知
)为原料制备四氢铝钠和高铁酸钠的流程如下(已知 是难溶于水的酸性氧化物):
是难溶于水的酸性氧化物):
回答下列问题:
(1)
 中氢的化合价为
中氢的化合价为(2)浸渣的主要成分是
 的具体作用是
的具体作用是(3)由
 制备
制备 的离子方程式为
的离子方程式为(4)“沉铝”后所得滤液经蒸干、灼烧得到固体是
(5)“合成”中乙醚作溶剂,发生反应的化学方程式为
(6)“有效氢”指单位质量(
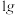 )含氢还原剂的还原能力相当于多少克氢气的还原能力。
)含氢还原剂的还原能力相当于多少克氢气的还原能力。 、
、 的“有效氢”如图所示,则乙代表
的“有效氢”如图所示,则乙代表
您最近半年使用:0次
解题方法
5 .  (绿矾)常用于制补血剂。以某废液[含
(绿矾)常用于制补血剂。以某废液[含 、
、 和
和 ]为原料制备绿矾并测定其纯度(已知
]为原料制备绿矾并测定其纯度(已知 溶解度随着温度升高而增大),流程如下图所示:
溶解度随着温度升高而增大),流程如下图所示:

称取a g绿矾溶于水配制成250 溶液,准确量取25
溶液,准确量取25 溶液,加入20
溶液,加入20 0.1
0.1
 溶液恰好完全反应,发生反应
溶液恰好完全反应,发生反应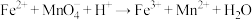 (未配平)。下列叙述错误的是
(未配平)。下列叙述错误的是
 (绿矾)常用于制补血剂。以某废液[含
(绿矾)常用于制补血剂。以某废液[含 、
、 和
和 ]为原料制备绿矾并测定其纯度(已知
]为原料制备绿矾并测定其纯度(已知 溶解度随着温度升高而增大),流程如下图所示:
溶解度随着温度升高而增大),流程如下图所示:
称取a g绿矾溶于水配制成250
 溶液,准确量取25
溶液,准确量取25 溶液,加入20
溶液,加入20 0.1
0.1
 溶液恰好完全反应,发生反应
溶液恰好完全反应,发生反应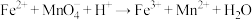 (未配平)。下列叙述错误的是
(未配平)。下列叙述错误的是| A.“操作2”是蒸发浓缩、降温结晶、过滤、洗涤、干燥 |
B.用 溶液可检验滤液是否含 溶液可检验滤液是否含 |
C.配制一定浓度溶液需要使用的定量仪器有托盘天平、量筒、250 容量瓶 容量瓶 |
D.该绿矾中 的质量分数为 的质量分数为 |
您最近半年使用:0次
名校
6 . 在浓盐酸中加入少量KMnO4,剧烈反应,产生黄绿色有刺激性气味的气体,溶液紫红色褪去,已知该反应的化学方程式为2KMnO4+16HCI(浓)=2KCI+2MnCl2+8H2O+5Cl2↑。结合下表信息,回答问题:
(1)标出该反应中电子转移的方向和数目 _______ 。
2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
其中氧化产物是_______ ,被还原的元素是_______ 。每生成71g氯气,则被氧化的还原剂的质量为_______ g。
(2)取一定量的酸性KMnO4溶液依次进行下列实验,有关现象记录如下:滴加适量H2O2,紫红色褪去,并有无色气泡产生;再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
①在配制酸性KMnO4溶液时,能否用盐酸?_______ ,原因是_______ 。
②KMnO4、H2O2、PbO2的氧化性由强到弱的可能顺序为_______ 。
③根据上述反应能否比较Cl2与H2O2的氧化性强弱?_______ 。
| 氯气(Cl2) | KMnO4 | PbO2 |
| 有刺激性气味,呈黄绿色,有毒气体 | 易溶于水,溶液呈紫红色,可用于杀菌消毒 | Pb的最高化合价为+4,其稳定化合价为+2,难溶于水,灰色固体 |
2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
其中氧化产物是
(2)取一定量的酸性KMnO4溶液依次进行下列实验,有关现象记录如下:滴加适量H2O2,紫红色褪去,并有无色气泡产生;再加入适量的PbO2固体,固体溶解,溶液又变为紫红色。
①在配制酸性KMnO4溶液时,能否用盐酸?
②KMnO4、H2O2、PbO2的氧化性由强到弱的可能顺序为
③根据上述反应能否比较Cl2与H2O2的氧化性强弱?
您最近半年使用:0次
名校
7 . 已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
(1)该“84消毒液”的物质的量浓度约为_______ mol·L-1。
(2)该同学参阅该“84消毒液”的配方,欲用NaCIO固体配制480mL含NaCIO质量分数为25%的消毒液。下列说法正确的是_______。
(3)84消毒液与洁厕灵(主要成分是盐酸)混合后使用,就会对人体产生严重的危害,发生的反应如下: ,取100mL上述稀释过的84消毒液与足量洁厕灵混合,产生氯气的体积在标准状况下约为
,取100mL上述稀释过的84消毒液与足量洁厕灵混合,产生氯气的体积在标准状况下约为_______ L(保留两位有效数字)。
(4)写出与Cl-具有相同电子数的正离子、负离子、分子各一种:_______ 、_______ 、_______ 。
| 84消毒液 有效成分:NaClO 规格:1000mL 质量分数:25% 密度:1.192g·cm-3 |
(2)该同学参阅该“84消毒液”的配方,欲用NaCIO固体配制480mL含NaCIO质量分数为25%的消毒液。下列说法正确的是_______。
| A.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| B.需要称量NaClO固体的质量为149.0g |
| C.将NaCIO固体于烧杯中溶解后,应立即将溶液转移到容量瓶中 |
| D.配制好的溶液可置于容量瓶中保存 |
 ,取100mL上述稀释过的84消毒液与足量洁厕灵混合,产生氯气的体积在标准状况下约为
,取100mL上述稀释过的84消毒液与足量洁厕灵混合,产生氯气的体积在标准状况下约为(4)写出与Cl-具有相同电子数的正离子、负离子、分子各一种:
您最近半年使用:0次
8 . 实验室制取少量氮气的反应为;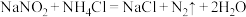 。下列关于该反应的说法正确的是
。下列关于该反应的说法正确的是
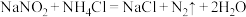 。下列关于该反应的说法正确的是
。下列关于该反应的说法正确的是A. 中氮元素被氧化 中氮元素被氧化 | B. 作氧化剂 作氧化剂 |
C. 发生还原反应 发生还原反应 | D.每生成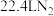 ,转移 ,转移 电子 电子 |
您最近半年使用:0次
名校
9 . 一块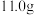 的铁铝合金,加入一定量的稀硫酸后合金完全溶解,然后加
的铁铝合金,加入一定量的稀硫酸后合金完全溶解,然后加 至溶液中无
至溶液中无 存在,加热除去多余的
存在,加热除去多余的 ,当加入
,当加入 溶液时沉淀量最多,且所得沉淀质量为
溶液时沉淀量最多,且所得沉淀质量为 ,下列说法正确的是
,下列说法正确的是
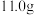 的铁铝合金,加入一定量的稀硫酸后合金完全溶解,然后加
的铁铝合金,加入一定量的稀硫酸后合金完全溶解,然后加 至溶液中无
至溶液中无 存在,加热除去多余的
存在,加热除去多余的 ,当加入
,当加入 溶液时沉淀量最多,且所得沉淀质量为
溶液时沉淀量最多,且所得沉淀质量为 ,下列说法正确的是
,下列说法正确的是| A.该合金中铁的质量为2.8g |
B.所加的稀硫酸中溶质的物质的量为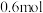 |
C.合金与稀硫酸反应生成 |
D.该合金与足量氢氧化钠反应,转移的电子数为 |
您最近半年使用:0次
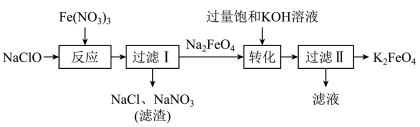
10 . 高铁酸钾( )能溶于水,微溶于浓
)能溶于水,微溶于浓 溶液,难溶于无水乙醇,低温碱性条件下比较稳定。工业上湿法制备
溶液,难溶于无水乙醇,低温碱性条件下比较稳定。工业上湿法制备 的流程如下,下列说法不正确的是
的流程如下,下列说法不正确的是
 )能溶于水,微溶于浓
)能溶于水,微溶于浓 溶液,难溶于无水乙醇,低温碱性条件下比较稳定。工业上湿法制备
溶液,难溶于无水乙醇,低温碱性条件下比较稳定。工业上湿法制备 的流程如下,下列说法不正确的是
的流程如下,下列说法不正确的是
| A.“过滤I”中用到的玻璃仪器有分液漏斗、玻璃棒、烧杯 |
| B.“反应”中,氧化剂和还原剂的物质的量之比为3:2 |
C.“转化”能进行说明该条件下 的溶解度小于 的溶解度小于 |
D.“过滤Ⅱ”所得 晶体可用无水乙醇洗涤 晶体可用无水乙醇洗涤 |
您最近半年使用:0次



