名校
1 . 二氧化氯泡腾片是常用的鱼缸消毒剂,也可用于除居室甲醛,其反应方程式可表示为: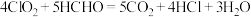 ,下列说法不正确的是
,下列说法不正确的是
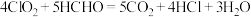 ,下列说法不正确的是
,下列说法不正确的是| A.甲醛具有还原性 |
B.二氧化氯是氧化剂,还原产物为 |
C.反应生成 ,则转移4mol电子 ,则转移4mol电子 |
D.若将二氧化氯改为次氯酸钠,消耗等量甲醛所需 与 与 的物质的量之比为 的物质的量之比为 |
您最近一年使用:0次
名校
2 . NO2的储存和还原技术能有效降低柴油发动机在空气过量时排放的NO2,原理如图1所示。用H2模拟尾气中还原性气体研究了Ba(NO3)2的催化还原过程,如图2所示。
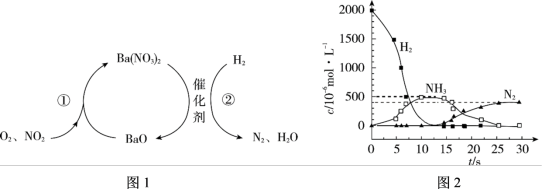
下列说法不正确 的是

下列说法
| A.反应①为4NO2 + O2 + 2BaO = 2Ba(NO3)2 |
| B.储存和还原技术也能降低尾气排放的NO |
| C.0~12.5 s内,氢气的消耗速率为v(H2) = 1.6 × 10﹣4 mol/(L·s) |
| D.反应②分两步进行, 第一步反应消耗的H2与Ba(NO3)2的物质的量之比是1∶8 |
您最近一年使用:0次
名校
解题方法
3 . 一种从阳极泥(主要成分为Cu、Ag、Pt、Au、 、
、 等)中回收Se和贵重金属的工艺流程如图所示:
等)中回收Se和贵重金属的工艺流程如图所示:
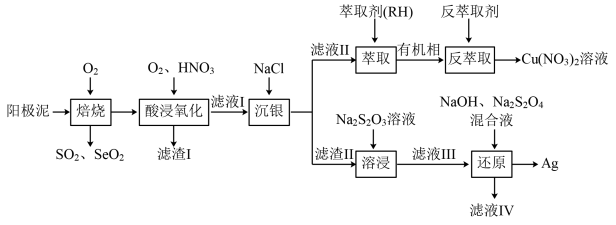
已知:①该工艺中萃取与反萃取的原理为: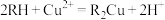 。
。
② 易与
易与 形成配离子:
形成配离子: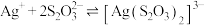 ,上述工艺条件下该反应的平衡常数为
,上述工艺条件下该反应的平衡常数为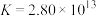 。
。
③上述工艺条件下,AgCl的溶度积常数: 。
。
(1)“焙烧”产生的; 与
与 的混合烟气可用水吸收制得单质Se,该反应的化学方程式为
的混合烟气可用水吸收制得单质Se,该反应的化学方程式为____________ 。
(2)“滤渣Ⅰ”的主要成分是______ (填化学式);“酸浸氧化”中通入氧气,体现了绿色化学的思想,其目的是____________ 。
(3)“反萃取剂”最好选用______ (填化学式)溶液。
(4)“溶浸”过程中滤渣Ⅱ被 溶液溶解,发生反应的平衡常数为
溶液溶解,发生反应的平衡常数为______ 。
(5)“还原”过程中; 没有参与氧化还原过程,“滤液Ⅳ”中还主要含有
没有参与氧化还原过程,“滤液Ⅳ”中还主要含有 。“还原”过程中氧化剂与还原剂的物质的量之比为
。“还原”过程中氧化剂与还原剂的物质的量之比为______ 。
(6)为减少工艺中试剂用量,“滤液Ⅳ”可返回______ (填工序名称)工序循环使用。
 、
、 等)中回收Se和贵重金属的工艺流程如图所示:
等)中回收Se和贵重金属的工艺流程如图所示:
已知:①该工艺中萃取与反萃取的原理为:
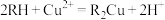 。
。②
 易与
易与 形成配离子:
形成配离子: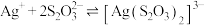 ,上述工艺条件下该反应的平衡常数为
,上述工艺条件下该反应的平衡常数为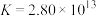 。
。③上述工艺条件下,AgCl的溶度积常数:
 。
。(1)“焙烧”产生的;
 与
与 的混合烟气可用水吸收制得单质Se,该反应的化学方程式为
的混合烟气可用水吸收制得单质Se,该反应的化学方程式为(2)“滤渣Ⅰ”的主要成分是
(3)“反萃取剂”最好选用
(4)“溶浸”过程中滤渣Ⅱ被
 溶液溶解,发生反应的平衡常数为
溶液溶解,发生反应的平衡常数为(5)“还原”过程中;
 没有参与氧化还原过程,“滤液Ⅳ”中还主要含有
没有参与氧化还原过程,“滤液Ⅳ”中还主要含有 。“还原”过程中氧化剂与还原剂的物质的量之比为
。“还原”过程中氧化剂与还原剂的物质的量之比为(6)为减少工艺中试剂用量,“滤液Ⅳ”可返回
您最近一年使用:0次
名校
解题方法
4 . 根据所学知识,回答下列问题。
(1)汽车尾气中常含有NO、CO等气体,在催化剂的作用下NO和CO可反应生成 和
和 ,请写出该反应的化学方程式:
,请写出该反应的化学方程式:___________ 。
(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:___________ 。
(3)胶体和溶液的本质区别是___________ (填标号)。
A.能否发生电泳 B.分散质粒子的直径大小不同 C.能否产生丁达尔效应
(4)下列状态的物质既属于电解质又能导电的是___________(填标号)。
(5)饮用水中的 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: ,上述反应中若生成标准状况下
,上述反应中若生成标准状况下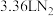 ,则转移的电子数目为
,则转移的电子数目为___________ 。
(1)汽车尾气中常含有NO、CO等气体,在催化剂的作用下NO和CO可反应生成
 和
和 ,请写出该反应的化学方程式:
,请写出该反应的化学方程式:(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体,请写出该反应的离子方程式:
(3)胶体和溶液的本质区别是
A.能否发生电泳 B.分散质粒子的直径大小不同 C.能否产生丁达尔效应
(4)下列状态的物质既属于电解质又能导电的是___________(填标号)。
| A.熔融的NaCl | B.纯净的矿泉水 | C.某品牌的饮料 | D.熟石灰固体 |
 对人类健康产生危害,为了降低饮用水中
对人类健康产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: ,上述反应中若生成标准状况下
,上述反应中若生成标准状况下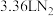 ,则转移的电子数目为
,则转移的电子数目为
您最近一年使用:0次
名校
解题方法
5 . 通常利用反应: 定性检验
定性检验 ,关于该反应的下列说法中,
,关于该反应的下列说法中,不正确 的是
 定性检验
定性检验 ,关于该反应的下列说法中,
,关于该反应的下列说法中,A. 被氧化 被氧化 | B.每消耗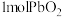 ,转移 ,转移 |
C. 和 和 的物质的量之比为5:2 的物质的量之比为5:2 | D.此反应会使溶液的 变大 变大 |
您最近一年使用:0次
23-24高一下·全国·课前预习
解题方法
6 . 酸雨的防治
用NaOH溶液可以吸收NOx,反应的化学方程式如下:
i.NO2+NO+2NaOH=2NaNO2+H2O
ii.2NO2+2NaOH=NaNO2+NaNO3+H2O
(1)反应i中,每消耗0.3molNO2,转移电子数为______ 。
(2)反应ii中,氧化剂和还原剂的物质的量之比为______ 。
用NaOH溶液可以吸收NOx,反应的化学方程式如下:
i.NO2+NO+2NaOH=2NaNO2+H2O
ii.2NO2+2NaOH=NaNO2+NaNO3+H2O
(1)反应i中,每消耗0.3molNO2,转移电子数为
(2)反应ii中,氧化剂和还原剂的物质的量之比为
您最近一年使用:0次
名校
7 . NA代表阿伏加德罗常数的值。下列说法正确的是
| A.粗铜冶炼过程中每消耗2NA电子,阳极质量减轻64 g |
| B.标况下,22.4 LCl2被足量NaOH溶液完全吸收,转移电子数为NA |
C.将0.1 mol  溶于1 L pH=1的硫酸中,溶液中含有的 溶于1 L pH=1的硫酸中,溶液中含有的 数目为01NA 数目为01NA |
D.常温下,1 L0.5 mol/LCH3COONH4溶液的pH=7,溶液中的 数等于0.5NA 数等于0.5NA |
您最近一年使用:0次
名校
8 . 部分物质的转化关系如下图所示。下列说法错误的是


| A.X是O2 | B.氧化性Na2FeO4比Z的强 |
| C.反应1中Na2O2只作氧化剂 | D.反应2中每生成1molZ转移2mole- |
您最近一年使用:0次
名校
解题方法
9 . 湿润的土壤中,氮元素的转化过程如下图所示。下列说法错误的是
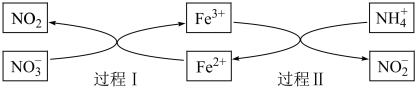

A.过程Ⅰ中NO 表现出氧化性 表现出氧化性 |
B.过程Ⅱ中NO 为氧化产物 为氧化产物 |
| C.上述转化中Fe2+的物质的量理论上不会发生改变 |
D.上述过程中,NO 与NH 与NH 恰好完全反应的物质的量之比为1∶6 恰好完全反应的物质的量之比为1∶6 |
您最近一年使用:0次
10 . 关于反应H2O+SO2+HClO=H2SO4(稀)+HCl,下列说法正确的是
| A.HClO发生氧化反应 |
| B.氧化性:HClO>H2SO4(稀) |
| C.参加反应的还原剂与氧化剂的质量之比为1∶1 |
| D.每生成2molHCl,转移2mol电子 |
您最近一年使用:0次



