解题方法
1 . 实验室可以用氯气制备多种物质,某化学小组在实验室制备 、NaClO和
、NaClO和 三种物质。实验装置如下图所示,其中C的试管里盛有15mL 30% KOH溶液,并置于热水浴中;D的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;F中硬质玻璃管中为还原铁粉,FeCl3能吸收空气里的水分而潮解。回答下列问题:
三种物质。实验装置如下图所示,其中C的试管里盛有15mL 30% KOH溶液,并置于热水浴中;D的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;F中硬质玻璃管中为还原铁粉,FeCl3能吸收空气里的水分而潮解。回答下列问题:
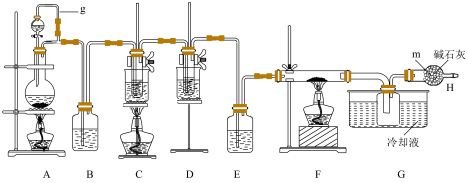
(1)装置A中用 和浓盐酸反应制备
和浓盐酸反应制备 的离子方程式为
的离子方程式为_______ 。
(2)装置A中g管的作用是_______ ;装置B中的试剂是_______ ;装置E中的试剂是_______ 。
(3)比较制取 和NaClO的反应条件,二者的差异是:
和NaClO的反应条件,二者的差异是:_______ 。
(4)写出制备NaClO反应的离子方程式_______ 。
(5)写出制备 的化学反应方程式
的化学反应方程式_______ 。
(6)若没有控制好反应温度,C中产物中可能有 、KClO和KCl三种盐生成,反应后
、KClO和KCl三种盐生成,反应后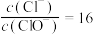 ,则溶液
,则溶液
_______ (填分数比)。
(7)碱石灰的成分是NaOH和CaO的混合物,盛放碱石灰的仪器m的名称是_______ ,其作用是(答出两条)_______ 。
 、NaClO和
、NaClO和 三种物质。实验装置如下图所示,其中C的试管里盛有15mL 30% KOH溶液,并置于热水浴中;D的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;F中硬质玻璃管中为还原铁粉,FeCl3能吸收空气里的水分而潮解。回答下列问题:
三种物质。实验装置如下图所示,其中C的试管里盛有15mL 30% KOH溶液,并置于热水浴中;D的试管里盛有15mL 8% NaOH溶液,并置于冰水浴中;F中硬质玻璃管中为还原铁粉,FeCl3能吸收空气里的水分而潮解。回答下列问题:
(1)装置A中用
 和浓盐酸反应制备
和浓盐酸反应制备 的离子方程式为
的离子方程式为(2)装置A中g管的作用是
(3)比较制取
 和NaClO的反应条件,二者的差异是:
和NaClO的反应条件,二者的差异是:(4)写出制备NaClO反应的离子方程式
(5)写出制备
 的化学反应方程式
的化学反应方程式(6)若没有控制好反应温度,C中产物中可能有
 、KClO和KCl三种盐生成,反应后
、KClO和KCl三种盐生成,反应后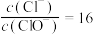 ,则溶液
,则溶液
(7)碱石灰的成分是NaOH和CaO的混合物,盛放碱石灰的仪器m的名称是
您最近一年使用:0次
名校
2 . 将一定质量的镁、铜合金加到稀硝酸溶液中,两者恰好完全反应,假设反应过程中还原产物全部是NO,向所得溶液中加入物质的量浓度为3mol·L-1的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是
| A.开始加入合金的质量可能为16.4g |
| B.参加反应的硝酸的物质的量为0.1mol |
| C.生成沉淀完全时消耗NaOH溶液的体积为100mL |
| D.标准状况下产物NO的体积为22.4L |
您最近一年使用:0次
3 . 三氟化氮(NF3)是一种无色、无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有HF、NO和HNO3,请根据要求回答下列问题:
(1)写出三氟化氮(NF3)的电子式_______ ,三氟化氮分子中所有的原子最外层_______ (填“满足”或“不满足”)8电子稳定结构,反应过程中,被氧化与被还原的元素原子的物质的量之比为_______ 。
(2)写出该反应的化学方程式:_______ 。若反应中生成0.2 mol HNO3,转移的电子数目为_______ 。
(3)三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F.据题意推测NF3、F2、NO三种气体中,氧化性由弱到强的顺序为_______ 。
(4)NF3是一种无色、无味的气体,一旦NF3在空气中泄漏,却还是易于发现。你判断该气体泄漏时的现象是_______ (答一点即可)。
(5)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO2、NaF、H2O外,还肯定有_______ (填化学式)。
(1)写出三氟化氮(NF3)的电子式
(2)写出该反应的化学方程式:
(3)三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F.据题意推测NF3、F2、NO三种气体中,氧化性由弱到强的顺序为
(4)NF3是一种无色、无味的气体,一旦NF3在空气中泄漏,却还是易于发现。你判断该气体泄漏时的现象是
(5)一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染,其产物除NaNO2、NaF、H2O外,还肯定有
您最近一年使用:0次
4 . 现有下列几个离子反应:① ;②
;② ;③
;③
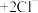 ;④
;④ 。下列有关上述反应说法错误的是
。下列有关上述反应说法错误的是
 ;②
;② ;③
;③
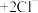 ;④
;④ 。下列有关上述反应说法错误的是
。下列有关上述反应说法错误的是A.氧化性: |
B.还原性: |
| C.反应①中氧化剂和氧化产物的物质的量之比是1∶3 |
| D.反应④恰好完全反应后溶液的pH值增大 |
您最近一年使用:0次
5 . 三星堆遗址发掘出了大量的文物,除了神秘的黄金面具之外,当属高大的青铜神树最为夺人眼球。修复后青铜神树表面有绿色的铜锈,它的化学成分是 (碱式碳酸铜),生锈的原理是:
(碱式碳酸铜),生锈的原理是: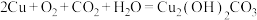 。下列有关该反应的说法错误的是
。下列有关该反应的说法错误的是
 (碱式碳酸铜),生锈的原理是:
(碱式碳酸铜),生锈的原理是: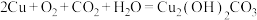 。下列有关该反应的说法错误的是
。下列有关该反应的说法错误的是| A.该反应既属于氧化还原反应,又属于化合反应 |
| B.该反应中氧化产物和还原产物是同一种物质 |
| C.氧化剂和还原剂的质量比为1∶2 |
D.反应生成1mol  转移的电子数是4 转移的电子数是4 |
您最近一年使用:0次
名校
解题方法
6 .  具有很好的导电性,在光学、电学等行业有着重要的用途,其分子结构如图所示。将干燥的氨气通入
具有很好的导电性,在光学、电学等行业有着重要的用途,其分子结构如图所示。将干燥的氨气通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: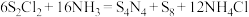 [已知
[已知 (分子结构为
(分子结构为 是硫单质中最稳定的]。下列说法错误的是
是硫单质中最稳定的]。下列说法错误的是

A. 属于分子晶体, 属于分子晶体,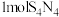 中含有 中含有 极性键 极性键 |
B. 中含有 中含有 非极性键 非极性键 |
C.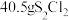 参与上述制备反应,转移 参与上述制备反应,转移 电子 电子 |
D. 的VSEPR模型均为四面体形 的VSEPR模型均为四面体形 |
您最近一年使用:0次
2024-03-03更新
|
384次组卷
|
2卷引用:山东省菏泽市东明县第一中学2023-2024学年高三下学期开学化学试题
名校
7 . 氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
I.电解水制备法 ),同时产生的氢原子会重组成
),同时产生的氢原子会重组成 。该过程如图所示:
。该过程如图所示:
(1)基态铜原子的价层电子轨道表示式为___________ 。
(2)已知:i.醛极易被氧化;ii.电解反应越难发生,电解所需电压越高
①在碱性条件下电解水制氢时,阳极发生的电极反应为___________ 。
②推测醛氧化制氢所需电压比电解水制氢___________ (填“低”、“高”或“相同”)。
③补全醛催化氧化时,阳极的电极反应式:___________ 。
 □
□ □
□
(3)上述电解装置工作时,每转移1 mol电子时,生成 的物质的量为
的物质的量为___________ 。
Ⅱ.甲烷水蒸气催化重整法
恒温恒压下甲烷和水蒸气的反应为: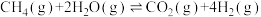

(4)达到平衡后通入氮气,分析 平衡转化率的变化及原因
平衡转化率的变化及原因___________ 。
(5)反应的过程中发生副反应
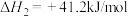 ,将
,将 混合气体通入反应体系,平衡时各组分的物质的量分数与温度的关系如图所示。分析750℃以后曲线a下降的原因是
混合气体通入反应体系,平衡时各组分的物质的量分数与温度的关系如图所示。分析750℃以后曲线a下降的原因是___________ 。
I.电解水制备法

 ),同时产生的氢原子会重组成
),同时产生的氢原子会重组成 。该过程如图所示:
。该过程如图所示:(1)基态铜原子的价层电子轨道表示式为
(2)已知:i.醛极易被氧化;ii.电解反应越难发生,电解所需电压越高
①在碱性条件下电解水制氢时,阳极发生的电极反应为
②推测醛氧化制氢所需电压比电解水制氢
③补全醛催化氧化时,阳极的电极反应式:
 □
□ □
□
(3)上述电解装置工作时,每转移1 mol电子时,生成
 的物质的量为
的物质的量为Ⅱ.甲烷水蒸气催化重整法
恒温恒压下甲烷和水蒸气的反应为:
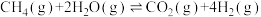

(4)达到平衡后通入氮气,分析
 平衡转化率的变化及原因
平衡转化率的变化及原因(5)反应的过程中发生副反应

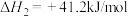 ,将
,将 混合气体通入反应体系,平衡时各组分的物质的量分数与温度的关系如图所示。分析750℃以后曲线a下降的原因是
混合气体通入反应体系,平衡时各组分的物质的量分数与温度的关系如图所示。分析750℃以后曲线a下降的原因是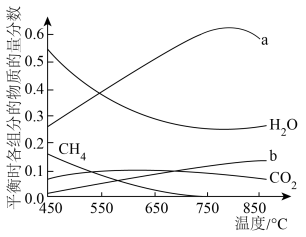
您最近一年使用:0次
2024-03-03更新
|
119次组卷
|
2卷引用: 北京市第十二中学2023-2024学年高二下学期开学考试化学试题
8 . 神舟十七号飞船的天线用钛镍记忆合金制造,工业上用钛酸亚铁(FeTiO3)冶炼钛(Ti)过程发生反应:FeTiO3+C+Cl2→TiCl4+FeCl3+CO(未配平)。下列说法正确的是
| A.C是氧化剂 |
| B.TiCl4是氧化产物 |
| C.生成3molCO时反应转移6mol电子 |
| D.配平后C和Cl2的化学计量数之比为6∶7 |
您最近一年使用:0次
2024-03-03更新
|
88次组卷
|
3卷引用:贵州省贵阳市白云区第二高级中学2023-2024学年高三上学期质量监测化学试卷
名校
解题方法
9 . 以金红石(主要成分为 ,含杂质
,含杂质 等)为原料“碳氯化法”高温生产钛的主要流程如下,下列说法错误的是
等)为原料“碳氯化法”高温生产钛的主要流程如下,下列说法错误的是

 ,含杂质
,含杂质 等)为原料“碳氯化法”高温生产钛的主要流程如下,下列说法错误的是
等)为原料“碳氯化法”高温生产钛的主要流程如下,下列说法错误的是
A.向粉碎后的固体中鼓入 使其“沸腾”有助于充分反应 使其“沸腾”有助于充分反应 |
B.在沸腾氯化炉中, 参加反应转移电子数为 参加反应转移电子数为 |
C.“碳氯化法”得到的 液体中混有杂质 液体中混有杂质 ,可蒸馏分离 ,可蒸馏分离 |
D.可用活泼金属 等在空气中加热还原 等在空气中加热还原 制备 制备 |
您最近一年使用:0次
解题方法
10 . 锰是冶金工业中不可缺少的添加剂,它的作用是增加合金金属材料的硬度、韧性、耐磨性和耐腐性,应用最广泛的有不锈钢、高锰钢、锰铝合金等。位于遵义市红花岗区坪桥工业园区的遵义天磁锰业集团有限公司就是一家电解锰公司;以碳酸锰为主要原料,其中含有少量铁、铝、钙、硅的氧化物或硫化物等杂质,以下是电解锰的简化工艺流程图:

(1)粉碎的目的___________ 。
(2)写出浸出时主要的离子反应___________ ,同时会产生的有毒气体是___________ 。
(3)加双氧水的作用方程式表示出来___________ 。
(4)加入氨水的作用是___________ ,除铁的离子反应___________ 。
(5)电解制锰的电极反应___________ ,当外电路转移2mol电子时,生成的气体是___________ ,在标准状况下的体积为___________ L,阳极液中产生的___________ 可循环使用。

(1)粉碎的目的
(2)写出浸出时主要的离子反应
(3)加双氧水的作用方程式表示出来
(4)加入氨水的作用是
(5)电解制锰的电极反应
您最近一年使用:0次



