解题方法
1 . 碳酸锌在工业上用途广泛。利用某种浸锌渣(主要含有 )制备
)制备 的一种流程如下:
的一种流程如下: ;
;
②室温下,部分离子浓度的对数 与
与 的关系如下图所示(其中
的关系如下图所示(其中 和
和 分别代表含铝、含硅和含锌微粒):
分别代表含铝、含硅和含锌微粒):
(1)“焙烧”时,金属硫化物均转化为氧化物,生成的气体 中主要成分是
中主要成分是______ (填化学式)。
(2)“碱浸”后,浸出液中含有金属元素的离子主要是 和
和______ (填离子符号);欲使浸出液中的含锌微粒完全沉淀,应调节 的范围是
的范围是______ 。
(3)浸渣回收银的过程中有配合物 生成,在碱性条件下用
生成,在碱性条件下用 还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为
还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为______ 。
(4)“除杂”时滤渣的主要成分是______ (填化学式)。
(5)“沉锌”时发生反应的离子方程式为______ ;此过程不宜用碳酸钠代替碳酸氢铵,原因是______ 。
 )制备
)制备 的一种流程如下:
的一种流程如下: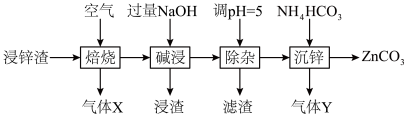
 ;
;②室温下,部分离子浓度的对数
 与
与 的关系如下图所示(其中
的关系如下图所示(其中 和
和 分别代表含铝、含硅和含锌微粒):
分别代表含铝、含硅和含锌微粒):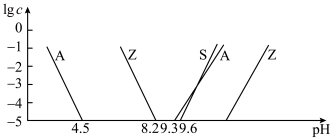
(1)“焙烧”时,金属硫化物均转化为氧化物,生成的气体
 中主要成分是
中主要成分是(2)“碱浸”后,浸出液中含有金属元素的离子主要是
 和
和 的范围是
的范围是(3)浸渣回收银的过程中有配合物
 生成,在碱性条件下用
生成,在碱性条件下用 还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为
还原该配合物,还原产物为银单质,同时放出N2,该反应中氧化剂与还原剂的物质的量之比为(4)“除杂”时滤渣的主要成分是
(5)“沉锌”时发生反应的离子方程式为
您最近半年使用:0次
名校
解题方法
2 . 我国最新型055型万吨驱逐舰上使用了最新一代国产有源相控阵雷达,采用了最先进的氮化镓( )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是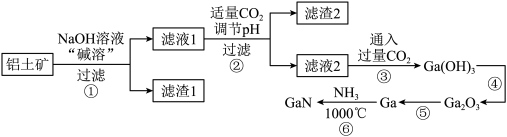
| A.可以通过粉碎铝土矿、搅拌等方法提高“碱溶”效率 |
B.由过程②、③可知, 的酸性比 的酸性比 强 强 |
C.已知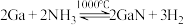 , , 与足量 与足量 反应,转移电子数为 反应,转移电子数为 |
D.滤渣1是 ,生成滤渣2的离子方程式可能为 ,生成滤渣2的离子方程式可能为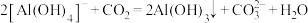 |
您最近半年使用:0次
3 . 实验室用磷矿脱镁废液制备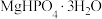 的实验过程可表示为
的实验过程可表示为 及少量
及少量 、
、 、
、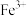 、
、 和
和 。
。
①向废液中加入 溶液调节
溶液调节 为
为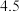 ,可达到
,可达到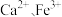 和
和 的最佳沉淀效果。其中
的最佳沉淀效果。其中 转化为
转化为 的离子方程式为
的离子方程式为_________ 。
②将除杂净化后的清液控制在一定温度,加入 浆液搅拌即可获得
浆液搅拌即可获得 固体。实验测得镁回收率、产品纯度与反应后溶液
固体。实验测得镁回收率、产品纯度与反应后溶液 关系如图所示。
关系如图所示。 小于6时,随着
小于6时,随着 增大,镁回收率上升,其原因是
增大,镁回收率上升,其原因是_______ 。 大于6时,随着
大于6时,随着 增大,产品纯度逐渐下降,其可能原因是
增大,产品纯度逐渐下降,其可能原因是_______ 。
(2)实验室用如下方案测定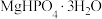 产品(含有
产品(含有 杂质)的纯度:准确称取
杂质)的纯度:准确称取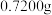 磷酸氢镁产品,加入足量稀硫酸溶解后配成
磷酸氢镁产品,加入足量稀硫酸溶解后配成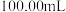 溶液。准确移取
溶液。准确移取 于锥形瓶中,用
于锥形瓶中,用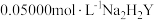 标准液滴定(离子方程式为
标准液滴定(离子方程式为 )至终点,平行滴定三次,平均消耗
)至终点,平行滴定三次,平均消耗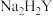 标准液
标准液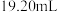 。计算该产品中
。计算该产品中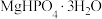 的纯度
的纯度_______ (写出计算过程)。
(3)恒温转化后的母液中主要含 和
和 。已知:水溶液中各含磷微粒的分布如图-2所示,
。已知:水溶液中各含磷微粒的分布如图-2所示, 和
和 的溶解度曲线如图-3所示;常温下
的溶解度曲线如图-3所示;常温下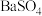 、
、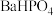 的溶度积常数依次为
的溶度积常数依次为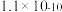 和
和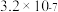 。请补充完整由恒温转化后的母液制备
。请补充完整由恒温转化后的母液制备 晶体的实验方案:用比浊法测定母液中
晶体的实验方案:用比浊法测定母液中 的浓度后,在搅拌下向一定体积的母液中
的浓度后,在搅拌下向一定体积的母液中_______ ,过滤、用无水乙醇洗涤,干燥。
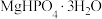 的实验过程可表示为
的实验过程可表示为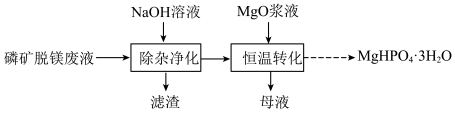
 及少量
及少量 、
、 、
、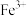 、
、 和
和 。
。①向废液中加入
 溶液调节
溶液调节 为
为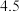 ,可达到
,可达到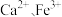 和
和 的最佳沉淀效果。其中
的最佳沉淀效果。其中 转化为
转化为 的离子方程式为
的离子方程式为②将除杂净化后的清液控制在一定温度,加入
 浆液搅拌即可获得
浆液搅拌即可获得 固体。实验测得镁回收率、产品纯度与反应后溶液
固体。实验测得镁回收率、产品纯度与反应后溶液 关系如图所示。
关系如图所示。 小于6时,随着
小于6时,随着 增大,镁回收率上升,其原因是
增大,镁回收率上升,其原因是
 大于6时,随着
大于6时,随着 增大,产品纯度逐渐下降,其可能原因是
增大,产品纯度逐渐下降,其可能原因是(2)实验室用如下方案测定
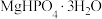 产品(含有
产品(含有 杂质)的纯度:准确称取
杂质)的纯度:准确称取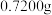 磷酸氢镁产品,加入足量稀硫酸溶解后配成
磷酸氢镁产品,加入足量稀硫酸溶解后配成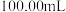 溶液。准确移取
溶液。准确移取 于锥形瓶中,用
于锥形瓶中,用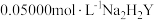 标准液滴定(离子方程式为
标准液滴定(离子方程式为 )至终点,平行滴定三次,平均消耗
)至终点,平行滴定三次,平均消耗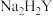 标准液
标准液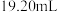 。计算该产品中
。计算该产品中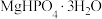 的纯度
的纯度(3)恒温转化后的母液中主要含
 和
和 。已知:水溶液中各含磷微粒的分布如图-2所示,
。已知:水溶液中各含磷微粒的分布如图-2所示, 和
和 的溶解度曲线如图-3所示;常温下
的溶解度曲线如图-3所示;常温下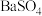 、
、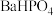 的溶度积常数依次为
的溶度积常数依次为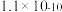 和
和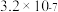 。请补充完整由恒温转化后的母液制备
。请补充完整由恒温转化后的母液制备 晶体的实验方案:用比浊法测定母液中
晶体的实验方案:用比浊法测定母液中 的浓度后,在搅拌下向一定体积的母液中
的浓度后,在搅拌下向一定体积的母液中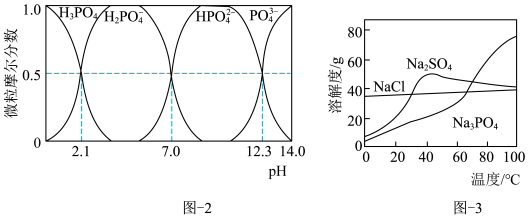
您最近半年使用:0次
名校
4 . 以硅藻土为载体的五氧化二钒(V2O3)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O3既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
以下是一种废钒催化剂回收工艺路线:
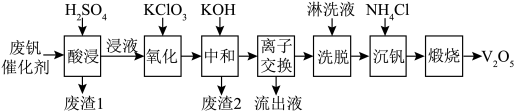
回答下列问题:
(1)“酸浸”时V2O5转化为 , 反应的离子方程式为
, 反应的离子方程式为___________ ,同时V2O4转化为 。“废渣1”的主要成分是
。“废渣1”的主要成分是______ 。
(2)“氧化”中使 变为
变为 , 则“氧化”环节中还原剂与氧化剂的物质的量之比为
, 则“氧化”环节中还原剂与氧化剂的物质的量之比为______ 。
(3)“中和”后的溶液中,钒主要以 形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
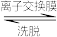
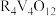 +
+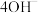 (以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈
(以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈_____ 性(填“敢”或“碱”)。
(4)检验“流出液”中含量最多的阳离子,其实验操作称为___ 。
(5)“煅烧”中发生反应的化学方程式 ,写出“沉钒”过程的离子方程式
,写出“沉钒”过程的离子方程式_________ 。
| 物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
| 质量分数/% | 2.20~2.90 | 2.8~3.32 | 22~28 | 60~65 | 1~2 | <1 |

回答下列问题:
(1)“酸浸”时V2O5转化为
 , 反应的离子方程式为
, 反应的离子方程式为 。“废渣1”的主要成分是
。“废渣1”的主要成分是(2)“氧化”中使
 变为
变为 , 则“氧化”环节中还原剂与氧化剂的物质的量之比为
, 则“氧化”环节中还原剂与氧化剂的物质的量之比为(3)“中和”后的溶液中,钒主要以
 形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
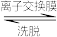
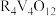 +
+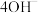 (以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈
(以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈(4)检验“流出液”中含量最多的阳离子,其实验操作称为
(5)“煅烧”中发生反应的化学方程式
 ,写出“沉钒”过程的离子方程式
,写出“沉钒”过程的离子方程式
您最近半年使用:0次
解题方法
5 . CH4既是一种重要的能源,也是一种重要的化工原料。
(1)已知8.0gCH4完全燃烧生成液体水放出444.8kJ热量。
CH4(g)+202(g)=CO2(g)+2H2O(1) ∆H=___________ kJ·mol-1。
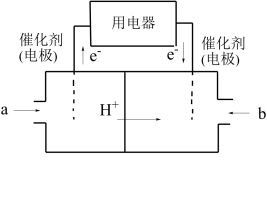
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为___________ ,通入b气体的电极反应式为___________ 。(质子交换膜只允许H'通过)___________ ℃左右。
②该反应催化剂的有效成分为CuAlO2,其用氧化物的形式表示为mCu2O·nAl2O3.m:n=___________ 。
(4)CH4还原法是处理NOx气体的一种方法。一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96LCH4可处理22.4LNOx,则x值为___________ 。
(1)已知8.0gCH4完全燃烧生成液体水放出444.8kJ热量。
CH4(g)+202(g)=CO2(g)+2H2O(1) ∆H=
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为
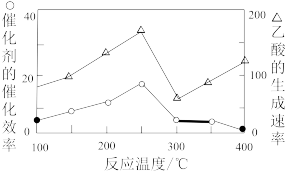
②该反应催化剂的有效成分为CuAlO2,其用氧化物的形式表示为mCu2O·nAl2O3.m:n=
(4)CH4还原法是处理NOx气体的一种方法。一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96LCH4可处理22.4LNOx,则x值为
您最近半年使用:0次
名校
6 . 为测定Cu和Cu2O混合粉末中Cu的含量。某同学将44.8g Cu和Cu2O混合粉末加入500mL 4.5mol/L的稀硝酸中,得到6.72LNO(标准状况下),忽略溶液体积的变化。下列说法正确的是
| A.反应后有固体剩余 | B.混合粉末中Cu的质量分数约为37% |
| C.反应后的溶液中c(Cu2+)=1.2mol/L | D.在反应后的溶液中加入足量铁粉,可置换出41.6g Cu |
您最近半年使用:0次
解题方法
7 . 草酸(H2C2O4)、草酸铵[(NH4)2C2O4]是重要的化合物。回答下列问题:
(1)实验表明,加热条件下,H2C2O4可分解生成CO2、CO和H2O。为了验证产物中的CO,设计如下实验装置:_______________ (装置可重复利用)。装置F中发生的化学反应方程式为_______________ 。
②能证明草酸晶体分解产物中有CO的现象是_______________ 。
(2)H2C2O4能与酸性高锰酸钾溶液反应,离子方程式为 。该反应中,还原剂为
。该反应中,还原剂为______________ (填化学式),若称取mg草酸晶体(H2C2O4·2H2O)粗产品,配成100mL溶液于锥形瓶中,加入V mL a mol·L-1KMnO4溶液,恰好完全反应,则该草酸晶体的纯度为______________ %[M(H2C2O4·2H2O)=126g·mol-1]。
(3)(NH4)2C2O4是良好的Co2+的沉淀剂,如下为(NH4)2C2O4加入CoSO4溶液中制备CoO的流程图:______________ (填化学式)。
②称量mg CoC2O4·2H2O[M(CoC2O4·2H2O)=183g·mol-1]“高温分解”,测得固体的失重率( )与温度的关系曲线如图所示:
)与温度的关系曲线如图所示:_______________ ;“高温分解”需控制的最低温度为_______________ (经测定290~890℃过程中产生的气体只有CO2)。
(1)实验表明,加热条件下,H2C2O4可分解生成CO2、CO和H2O。为了验证产物中的CO,设计如下实验装置:
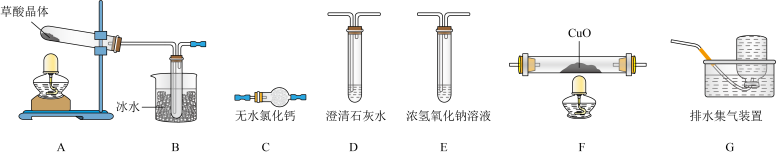
②能证明草酸晶体分解产物中有CO的现象是
(2)H2C2O4能与酸性高锰酸钾溶液反应,离子方程式为
 。该反应中,还原剂为
。该反应中,还原剂为(3)(NH4)2C2O4是良好的Co2+的沉淀剂,如下为(NH4)2C2O4加入CoSO4溶液中制备CoO的流程图:
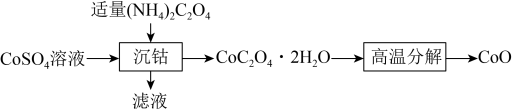
②称量mg CoC2O4·2H2O[M(CoC2O4·2H2O)=183g·mol-1]“高温分解”,测得固体的失重率(
 )与温度的关系曲线如图所示:
)与温度的关系曲线如图所示: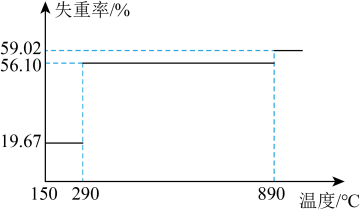
您最近半年使用:0次
解题方法
8 . 向含xmolHNO3和ymolH2SO4的混合稀溶液中缓慢加入铁粉,其氧化产物与所加铁粉的物质的量关系如图所示:
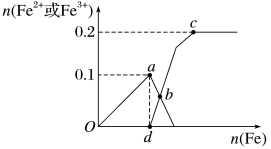
A.a点溶液中所含离子主要为Fe3+、 、 、 |
| B.dc段表示Fe2+物质的量变化,dc全段发生反应的离子方程式为Fe+2Fe3+=3Fe2+ |
| C.x=0.1,y=0.2 |
| D.反应至c点,可收集到标准状况下的气体体积为2.24L |
您最近半年使用:0次
名校
9 . 硝酸工业废气中一定量的NO和 能被足量的
能被足量的 溶液完全吸收,溶液中生成的
溶液完全吸收,溶液中生成的 和
和 两种离子的物质的量与废气中
两种离子的物质的量与废气中 的物质的量分数
的物质的量分数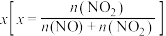 的关系如图。已知溶液中发生了两个反应:
的关系如图。已知溶液中发生了两个反应: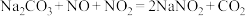 、
、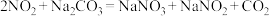 。下列说法错误的是
。下列说法错误的是
 能被足量的
能被足量的 溶液完全吸收,溶液中生成的
溶液完全吸收,溶液中生成的 和
和 两种离子的物质的量与废气中
两种离子的物质的量与废气中 的物质的量分数
的物质的量分数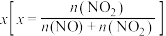 的关系如图。已知溶液中发生了两个反应:
的关系如图。已知溶液中发生了两个反应: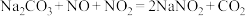 、
、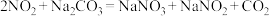 。下列说法错误的是
。下列说法错误的是
A.图中线段b表示 |
B.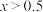 ,随x的增大,溶液中 ,随x的增大,溶液中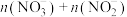 不变 不变 |
C.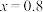 时,反应可收集到标准状况下 时,反应可收集到标准状况下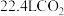 |
D.若所得溶液中 ,则 ,则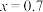 |
您最近半年使用:0次
名校
解题方法
10 . 向含 、
、 、
、 的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
 、
、 、
、 的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5,线段IV表示一种含氧酸,且I和IV表示的物质中含有相同的元素。下列说法不正确的是
A.原溶液中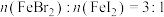 | B.线段II表示 的变化情况 的变化情况 |
C.线段IV表示 的变化情况 的变化情况 | D.根据图像可计算出a=5 |
您最近半年使用:0次



